Marktausblick für GMP-Biologika:
Der Markt für GMP-Biologika hatte 2025 ein Volumen von 71,45 Milliarden US-Dollar und wird bis 2035 voraussichtlich auf über 301,87 Milliarden US-Dollar anwachsen, was einer durchschnittlichen jährlichen Wachstumsrate (CAGR) von über 15,5 % im Prognosezeitraum 2026–2035 entspricht. Für das Jahr 2026 wird das Marktvolumen für GMP-Biologika auf 81,42 Milliarden US-Dollar geschätzt.

Der Markt für GMP-konforme Biologika verzeichnet ein deutliches Wachstum, angetrieben durch vielfältige Synergien, die die steigende Nachfrage nach qualitativ hochwertigen und konformen Biologika unterstreichen. Die zunehmende Verbreitung chronischer Erkrankungen wie Krebs und Autoimmunerkrankungen befeuert die Nachfrage nach innovativen biologischen Therapien. Darüber hinaus ergänzen höhere regulatorische Standards mit verbesserter Sicherheit und Wirksamkeit die Investitionen in modernste GMP-konforme Produktionsanlagen. So berichtete WuXi Biologics beispielsweise im Dezember 2024 über bedeutende Erfolge an seinem hochmodernen neuen Standort in Dundalk, Irland. In der Produktionsanlage MFG7 wurden mehrere Prozessleistungsqualifizierungsläufe (PPQ) mit jeweils 16.000 Litern erfolgreich abgeschlossen.
Darüber hinaus trägt die zunehmende Nutzung personalisierter Therapien sowie die Fortschritte in der Biologika-Pipeline etablierter und neu gegründeter Pharmaunternehmen zum steigenden Verbrauch von GMP-konformen Biologika bei. So wurde beispielsweise im August 2024 die Entwicklung von NECVAX-NEO1, einem oralen, bakteriellen DNA-Impfstoff, der auf patientenspezifische Tumor-Neoantigene abzielt, durch eine Kooperation zwischen AGC Biologics und NEC BioTherapeutics vorangetrieben. Durch die Nutzung der biotechnologischen Kompetenzen beider Unternehmen zielt diese bedeutende und vielversprechende Partnerschaft darauf ab, die Entwicklung personalisierter Krebstherapien zu verbessern. Wissenschaftliche Innovation und regulatorische Anforderungen entsprechen somit den Bedürfnissen des Marktes.
Schlüssel GMP-konforme Biologika Markteinblicke Zusammenfassung:
Regionale Einblicke:
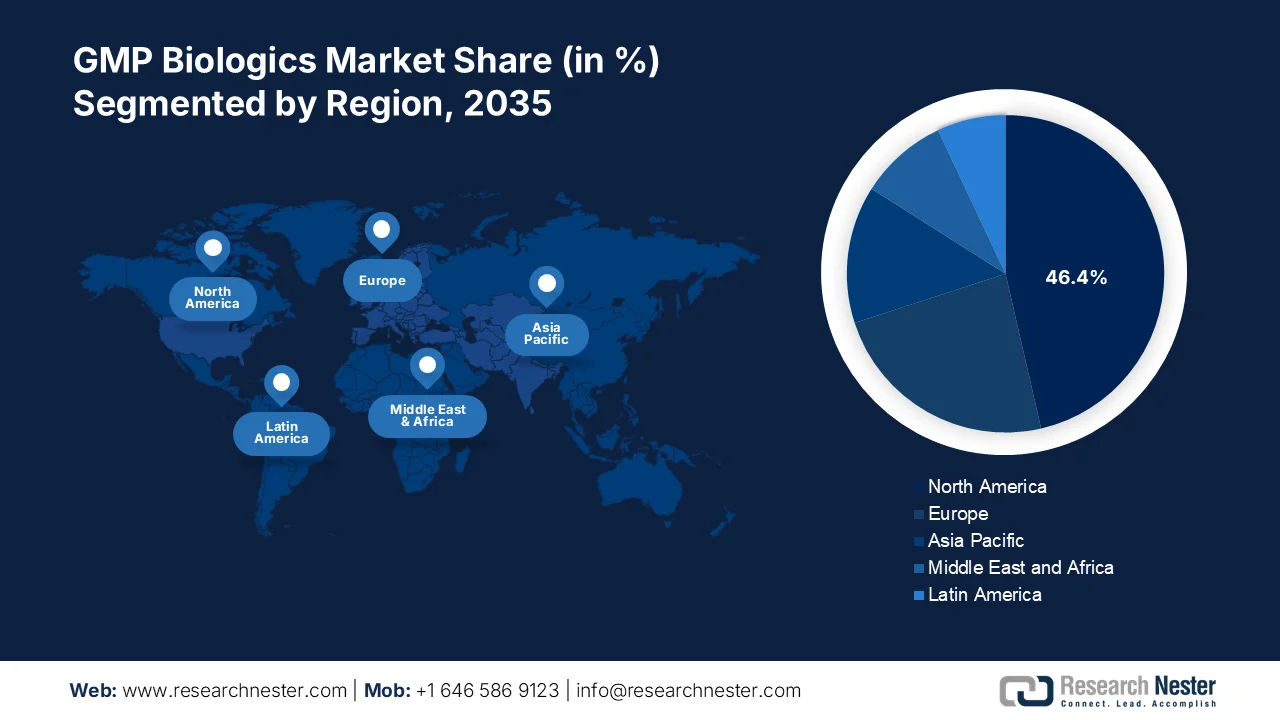
- Es wird erwartet, dass Nordamerika bis 2035 über 46,4 % des Umsatzes im GMP-Biologika-Markt erzielen wird, was auf Fortschritte in der Begleitdiagnostik und der personalisierten Medizin zurückzuführen ist.
- Für den asiatisch-pazifischen Raum wird bis 2035 das schnellste Wachstum des GMP-Biologika-Marktes erwartet, angetrieben durch eine robuste Produktionsinfrastruktur und unterstützende regulatorische Rahmenbedingungen, die die Vermarktung von Biologika fördern.
Segmenteinblicke:
- Es wird erwartet, dass das Segment der Krankenhäuser bis 2035 einen Anteil von mehr als 61,6 % am Markt für GMP-Biologika ausmachen wird, was auf die steigende Prävalenz von Krebs und anderen chronischen Krankheiten zurückzuführen ist, die eine Verabreichung von Biologika im Krankenhaus erfordern.
- Es wird erwartet, dass das Segment der monoklonalen Antikörper den Markt im Prognosezeitraum 2026–2035 anführen wird, angetrieben durch die steigende Nachfrage nach zielgerichteten Therapien und Fortschritte bei den mAb-Produktionstechnologien.
Wichtigste Wachstumstrends:
- Fortschritte in der Biotechnologie
- Zunehmende Auslagerung an Auftragsfertiger
Größte Herausforderungen:
- Kontaminationsrisiko
- Lange Entwicklungszeiten
Wichtige Akteure: Cisco Systems, Inc., Palo Alto Networks, Inc., Fortinet, Inc., IBM Corporation, Check Point Software Technologies Ltd., McAfee, LLC, Juniper Networks, Inc., Dell Technologies Inc., Hewlett Packard Enterprise Development LP, Broadcom Inc., FireEye, Inc., Symantec Corporation, F5 Networks, Inc., VMware, Inc.
Global GMP-konforme Biologika Markt Prognose und regionaler Ausblick:
Marktgröße und Wachstumsprognosen:
- Marktgröße 2025: 71,45 Milliarden US-Dollar
- Marktgröße 2026: 81,42 Milliarden US-Dollar
- Prognostizierte Marktgröße: 301,87 Milliarden US-Dollar bis 2035
- Wachstumsprognose: 15,5 % jährliches Wachstum (2026–2035)
Wichtigste regionale Dynamiken:
- Größte Region: Nordamerika (46,4 % Anteil bis 2035)
- Region mit dem schnellsten Wachstum: Asien-Pazifik
- Führende Länder: Vereinigte Staaten, Deutschland, Schweiz, Japan, Vereinigtes Königreich
- Schwellenländer: China, Indien, Japan, Südkorea, Brasilien
Last updated on : 27 February, 2026
GMP-Biologika-Markt – Wachstumstreiber und Herausforderungen
Wachstumstreiber
- Fortschritte in der Biotechnologie: Ein entscheidender Wachstumstreiber im Markt für GMP-konforme Biologika sind Fortschritte in der Biotechnologie. Sie ermöglichen die Entwicklung innovativerer und wirksamerer Therapien. So kündigte beispielsweise Poseida Therapeutics, Inc. im April 2024 an, Fortschritte in seiner einzigartigen, nicht-viralen Plattform für Gentechnik und Wirkstoffverabreichung zur Behandlung seltener Erkrankungen vorzustellen. Diese Fortschritte in der Entwicklung biologischer Arzneimittel sind wirksam bei komplexen, bisher nicht diagnostizierten Krankheitsbildern und eröffnen damit neue Märkte für GMP-konforme Biologika.
- Zunehmende Auslagerung an Auftragshersteller: Die Auslagerung an Auftragshersteller zählt zu den vielversprechendsten Wachstumstreibern im GMP-Biologika-Markt. Die Herstellung erfordert spezifische Fachkenntnisse und ist daher kostengünstig. So gab Samsung Biologics beispielsweise im Oktober 2024 einen Auftragsfertigungsvertrag mit einem asiatischen Pharmaunternehmen im Wert von 1,24 Milliarden US-Dollar bekannt. Dieser Vertrag wird die Einführung hochwertiger und effizienter Biopharmazeutika ermöglichen. Dadurch erhält das Unternehmen Zugang zu erstklassigen Fertigungskapazitäten und verkürzt die Markteinführungszeit. Zudem wird die Konzentration auf Kernkompetenzen durch die strikte Einhaltung regulatorischer Anforderungen sichergestellt.
Herausforderungen
- Kontaminationsrisiko: Das größte Problem im GMP-konformen Markt für Biologika ist die Kontamination, vor allem aufgrund der Komplexität und Sensibilität des Herstellungsprozesses. Da diese Arzneimittel aus lebenden Organismen gewonnen werden, erfordern sie eine streng kontrollierte Umgebung, um mikrobielle, partikuläre oder virale Kontaminationen zu vermeiden. Bereits geringfügige Abweichungen vom strengen Reinheitsprotokoll können die Produktqualität und die Patientensicherheit gefährden und kostspielige Rückrufe sowie behördliche Strafen nach sich ziehen. Daher ist die Einhaltung strenger Kontaminationskontrollmaßnahmen in jeder Phase des Produktionsprozesses für Unternehmen der Biologika-Industrie sehr komplex und mit einem hohen operativen und finanziellen Aufwand verbunden.
- Lange Entwicklungszeiten: Die größte Herausforderung des Marktes sind die langen Entwicklungszeiten, da der Entwicklungsprozess von Biologika komplex und sehr zeitaufwendig ist. Biologika erfordern umfangreiche Forschung, klinische Prüfungen und strenge Scale-up-Prozesse, um Sicherheit, Wirksamkeit und die Einhaltung regulatorischer Vorgaben zu gewährleisten. Die Notwendigkeit hochpräziser Optimierung in Zellkultur, Proteinexpression und Aufreinigungsprozessen sowie langwierige Zulassungsverfahren verlängern die Entwicklungszyklen von Biologika um mehrere Jahre. Diese Verzögerungen verzögern den Markteintritt und erhöhen die finanzielle Belastung.
Marktgröße und Prognose für GMP-Biologika:
| Berichtsattribut | Einzelheiten |
|---|---|
|
Basisjahr |
2025 |
|
Prognosejahr |
2026–2035 |
|
CAGR |
15,5 % |
|
Marktgröße im Basisjahr (2025) |
71,45 Milliarden US-Dollar |
|
Prognostizierte Marktgröße (2035) |
301,87 Milliarden US-Dollar |
|
Regionaler Geltungsbereich |
|
Marktsegmentierung für GMP-Biologika:
Anwendungssegmentanalyse
Prognosen zufolge werden Krankenhäuser bis 2035 einen Marktanteil von über 61,6 % im Bereich der GMP-konformen Biologika halten. Moderne Biologika wie monoklonale Antikörper, Gentherapien und individualisierte Therapien werden hauptsächlich in Krankenhäusern verabreicht, insbesondere zur Behandlung von Erkrankungen wie Krebs, Autoimmunerkrankungen und genetischen Krankheiten. Diese Erkrankungen nehmen zu und lassen sich in Krankenhäusern besser behandeln. Beispielsweise gaben die National Institutes of Health im Januar 2024 bekannt, dass im Jahr 2020 fast 10 Millionen Menschen an Krebs gestorben sind. Bis 2040 wird ein Anstieg der Krebsfälle um mehr als 40 % erwartet. Zwischen 2020 und 2050 werden die geschätzten globalen Kosten für Krebs 25 Billionen US-Dollar übersteigen.
Typensegmentanalyse
Aufgrund des Produkttyps dürfte das Segment der monoklonalen Antikörper den Markt für GMP-Biologika im Prognosezeitraum dominieren, da monoklonale Antikörper bei den meisten chronischen und tödlichen Erkrankungen, darunter Krebs, Autoimmunerkrankungen und Infektionskrankheiten, weit verbreitet sind. Fortschritte in der mAb-Produktionstechnologie, die steigende Nachfrage nach zielgerichteten Therapien und die zunehmenden Zulassungen beschleunigen die Markteinführung von mAbs. So wurde beispielsweise im September 2023 SUREmAb von KBI Biopharma, Inc. eingeführt. SUREmAb basiert auf der SUREtechnology-Plattform von KBI für die effiziente, sichere und kostengünstige Entwicklung und Herstellung monoklonaler Antikörper (mAbs). SUREmAb ist ein vertikal integriertes, globales Angebot, das die Entwicklungszeiten für internationale Biopharmazeutika-Hersteller verkürzen soll.
Unsere detaillierte Analyse des globalen Marktes umfasst die folgenden Segmente:
Anwendung |
|
Typ |
|

Vishnu Nair
Leiter - Globale GeschäftsentwicklungPassen Sie diesen Bericht an Ihre Anforderungen an – sprechen Sie mit unserem Berater für individuelle Einblicke und Optionen.
GMP-Biologika-Markt – Regionale Analyse
Einblicke in den nordamerikanischen Markt
Der nordamerikanische Markt für GMP-konforme Biologika wird bis 2035 voraussichtlich einen Umsatzanteil von über 46,4 % erreichen. Das Marktwachstum ist auf Fortschritte in der Begleitdiagnostik und der personalisierten Medizin zurückzuführen. Darüber hinaus tragen der Einsatz monoklonaler Antikörper und Biosimilars, technologische Entwicklungen in der Bioprozessierung sowie der zunehmende Fokus auf individualisierte Therapien zu einer steigenden Nachfrage bei. Diese Entwicklungen führen zu einer erhöhten Nachfrage nach biologischen Produkten, da sie Behandlungen effizienter und zielgerichteter machen.
Der US-amerikanische Markt für GMP-konforme Biologika wächst exponentiell aufgrund eines deutlichen Anstiegs der Forschungs- und Entwicklungsaktivitäten im Bereich Biopharmazeutika. So beschloss beispielsweise Bionova Scientific im Juni 2024, einen neuen Geschäftsbereich für Dienstleistungen mit Plasmid-DNA zu eröffnen und eigens dafür eine Anlage in Texas, USA, zu errichten. Zusätzliche Wachstumschancen ergaben sich durch den Ausbau etablierter Geschäftsbereiche wie Planova™-Virusentfernungsfilter und den Einstieg in die CRO- (Auftragsforschungsinstitute) und CDMO-Branchen (Auftragsentwicklungs- und -herstellungsunternehmen), wobei das Unternehmen seinen Kundenstamm und seine starke Marke nutzte.
Der kanadische Markt für GMP-konforme Biologika verzeichnet ein bemerkenswertes Wachstum, bedingt durch den Ausbau von Produktionsanlagen im Bereich der Biologika. So kündigte beispielsweise Eurofins CDMO Alphora Inc. im September 2024 den Bau einer neuen GMP-konformen Produktionsanlage für Biologika (ca. 4.645 m²) in Mississauga, Ontario, an. In dieser Anlage sollen monoklonale Antikörper (mAbs) und Proteintherapien für klinische und kommerzielle Anwendungen hergestellt werden. Die Investition wird von der kanadischen Bundesregierung und durch Mittel aus dem Strategic Initiative Fund (SIF) gefördert. Die Anlage soll die Bioproduktionskapazitäten Kanadas stärken und gleichzeitig das Biologika-Ökosystem und die Beschäftigungsbasis in Kanada festigen.
Einblicke in den asiatisch-pazifischen Markt
Der asiatisch-pazifische Raum wird voraussichtlich bis 2035 der am schnellsten wachsende Markt für GMP-konforme Biologika sein. Modernste Produktionsstätten, Lieferketten und Forschungsinstitute bilden die solide Infrastruktur der Region, die für die Herstellung und den Vertrieb von Biologika unerlässlich ist. Das Wachstum der Region wird zudem durch eine starke regulatorische Grundlage gefördert, die die Zulassung und Vermarktung biologischer Arzneimittel unterstützt. Darüber hinaus treibt die Entwicklung neuartiger Biologika für vielfältige therapeutische Zwecke den Bedarf an GMP-konformer Produktion voran.
Der indische Markt für GMP-konforme Biologika wird aufgrund regulatorischer Maßnahmen und förderlicher Regierungspolitik zur Innovation und Entwicklung biotechnologischer Verfahren im medizinischen Bereich voraussichtlich deutlich wachsen. So erteilte die Europäische Arzneimittel-Agentur (EMA) Biocon Biologics Ltd (BBL) im Juni 2024 die Genehmigung zur Herstellung des Biosimilars Bevacizumab in ihrer hochmodernen Produktionsstätte für monoklonale Antikörper (mAbs) in Bengaluru. Diese Zulassung wird die Versorgung von Patienten in allen europäischen Märkten erheblich verbessern.
Der Markt für GMP-konforme Biologika in China verzeichnet bemerkenswerte Wachstumschancen und dürfte die Aktivitäten des Landes im Bereich Biologika weiter intensivieren. So führte WuXi Biologics beispielsweise im August 2023 die erste Scale-up-Produktion von 2.000 Litern Wirkstoff (DS) nach GMP-Richtlinien durch. Dabei nutzte das Unternehmen seine hochentwickelte Fed-Batch-Plattform WuXiUI™, die eine Vervierfachung der Produktivität gegenüber dem herkömmlichen Fed-Batch-Verfahren ermöglichte. Darüber hinaus fördern Fortschritte im Bereich der Biologika das Ökosystem und tragen so zu weiteren Entwicklungen und besseren Ergebnissen bei.
Akteure auf dem GMP-Biologika-Markt:
- Novartis AG
- Unternehmensübersicht
- Geschäftsstrategie
- Wichtigste Produktangebote
- Finanzielle Leistung
- Wichtigste Leistungsindikatoren
- Risikoanalyse
- Aktuelle Entwicklung
- Regionale Präsenz
- SWOT-Analyse
- Pfizer Inc.
- Sanofi
- GlaxoSmithKline plc
- Johnson & Johnson
- Eli Lilly and Company
- Samsung Biologics Co. Ltd.
- WuXi AppTec
Die starke Präsenz von Pharmaunternehmen im Markt für GMP-konforme Biologika prägt die Landschaft, indem sie die Dynamik des wachsenden Bedarfs an neuartigen und wirksamen Medikamenten bewältigen. So gab beispielsweise Immunity Bio, Inc. im Mai 2024 eine Partnerschaft mit dem Serum Institute of India (SII) zur Verfügbarkeit von BCG bekannt. Dies sichert dem Unternehmen eine substanzielle Erstversorgung mit ANKTIVA für klinische Studien und die kommerzielle Anwendung, noch bevor die eigenen Abfüll- und Wirkstoffproduktionsanlagen in New York und Kalifornien vollständig in Betrieb sind.
Hier ist die Liste einiger wichtiger Akteure:
Neueste Entwicklungen
- Im November 2024 erhielt die Aurobindo Pharma-Tochtergesellschaft CuraTeQ Biologics von der Europäischen Arzneimittel-Agentur (EMA) ein GMP-Konformitätszertifikat für ihre Produktionsstätte für Biosimilars.
- Im März 2024 gab Aragen Biologics Pvt Ltd. bekannt, dass die erste Phase ihrer Produktionsanlage für Biologika in Bangalore, Indien (Investition: 30 Millionen US-Dollar), in Betrieb genommen wurde. Zur Herstellung eines neuartigen monoklonalen Antikörpers (mAb) gegen Krebs hat das Unternehmen außerdem sein erstes Kleinserienprojekt für eine US-amerikanische Organisation abgeschlossen.
- Report ID: 6963
- Published Date: Feb 27, 2026
- Report Format: PDF, PPT
- Entdecken Sie eine Vorschau auf die wichtigsten Markttrends und Erkenntnisse
- Prüfen Sie Beispiel-Datentabellen und Segmentaufgliederungen
- Erleben Sie die Qualität unserer visuellen Datendarstellungen
- Bewerten Sie unsere Berichtsstruktur und Forschungsmethodik
- Werfen Sie einen Blick auf die Analyse der Wettbewerbslandschaft
- Verstehen Sie, wie regionale Prognosen dargestellt werden
- Beurteilen Sie die Tiefe der Unternehmensprofile und Benchmarking
- Sehen Sie voraus, wie umsetzbare Erkenntnisse Ihre Strategie unterstützen können
Entdecken Sie reale Daten und Analysen
Häufig gestellte Fragen (FAQ)
GMP-konforme Biologika Umfang des Marktberichts
Die kostenlose Stichprobe umfasst aktuelle und historische Marktgrößen, Wachstumstrends, regionale Diagramme und Tabellen, Unternehmensprofile, segmentweise Prognosen und mehr.
Kontaktieren Sie unseren Experten
Urheberrecht © 2026 Research Nester. Alle Rechte vorbehalten.




