Marktaussichten für die Behandlung von Gonorrhö:
Der Markt für Gonorrhöbehandlungen hatte im Jahr 2025 ein Volumen von 1,39 Milliarden US-Dollar und wird bis Ende 2035 voraussichtlich auf 2,8 Milliarden US-Dollar anwachsen, was einem durchschnittlichen jährlichen Wachstum von 7,2 % im Prognosezeitraum 2026–2035 entspricht. Im Jahr 2026 wird das Marktvolumen für Gonorrhöbehandlungen auf 1,49 Milliarden US-Dollar geschätzt.
Der globale Markt für Gonorrhö-Behandlungen wächst stetig. Laut WHO wurden 2020 weltweit rund 82,4 Millionen neue Fälle gemeldet. Auch in den USA ist ein allmählicher Anstieg der gemeldeten Fälle zu verzeichnen: 2021 wurden 710.151 Fälle registriert, was 214 Fällen pro 100.000 Einwohner entspricht. Diese stark wachsende Patientenzahl beeinflusst die Nachfrage nach Antibiotika und Diagnostika und erhöht gleichzeitig den Druck auf die Lieferkette für pharmazeutische Wirkstoffe und Medizinprodukte. Die Lieferkette ist stark von Rohstoffen abhängig, die aus asiatischen Produktionszentren, insbesondere aus China und Indien, bezogen werden.
Gemeldete Fälle und Melderaten nach Bundesstaat, nach Raten geordnet, USA, 2021
Rang | Zustand | Fälle | Rate pro 100.000 Einwohner |
1 | Mississippi | 12.617 | 427,7 |
2 | Süd-Dakota | 3.258 | 363,9 |
3 | Louisiana | 16.390 | 354,5 |
4 | Alabama | 16.191 | 321.3 |
5 | South Carolina | 16.052 | 309.2 |
6 | Georgia | 31.996 | 296,3 |
7 | North Carolina | 28.612 | 271.2 |
8 | Arkansas | 8.176 | 270.2 |
9 | Nevada | 8.488 | 270,0 |
10 | Alaska | 1.977 | 269,8 |
11 | Tennessee | 18.768 | 269.1 |
12 | Oklahoma | 10.273 | 257,7 |
13 | Missouri | 15.714 | 254,8 |
14 | Arizona | 18.426 | 253.2 |
15 | Illinois | 30.454 | 240.3 |
16 | New Mexico | 5.080 | 240.1 |
17 | Ohio | 27.838 | 236,3 |
18 | Kalifornien | 91.461 | 233.1 |
19 | Norddakota | 1.735 | 223,9 |
20 | Texas | 64.623 | 218,9 |
21 | Michigan | 21.954 | 218.4 |
22 | New York | 43.048 | 217,0 |
— | US GESAMT | 710.151 | 214,0 |
Quelle: CDC

Markt für Gonorrhoe-Behandlungen – Wachstumstreiber und Herausforderungen
Wachstumstreiber ?
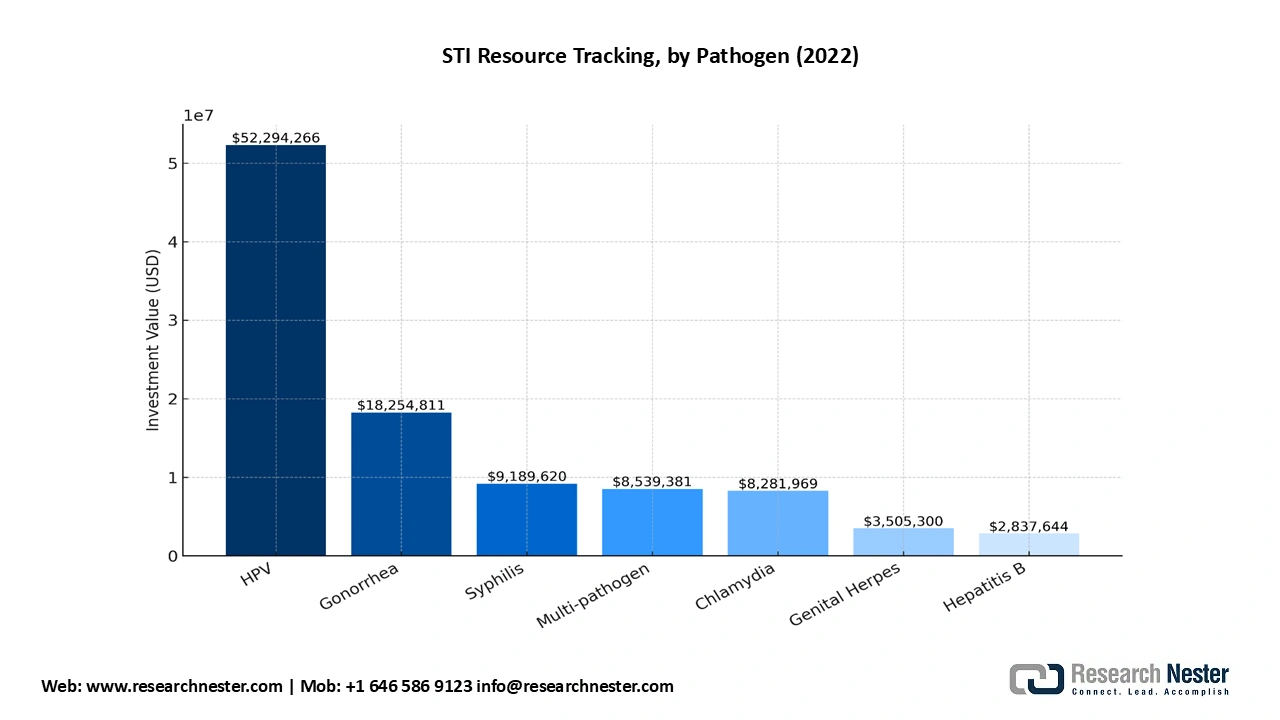
Zunehmende Prävalenz und wachsender Patientenstamm: Vor der COVID-19-Pandemie stiegen die Chlamydien-Inzidenzraten um 1 % pro Monat (95 %-KI: 1,01–1,01; RR = 1,01) und waren um 3 % höher pro 1.000 US-Dollar zusätzlicher ICD-Finanzierung (95 %-KI: 1,01–1,06; RR = 1,03) pro Kopf. Die Gonorrhö-Raten stiegen vierteljährlich um 1 % (95 %-KI: 0,98–1,05; RR = 1,01) und waren bei höheren ICD-Investitionen pro Kopf um 6 % höher (95 %-KI: 1,01–1,11; RR = 1,06). Höhere Chlamydien-Raten spiegeln einen geringeren Rückgang der Chlamydienfälle in den öffentlichen Gesundheitseinrichtungen wider. Die US-amerikanischen National Institutes of Health (NIH) und die Bill & Melinda Gates Foundation gehören zu den größten Investoren in die Forschung und Entwicklung im Gesundheitswesen und verfolgen die Finanzierungstrends in der Produktentwicklung sowie in der Impfstoff- und Diagnostikforschung für häufige sexuell übertragbare Infektionen (STI) wie Gonorrhö, Syphilis, Chlamydien, Hepatitis B, humane Papillomviren (HPV), Genitalherpes und Trichomoniasis. Laut dem AVAC-Bericht 2024 flossen 51 % der Mittel in die HPV-Forschung und -Entwicklung, wobei Gonorrhö und Syphilis 2022 zu den am höchsten finanzierten Forschungsbereichen zählten.
Unterbrochene Zeitreihe der vierteljährlich bestätigten Gonorrhoefälle bei Jugendlichen im Alter von 13 bis 19 Jahren während der COVID-19-Pandemie in Ontario, Kanada.
Variablen | aRR | 95 % KI |
Zeit | 1.01 | 0,98, 1,05 |
Pandemie | 0,51 | 0,04, 7,22 |
Zeit und Pandemie | 1.01 | 0,91, 1,13 |
ICD-Finanzierung | 1,06 | 1.01, 1.11 |
ICD-Finanzierung und Zeit | 1,00 | 0,99, 1,00 |
Niveauwechsel: ICD-Finanzierung und Pandemie | 1.11 | 0,92, 1,33 |
Steigungsänderung: Zeit, Pandemie und ICD-Finanzierung | 0,99 | 0,99, 1,00 |
- Staatliche und Medicare-Ausgaben für die Behandlung im Rahmen der Arzneimittelentwicklung und klinischen Studien: Laut dem AVAC-Bericht 2024 wurden 18 Millionen US-Dollar für die Forschung und Entwicklung von Gonorrhö-Impfstoffen, 50 Millionen US-Dollar für HPV-Impfstoffe, 9 Millionen US-Dollar für Syphilis-Impfstoffe, 3,5 Millionen US-Dollar für Genitalherpes-Impfstoffe, 8 Millionen US-Dollar für Chlamydien-Impfstoffe und 2,8 Millionen US-Dollar für Hepatitis-B-Impfstoffe aufgewendet. Von den gesamten Investitionen in die Diagnostik entfielen 66 % auf die Forschung und Entwicklung von Impfstoffen gegen mehrere Krankheitserreger (einschließlich Gonorrhö, Chlamydien, Syphilis und Genitalherpes). 103 Millionen US-Dollar wurden für die Forschung und Entwicklung von Impfstoffen gegen sexuell übertragbare Infektionen (STI) bereitgestellt, davon 6,8 Millionen US-Dollar (7 %) für die Diagnostikforschung und 93 Millionen US-Dollar (90 %) für die Impfstoffentwicklung. Die National Institutes of Health (NIH) trugen beachtliche 73 % der Investitionen in die diagnostische Forschung und Entwicklung. Darüber hinaus erhielt das Zentrum für Translationale Immunologie des Instituts für Biomedizinische Wissenschaften an der Georgia State University im September 2022 einen fünfjährigen Bundeszuschuss in Höhe von 4,9 Millionen US-Dollar, um Neisseria gonorrhoeae und die Ernährungsimmunität zu erforschen, die das mikrobielle Wachstum durch Aushungern eindringender Krankheitserreger verhindert.
Medikamente zur Behandlung von Gonorrhö fallen unter die Medicare-Teil-D-Arzneimittel. Bis die voraussichtlichen Selbstbeteiligungskosten oder die Preise der Kostenträger im Jahr 2025 2.000 US-Dollar und im Jahr 2026 schätzungsweise 2.100 US-Dollar erreichen, werden Medikamente, die von Medicare Teil D abgedeckt werden, als Zuzahlung vom Patienten getragen. Dies gilt sowohl für Generika als auch für Markenmedikamente.
Quelle: AVAC
Zusammenfassung der klinischen Studie
- NCT04010539 (Gepotidacin vs Ceftriaxon + Azithromycin)
Feld | Detail |
Offizieller Titel | Eine randomisierte, multizentrische, offene Phase-III-Studie an Jugendlichen und Erwachsenen zum Vergleich der Wirksamkeit und Sicherheit von Gepotidacin mit Ceftriaxon plus Azithromycin bei der Behandlung unkomplizierter urogenitaler Gonorrhö, verursacht durch Neisseria gonorrhoeae |
Sponsor / Verantwortliche Partei | GlaxoSmithKline (GSK) |
Studientyp | Interventionell (klinische Studie) |
Phase | Phase 3 |
Design (gesamt) | Randomisierte, multizentrische, offene, parallele Zuteilung |
Zuweisung | Randomisiert |
Hauptzweck | Behandlung |
Zustand / Indikation | Unkomplizierte urogenitale Gonorrhö (Neisseria gonorrhoeae) |
Interventionen / Waffen | Experimentell: Gepotidacin - oral: 3000 mg (4 × 750 mg Tabletten) zu Studienbeginn (Tag 1) am Studienort; zweite orale Dosis von 3000 mg (4 × 750 mg) selbstverabreicht 10-12 Stunden später. |
Primärer Endpunkt | Anzahl der Teilnehmer mit kulturell bestätigter bakterieller Eradikation von N. gonorrhoeae im Urogenitalbereich beim Kontrollbesuch (Tag 4–8). (Gemessene Ausgangswerte → Kontrollbesuch) |
Wichtigste sekundäre Ergebnisparameter | Kulturbestätigte bakterielle Eradikation aus dem Rektalbereich (TOC Tag 4-8); aus dem Rachenbereich (TOC Tag 4-8); Anzahl der Teilnehmer mit behandlungsbedingten unerwünschten Ereignissen (TEAEs) und schwerwiegenden unerwünschten Ereignissen (SAEs) (bis zu 21 Tage); Veränderungen der hämatologischen und klinisch-chemischen Parameter gegenüber dem Ausgangswert; Ergebnisse der Urinanalyse; Vitalzeichen. |
Teilnahmeberechtigung - Alter | ≥ 12 Jahre |
Teilnahmeberechtigung - Geschlecht | Alle Geschlechter sind teilnahmeberechtigt. |
Einschreibungen (tatsächlich) | 628 Teilnehmer (tatsächlich) |
Studienbeginn (tatsächlich) | 21.10.2019 |
Primärer Fertigstellungsgrad (tatsächlich) | 10.10.2023 |
Studienabschluss (tatsächlich) | 10.10.2023 |
Anzahl der Standorte | 51 Standorte (die aufgeführten Länder umfassen: USA, Australien, Deutschland, Mexiko, Spanien, Vereinigtes Königreich – mehrere Städte pro Land, wie angegeben) |
Wichtige Ausschlussbeispiele | Aktuelle Epididymitis/Orchitis; Verdacht auf/bestätigte Chlamydia-trachomatis-Infektion, die eine unaufschiebbare Behandlung erfordert; BMI ≥40 oder ≥35 mit Komorbidität; bekannte Überempfindlichkeit gegenüber den Studienmedikamenten; Immunschwäche; signifikante Nieren-/Leberfunktionsstörung; kürzliche Exposition gegenüber dem Prüfpräparat; QT-Verlängerung oder Anwendung von QT-verlängernden Arzneimitteln; Schwangerschaft/Stillzeit. |
Bemerkenswerte Inklusionsbeispiele | Klinischer Verdacht auf eine urogenitale Gonokokkeninfektion (oder kürzlich positive Kultur/NAAT bis zu 5-7 Tage zurück); Bereitschaft, während der gesamten Behandlung auf sexuelle Aktivitäten zu verzichten oder Kondome zu benutzen; Körpergewicht >45 kg; Fähigkeit zur informierten Einwilligung/Zustimmung. |
Sicherheitsüberwachung | TEAEs / SAEs wurden bis zu 21 Tage lang erfasst; Laborwerte, Urinanalysen, Vitalparameter, EKG-Screening / QTc-Spezifikation waren Ausschlusskriterien. |
Ergebnisse veröffentlicht / Datum | Ergebnisse erstmals eingereicht: 01.05.2024; Ergebnisse erstmals veröffentlicht: 30.05.2024; Letzte Aktualisierung: 30.05.2024; Letzte Überprüfung: April 2024 |
Hinweis zu Regulierungs- und Gerichtsbarkeitsbestimmungen | Untersucht ein von der US-amerikanischen FDA reguliertes Arzneimittel (Aufzeichnungshinweis) |
Andere Kennungen | Weitere Studienkennnummern: 116577; EudraCT-Nummer: 2018-001780-23 |
Anmerkungen / zusätzliche Hinweise (aus dem Protokoll) | Offene Phase-3-Nichtunterlegenheitsstudie; Vergleichsregime: 500 mg Ceftriaxon i.m. + 1000 mg Azithromycin als Einzeldosis; Ergebnisse und Begleitdokumente (Protokoll, SAP) sind über den ClinicalTrials.gov-Datensatz und das Datenaustauschportal des Sponsors verfügbar. |
Quelle: ClinicalTrials.gov
2. NCT05027516 (ResistAZM)
Feld | Wert |
Studientitel (kurz) | Studie zum Vergleich von Ceftriaxon plus Azithromycin versus Ceftriaxon allein zur Behandlung von Gonorrhö (ResistAZM) |
Offizieller Titel | Eine offene, randomisierte, kontrollierte Studie zum Vergleich der Wirkung von Ceftriaxon plus Azithromycin versus Ceftriaxon allein zur Behandlung von Neisseria gonorrhoeae auf das Resistom |
Sponsor / Verantwortliche Partei | Institut für Tropenmedizin, Belgien |
Studientyp | Interventionell |
Phase | Phase 4 |
Studienstatus (aus den Unterlagen) | Abgeschlossen (Ergebnisse veröffentlicht) – letzte Aktualisierung: 02.08.2024 |
Kurzzusammenfassung | Randomisierte, kontrollierte Studie mit 42 Männern mit Gonorrhoe in der ITM-STI/HIV-Ambulanz; Randomisierung im Verhältnis 1:1 zu Ceftriaxon allein oder Ceftriaxon + Azithromycin; Nachuntersuchung an Tag 14 zur Beurteilung der Heilung und Überwachung des Mikrobioms/Resistoms. Primärer Endpunkt ist die Differenz in der Häufigkeit von Resistenzgenen im rektalen Mikrobiom an Tag 14. |
Bedingungen | Neisseria gonorrhoeae (Gonorrhö) |
Andere Studien-ID-Nummern | ITM202101 |
Studienbeginn (tatsächlich) | 17.01.2022 |
Primärer Fertigstellungsgrad (tatsächlich) | 09.05.2022 |
Studienabschluss (tatsächlich) | 09.05.2022 |
Einschreibungen (tatsächlich) | 42 |
Anzahl der Standorte / Land | 1. Standort – Institut für Tropenmedizin, Antwerpen, Belgien |
Berechtigte Altersgruppen | 18 Jahre und älter |
Berechtigte Geschlechter | Männlich (Einschluss: männliches Geschlecht bei Geburt) |
Gesunde Freiwillige werden angenommen? | NEIN |
Geschlechtsbasierte Anspruchsberechtigung | Ja – die Einbeziehung ist auf das männliche Geschlecht bei der Geburt beschränkt. |
Zuweisung | Randomisiert |
Interventionsmodell | Parallelzuweisung |
Maskierung | Vierergruppe (Teilnehmer; Pflegekraft; Prüfarzt; Ergebnisbeurteiler) |
Hauptzweck | Unterstützende Pflege |
Interventionen / Waffen (Details) | Arm 1 (Aktiver Vergleichsstoff - Rocephin): Ceftriaxon 1 g + Lidocain 35 mg, intramuskuläre Injektion (Einzeldosis). |
Primärer Endpunkt | Makrolidresistenzdeterminanten: Verhältnis der mittleren Anzahl an Makrolidresistenzdeterminanten-Messungen in anorektalen Proben an Tag 14 zwischen der Ceftriaxon/Azithromycin-Gruppe und der Ceftriaxon-Gruppe. Zeitraum: Tag 14. |
Wichtigste sekundäre Ergebnisparameter | Zählung der Resistenzdeterminanten für jede Nicht-Makrolid-Antibiotikaklasse (Tag 14); Erwerb phänotypischer Resistenz gegen Azithromycin durch N. gonorrhoeae in Morbidostat nach Exposition gegenüber kommensalen Neisseria-DNA-Extrakten aus jeder Behandlungsgruppe (Tag 0 und Tag 14). |
Highlights der Inklusion (aus den Unterlagen) | Fähigkeit und Bereitschaft zur Abgabe einer schriftlichen Einverständniserklärung; männliches Geschlecht bei Geburt; ≥ 18 Jahre; bestätigte Diagnose einer Urethritis, Proktitis oder Pharyngitis aufgrund von N. gonorrhoeae (symptomatisch oder asymptomatisch) durch positiven NAAT oder (bei Urethritis) positiven Gram-/Methylenblau-Färbung. |
Ausschlussmerkmale (aus dem Datensatz) | Anwendung von Makrolid-Antibiotika in den letzten 6 Monaten; bekannte Kontraindikationen/Allergie gegen Ceftriaxon, Azithromycin oder Lidocain; Vorliegen einer anderen Erkrankung/anderen sexuell übertragbaren Infektion, die bei Studieneinschluss wahrscheinlich ein anderes Antibiotikum erfordern wird, nach Einschätzung des behandelnden Arztes. |
IPD-Sharing-Plan | Nein (Plan für individuelle Teilnehmerdaten: Nein) |
Datum der Ergebnismeldung (aus den Aufzeichnungen) | Ergebnisse erstmals eingereicht: 05.06.2023; Ergebnisse erstmals eingereicht, die die Qualitätskriterien erfüllten: 15.02.2024; Ergebnisse erstmals veröffentlicht: 02.08.2024; Letzte Aktualisierung veröffentlicht: 02.08.2024; Letzte Überprüfung: Februar 2024. |
Anmerkungen / Kommentare (aus dem Protokoll) | Der primäre Endpunkt konzentriert sich auf das Resistom (Determinanten der Makrolidresistenz) in anorektalen Proben an Tag 14; kleine randomisierte kontrollierte Studie (n=42), die darauf abzielte, die Auswirkungen der Hinzunahme von Azithromycin zur Ceftriaxon-Therapie auf das Mikrobiom/Resistom zu bewerten. |
Quelle: ClinicalTrials.gov
Herausforderungen
Preisbeschränkungen durch staatliche Gesundheitssysteme: Staatliche Preisobergrenzen schränken die Rentabilität in verschiedenen entwickelten Märkten ein. Die gesetzliche Krankenversicherung in Deutschland hat die Erstattungsgrenzen für Antibiotika begrenzt und damit die Gewinnmargen der Anbieter minimiert. Diese Herausforderungen erschweren es den Herstellern, ihre Investitionen in Forschung und Entwicklung wieder hereinzuholen. Andererseits wirken solche Preisregulierungen, die auf die Kontrolle öffentlicher Ausgaben abzielen, als Hemmnisse für den Markteintritt und die Innovation im Bereich der Gonorrhö-Behandlung. Laut Europäischer Kommission behindern diese Maßnahmen insbesondere die Markteinführung neuer Medikamente in Therapiegebieten wie sexuell übertragbaren Infektionen.
Marktgröße und Prognose für die Behandlung von Gonorrhö:
| Berichtsattribut | Einzelheiten |
|---|---|
|
Basisjahr |
2025 |
|
Prognosejahr |
2026–2035 |
|
CAGR |
7,2 % |
|
Marktgröße im Basisjahr (2025) |
1,39 Milliarden US-Dollar |
|
Prognostizierte Marktgröße (2035) |
2,8 Milliarden US-Dollar |
|
Regionaler Geltungsbereich |
|
Marktsegmentierung der Gonorrhoe-Behandlung:
Segmentanalyse der Wirkstoffklassen
Antibiotika werden den Markt für Gonorrhöbehandlungen mit einem globalen Marktanteil von 65,2 % im Jahr 2030 dominieren. Dieser Markt wird hauptsächlich durch die stetige Verbesserung der klinischen Wirksamkeit und die weltweite Akzeptanz von Wirkstoffen wie Cephalosporinen und Makroliden angetrieben. Laut Berichten der WHO und des CDC werden diese Wirkstoffe aufgrund zunehmender Antibiotikaresistenzen häufig in Kombinationstherapien eingesetzt. Innovationen in der Entwicklung neuer Medikamente prägen den Markt für Gonorrhöbehandlungen und die zukünftige Behandlungslandschaft, insbesondere bei multiresistenten Fällen.
Segmentanalyse der Behandlungsarten
Die duale Therapie dominiert den Markt für Gonorrhöbehandlungen und wird voraussichtlich einen Marktanteil von 55,2 % erreichen, vor allem durch die Kombination von Ceftriaxon und Azithromycin. Aufgrund ihrer nachgewiesenen Wirksamkeit gegen Stämme von Neisseria gonorrhoeae bleibt die duale Therapie die erste Wahl in der Gonorrhöbehandlung. Laut Bericht der WHO und des CDC begegnet dieses Behandlungsschema der zunehmenden Herausforderung der Antibiotikaresistenz durch die Nutzung zweier unterschiedlicher Wirkmechanismen und reduziert somit das Risiko einer Reinfektion und von Therapieversagen.
Unsere detaillierte Analyse des globalen Marktes für Gonorrhoe-Behandlungen umfasst die folgenden Segmente: ?
Segment | Teilsegment |
Wirkstoffklasse |
|
Behandlungsart |
|
Verabreichungsweg |
|
Infektionsart |
|

Vishnu Nair
Leiter - Globale GeschäftsentwicklungPassen Sie diesen Bericht an Ihre Anforderungen an – sprechen Sie mit unserem Berater für individuelle Einblicke und Optionen.
Markt für Gonorrhoe-Behandlungen – Regionale Analyse
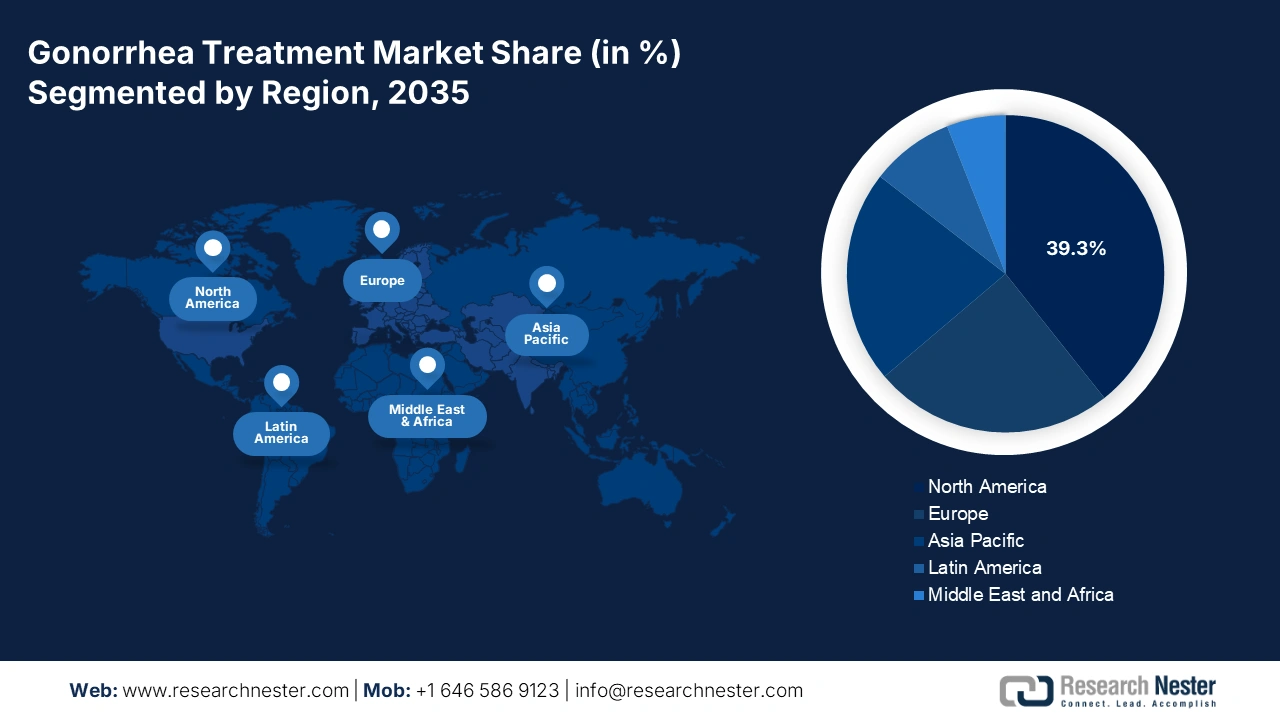
Einblicke in den nordamerikanischen Markt
Nordamerika ist führend auf dem Markt für Gonorrhö-Behandlungen und wird voraussichtlich einen Marktanteil von 39,3 % erreichen, bedingt durch die steigende Zahl von Patienten mit antibiotikaresistenter Gonorrhö. Mit zunehmender Patientenzahl steigt auch der Bedarf an Investitionen in effektive Diagnostik und Therapieverfahren. Durch die verstärkte Anwendung von Nukleinsäureamplifikationstests (NAAT) und Investitionen in Cephalosporin-basierte und duale Antibiotikatherapien positioniert sich Nordamerika an der Spitze der Behandlungsinnovation. Sowohl in den USA als auch in Kanada ist ein Anstieg der Fälle von antibiotikaresistenter Gonorrhö zu verzeichnen.
Der US-amerikanische Markt für Gonorrhöbehandlungen wächst rasant, parallel zu den steigenden Fallzahlen mit 714.000 Fällen im Jahr 2021. Laut CDC wurden die Mittel für sexuell übertragbare Infektionen (STI) im Rahmen von Initiativen zur öffentlichen Gesundheitsvorsorge und Forschung & Entwicklung erhöht. Der US-Kongress stellte 2023 1,39 Milliarden US-Dollar für die STI-Prävention bereit. Nukleinsäureamplifikationstests (NAATs) gelten weiterhin als Goldstandard in der Diagnostik und machen einen erheblichen Anteil aller klinischen Labortests aus. PhRMA und NIH arbeiten mit der US-Regierung zusammen, um die Entwicklung von Antibiotika-Kombinationstherapien zu beschleunigen und die Überwachung von Antibiotikaresistenzen zu verbessern.
Einblicke in den europäischen Markt
Europa ist der am schnellsten wachsende Markt für Gonorrhöbehandlungen und wird voraussichtlich bis 2035 einen Anteil von 24,3 % erreichen. Der europäische Markt für Gonorrhöbehandlungen expandiert insbesondere aufgrund zunehmender Antibiotikaresistenzen, steigender Prävalenz sexuell übertragbarer Infektionen und verstärkter Maßnahmen im Bereich der öffentlichen Gesundheit. Innovationen und Trends in diesem Markt, wie die Nutzung digitaler Gesundheitsplattformen und E-Rezepte, verbessern den Zugang zu Behandlungen für Jugendliche und Risikogruppen. Darüber hinaus nimmt das Engagement nationaler Gesundheitsbehörden zu, was die Verbreitung von Behandlungen in Krankenhäusern, Kliniken und Online-Apotheken fördert.
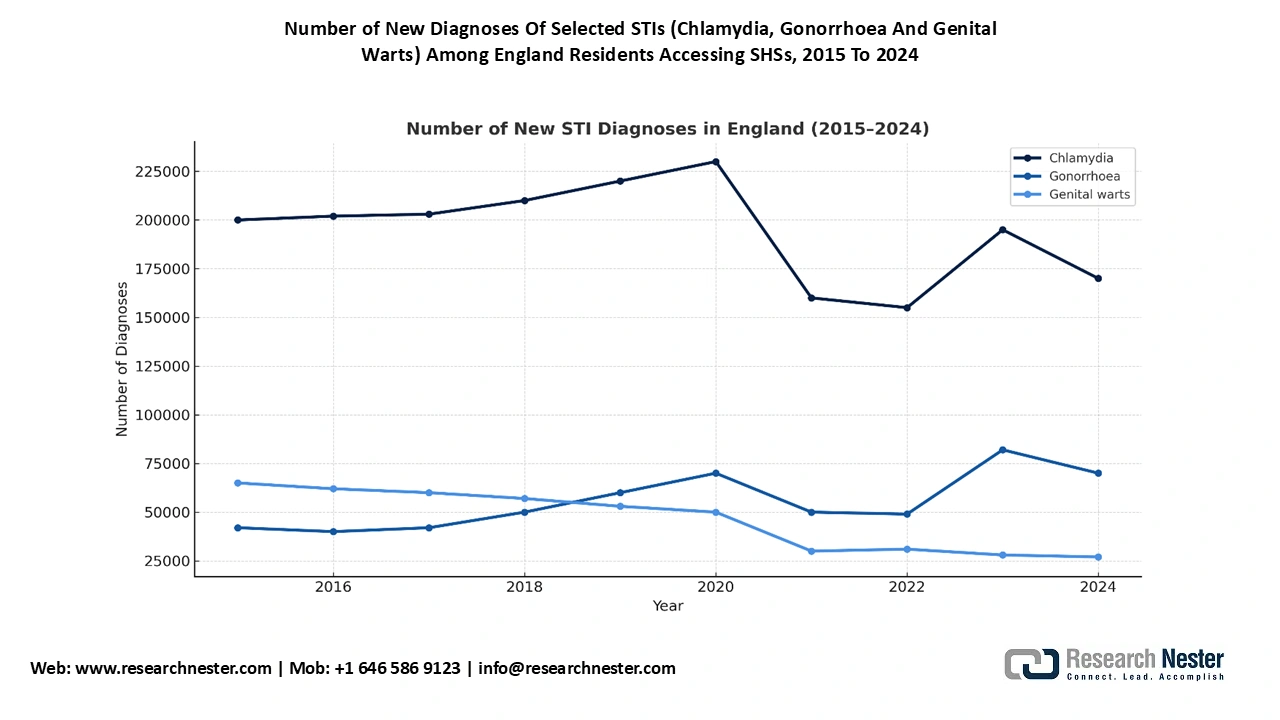
Quelle: Regierung des Vereinigten Königreichs
Es wird erwartet, dass Großbritannien im Jahr 2035 mit einem Umsatzanteil von 24,4 % den Markt für Gonorrhöbehandlungen anführen wird. Laut der Local Government Association wurden 2021 in den nationalen Einrichtungen für sexuelle und reproduktive Gesundheit (SRH) 4.002.827 Beratungen durchgeführt, was einem Anstieg von 15,7 % gegenüber 2020 und von 36 % seit 2013 entspricht. Darüber hinaus wurden 2021 in den SRH-Einrichtungen 1.949.940 Untersuchungen zur sexuellen Gesundheit durchgeführt, darunter auch diagnostische Tests auf Gonorrhö, Chlamydien, Syphilis und HIV. Dies bedeutet einen Anstieg von 18,7 % gegenüber 2020 und ein Wachstum von 29 % im Vergleich zu 2013. Der Markt für Gonorrhöbehandlungen in Großbritannien wird durch die kontinuierlich steigenden öffentlichen Investitionen und die rasche Verbreitung digitaler Gesundheitsdienste angetrieben. Großbritannien bleibt der größte Markt für die Behandlung von Gonorrhö in Europa, was auf den Anstieg der STI-Prävalenz, insbesondere bei Personen im Alter von 16 bis 30 Jahren, zurückzuführen ist.
Wichtige Akteure auf dem Markt für Gonorrhoe-Behandlungen:
- Unternehmensübersicht
- Geschäftsstrategie
- Wichtigste Produktangebote
- Finanzielle Leistung
- Wichtigste Leistungsindikatoren
- Risikoanalyse
- Aktuelle Entwicklung
- Regionale Präsenz
- SWOT-Analyse
Der globale Markt für Gonorrhö-Behandlungen ist hart umkämpft, und verschiedene Akteure konkurrieren mit innovativen Antibiotika, Kombinationstherapien und Diagnostika. Führende Unternehmen wie Pfizer, GSK und Merck treiben den Markt für Gonorrhö-Behandlungen voran, indem sie in die Entwicklung von Zweifachtherapien investieren und ihre Kapazitäten ausbauen. Gleichzeitig dominieren indische Hersteller wie Cipla und Sun Pharma den Markt, indem sie die Verfügbarkeit in Entwicklungsländern fördern. Darüber hinaus schafft die Wettbewerbsfähigkeit führender Innovatoren vielfältige Chancen entlang der gesamten Wertschöpfungskette.
Hier ist eine Liste der wichtigsten Akteure auf dem Markt für Gonorrhoe-Behandlungen:
Firmenname (Land) | Marktanteil (Schätzung 2035) |
Pfizer Inc. (USA) | 8,6 % |
GlaxoSmithKline plc (UK) | 7,1 % |
Merck & Co., Inc. (USA) | 6,7 % |
F. Hoffmann-La Roche AG (Schweiz) | 6,2 % |
Astellas Pharma Inc. (Japan) | 5,3 % |
Sanofi SA (Frankreich) | xx% |
Bayer AG (Deutschland) | xx% |
AbbVie Inc. (USA) | xx% |
Takeda Pharmaceutical Co. Ltd. (Japan) | xx% |
Cipla Ltd. (Indien) | xx% |
Sun Pharmaceutical Industries Ltd. (Indien) | xx% |
Hikma Pharmaceuticals (UK/Jordanien) | xx% |
Dr. Reddy's Laboratories Ltd. (Indien) | xx% |
Daiichi Sankyo Co., Ltd. (Japan) | xx% |
Lupin Ltd. (Indien) | xx% |
Celltrion Inc. (Südkorea) | xx% |
Biocon Ltd. (Indien) | xx% |
CSL Limited (Australien) | xx% |
Aurobindo Pharma (Indien) | xx% |
Pharmaniaga Berhad (Malaysia) | xx% |
Nachfolgend sind die von den einzelnen Unternehmen im Markt für Gonorrhoe-Behandlungen abgedeckten Bereiche aufgeführt:
Neueste Entwicklungen
- Im Mai 2025 kündigte Roche den Start seiner Phase-3-Studie mit Zosurabalpin an. Der Beginn dieser Studie wird für 2026 erwartet.
- Im April 2024 genehmigte die US-amerikanische Arzneimittelbehörde FDA Zevtera zur Injektion (Ceftobiprolmedocaril-Natrium) oder Ceftriaxon, das sowohl für Erwachsene als auch für Kinder mit ambulant erworbener bakterieller Pneumonie (CARP) geeignet ist.
- Report ID: 7808
- Published Date: Oct 03, 2025
- Report Format: PDF, PPT
- Entdecken Sie eine Vorschau auf die wichtigsten Markttrends und Erkenntnisse
- Prüfen Sie Beispiel-Datentabellen und Segmentaufgliederungen
- Erleben Sie die Qualität unserer visuellen Datendarstellungen
- Bewerten Sie unsere Berichtsstruktur und Forschungsmethodik
- Werfen Sie einen Blick auf die Analyse der Wettbewerbslandschaft
- Verstehen Sie, wie regionale Prognosen dargestellt werden
- Beurteilen Sie die Tiefe der Unternehmensprofile und Benchmarking
- Sehen Sie voraus, wie umsetzbare Erkenntnisse Ihre Strategie unterstützen können
Entdecken Sie reale Daten und Analysen
Häufig gestellte Fragen (FAQ)
Gonorrhoe-Behandlung Umfang des Marktberichts
Die kostenlose Stichprobe umfasst aktuelle und historische Marktgrößen, Wachstumstrends, regionale Diagramme und Tabellen, Unternehmensprofile, segmentweise Prognosen und mehr.
Kontaktieren Sie unseren Experten




