Перспективы рынка программного обеспечения для сопоставления клинических испытаний:
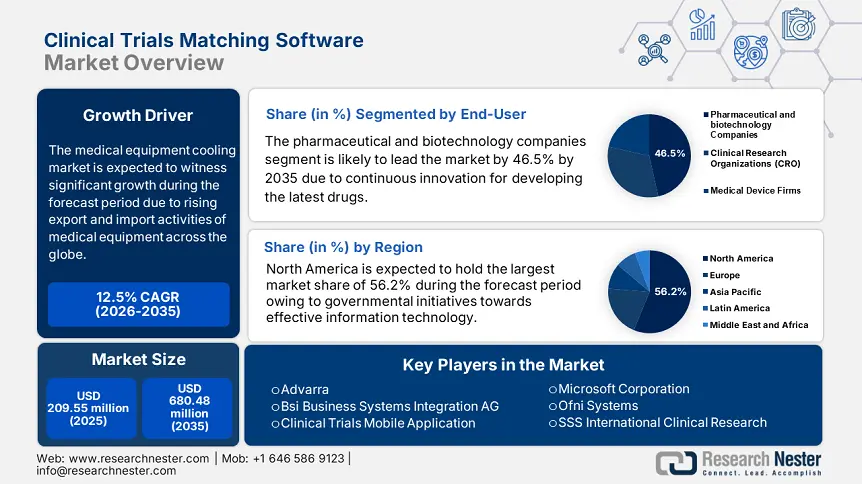
Объем рынка программного обеспечения для сопоставления результатов клинических испытаний в 2025 году оценивался в 209,55 млн долларов США и, как ожидается, достигнет 680,48 млн долларов США к 2035 году, увеличиваясь на уровне около 12,5% в год в прогнозируемый период, то есть с 2026 по 2035 год. В 2026 году объем рынка программного обеспечения для сопоставления результатов клинических испытаний оценивается в 233,12 млн долларов США.
Внедрение автоматизированных программных инструментов в клинические исследования обеспечивает эффективный метод быстрого выявления пациентов, потенциально подходящих для участия в клинических исследованиях, что в значительной степени способствует развитию рынка программного обеспечения для сопоставления данных клинических исследований. Согласно статье, опубликованной NLM в феврале 2023 года, клиническое исследование состоит из различных фаз: фазы 0 (исследовательская), фазы Ia, Ib и Ic (нетерапевтическое исследование), фазы II, IIa и IIb (исследовательское исследование), фазы III (терапевтическое подтверждающее исследование) и фазы IV (пострегистрационное исследование). Таким образом, сочетание всех этих фаз и включение инновационных программных инструментов достаточно эффективно для расширения рынка.
Рынок программного обеспечения для сопоставления данных клинических исследований переживает бурный рост благодаря использованию технологий и вычислительных машин для оценки вероятности исследования, упрощения набора и ведения участников, обеспечения доступа к различным группам населения, рационализации сбора данных и упрощения управления данными. В связи с этим внедрение компьютеров и наборов инструментов в клинические исследования является исключительно распространенным, что повышает спрос на них. Согласно отчету OEC за 2023 год, мировой объем торговли компьютерами составил 323 млрд долларов США, при этом Китай является крупнейшим экспортером с объемом 158 млрд долларов США, а США — крупнейшим импортером с объемом 93,2 млрд долларов США.
Более того, использование наборов инструментов в клинических исследованиях полезно для эффективного управления исследовательскими операциями, данными и коммуникацией на протяжении всего жизненного цикла исследования, что способствует развитию рынка программного обеспечения, соответствующего клиническим исследованиям. Кроме того, они способствуют внедрению изменений в практику и могут включать стратегии внедрения руководств, информирования о политике и предоставления качественных материалов для аудита. Согласно отчёту OEC за 2023 год, объём международной торговли наборами инструментов оценивается в 1,29 млрд долларов США, при этом Китай является крупнейшим экспортёром с объёмом 606 млн долларов США, а Германия — крупнейшим импортёром с объёмом 114 млн долларов США, что положительно влияет на рост рынка.
Сравнение экспорта/импорта компьютеров и наборов инструментов
Страны | Компьютеры | Наборы инструментов | ||
Экспорт | Импорт | Экспорт | Импорт | |
Мексика | 29,5 млрд долларов США | - | - | - |
Тайбэй | 27,1 млрд долларов США | - | 158,0 млн долларов США | - |
Вьетнам | 15,9 млрд долларов США | - | - | - |
Соединенные Штаты | 15,3 млрд долларов США | 93,2 млрд долларов США | 59,6 млн долларов США | 82,4 млн долларов США |
Германия | - | 20,4 млрд долларов США | 147,0 млн долларов США | 114,0 млн долларов США |
Гонконг | - | 15,5 млрд долларов США | - | - |
Нидерланды | - | 14,3 млрд долларов США | 29,3 млн долларов США | 68,4 млн долларов США |
Соединенное Королевство | - | 13,0 млрд долларов США | - | - |
Россия | - | - | - | 114,0 млн долларов США |
Франция | - | - | - | 93,7 млн долларов США |
Источник: OEC 2023
Ключ Программное обеспечение для сопоставления клинических испытаний Сводка рыночной аналитики:
Региональные особенности:
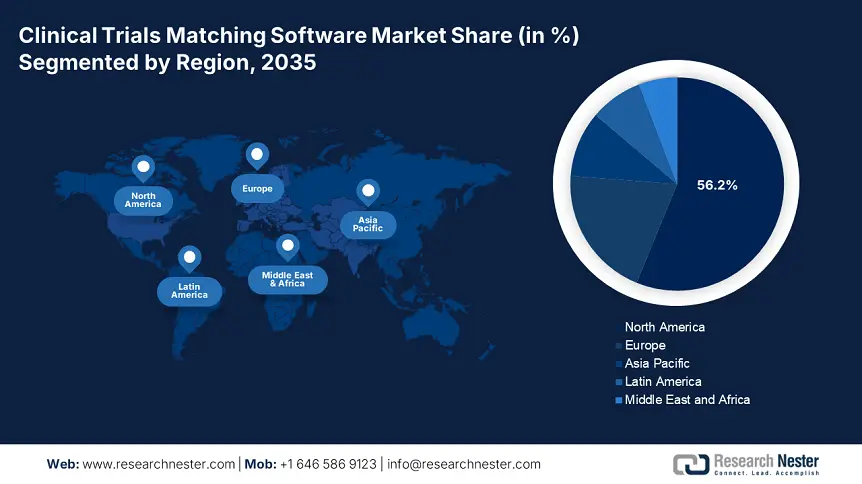
- Северная Америка занимает 56,20% рынка программного обеспечения для сопоставления данных клинических испытаний. Это обусловлено принятием систем сопоставления данных клинических испытаний лекарственных препаратов, государственными стратегиями и инициативами Национальных институтов здравоохранения, что гарантирует уверенный рост к 2035 году.
- Ожидается, что рынок программного обеспечения для сопоставления данных клинических испытаний в Азиатско-Тихоокеанском регионе будет расти самыми быстрыми темпами к 2035 году благодаря наличию большого количества пациентов и росту числа ИТ-проектов в сфере здравоохранения.
Анализ сегмента:
- Прогнозируется, что к 2035 году доля фармацевтических и биотехнологических компаний на рынке превысит 46,5%, что обусловлено большим количеством испытаний лекарственных препаратов, необходимых для их вывода на рынок.
- Прогнозируется значительный рост сегмента программного обеспечения в период с 2026 по 2035 год, что обусловлено более широким использованием и внедрением испытаний лекарственных препаратов, проведением исследований и разработок, а также щедрыми взносами медицинских организаций.
Основные тенденции роста:
- Расширение активности клинических исследований
- Цифровизация исследований
Основные проблемы:
- Дорогое программное обеспечение
- Недостаточный уровень обучения и адаптации
- Ключевые игроки:Advarra, Antidote Technologies, Inc., IBM Clinical Development, мобильное приложение Clinical Trials.
Глобальный Программное обеспечение для сопоставления клинических испытаний Рынок Прогноз и региональный обзор:
Прогнозы размера рынка и роста:
- Объем рынка в 2025 году: 209,55 млн долларов США
- Объем рынка в 2026 году: 233,12 млн долларов США
- Прогнозируемый размер рынка: 680,48 млн долларов США к 2035 году
- Прогнозы роста: 12,5% CAGR (2026–2035 гг.)
Ключевая региональная динамика:
- Крупнейший регион: Северная Америка (доля 56,2 % к 2035 году).
- Самый быстрорастущий регион: Азиатско-Тихоокеанский регион.
- Доминирующие страны: США, Германия, Япония, Великобритания, Франция.
- Развивающиеся страны: Китай, Индия, Бразилия, Россия, Мексика.
Last updated on : 26 August, 2025
Факторы роста и проблемы рынка программного обеспечения для сопоставления клинических испытаний:
Драйверы роста
- Рост активности клинических испытаний: Ожидается, что рынок программного обеспечения для сопоставления результатов клинических испытаний будет расти в зависимости от расширения масштабов клинических испытаний на международном уровне. Согласно отчёту ВОЗ за декабрь 2024 года, в США количество испытаний увеличилось на 186 497, за ними следуют Китай (135 747), Индия (74 031), Япония (65 167), Германия (54 902) и многие другие страны. Это обусловлено растущим проникновением передовых медицинских технологий в сочетании с растущим спросом на инновационные препараты с высокой эффективностью, что значительно ускоряет развитие и развитие рынка.
- Цифровизация в исследованиях: Внедрение сложных технологий, таких как системы электронного сбора данных (EDC) и системы управления клиническими испытаниями, увеличивает спрос на программное обеспечение для клинических испытаний во всем мире. Согласно статье, опубликованной в журнале Mayo Clinic Proceedings в октябре 2023 года, 94% больниц в США активно используют электронные медицинские карты (ЭМК) для оказания медицинской помощи, что составляет 45% от общей численности пациентов в регионе, имеющих медицинские карты в ЭМК. Электронные медицинские карты изначально задумывались как инструмент для оказания медицинской помощи, ориентированной на пациента, но клинические исследователи воспользовались их практически повсеместным внедрением в различных аспектах исследований.
Проблемы
- Дорогое программное обеспечение: Высокая стоимость систем сопоставления данных фактически сдерживает рост рынка программного обеспечения для сопоставления данных клинических исследований. Некоторые аспекты программного обеспечения, такие как стоимость установки, стоимость каждого пользователя, договорные обязательства, стоимость исследования, стоимость обслуживания, обучения, поддержки и системной интеграции, в совокупности увеличивают общую стоимость внедрения программных решений для сопоставления данных клинических исследований. Кроме того, организации взимают плату за настройку и конфигурирование в зависимости от конкретных организационных и исследовательских требований.
- Недостаточная подготовка и адаптация: Медицинские работники могут не иметь необходимой подготовки для эффективного использования передовых инструментов сопоставления данных клинических исследований, что ограничивает их потенциальную пользу. Более того, сложные исследования часто включают множество переменных и строгие критерии отбора, что затрудняет разработку специалистами программных решений для точного и эффективного сопоставления данных пациентов. Это создает пробелы в общем процессе проведения исследований, что приводит к получению неполных результатов и, таким образом, сдерживает развитие мирового рынка программного обеспечения для сопоставления данных клинических исследований.
Объем и прогноз рынка программного обеспечения для сопоставления клинических испытаний:
| Атрибут отчёта | Детали |
|---|---|
|
Базовый год |
2025 |
|
Прогнозируемый период |
2026-2035 |
|
CAGR |
12,5% |
|
Размер рынка базового года (2025) |
209,55 млн долларов США |
|
Прогнозируемый размер рынка на год (2035) |
680,48 млн долларов США |
|
Региональный охват |
|
Сегментация рынка программного обеспечения для сопоставления клинических испытаний:
Конечный пользователь (фармацевтические и биотехнологические компании, организации клинических исследований (CRO), компании-производители медицинских приборов)
Ожидается, что к 2035 году сегмент фармацевтических и биотехнологических компаний займет более 46,5% рынка программного обеспечения для клинических испытаний. Развитие этого сегмента объясняется большим количеством испытаний лекарственных препаратов, необходимых для вывода продукта на рынок. Например, согласно отчёту Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) за апрель 2024 года, Центр инноваций в области клинических испытаний (CDER) успешно запустил Центр инноваций в области клинических испытаний (C3T1), призванный стимулировать революционные инициативы и служить центром координации, обмена знаниями и взаимодействия как с внутренними, так и с внешними организациями. Таким образом, это развитие, осуществляемое совместно с FDA, является огромным вкладом в развитие рынка во всем мире.
Компоненты ( программное обеспечение, услуги )
Ожидается, что сегмент программного обеспечения окажет значительное влияние на рынок программного обеспечения для клинических исследований в течение прогнозируемого периода. Этот рост объясняется расширением использования и внедрения испытаний лекарственных препаратов, проведением исследований и разработок, а также щедрыми взносами медицинских организаций в поддержку и проведение сложных испытаний лекарственных препаратов. Например, как указано в статье, опубликованной в журнале Drug Discovery Today в феврале 2025 года, средняя вероятность первого одобрения составляет 14,3% в ведущих фармацевтических компаниях, специализирующихся на научных исследованиях, и варьируется от 8% до 23%. Таким образом, это обеспечивает общий уровень успешности клинических разработок от 7% до 25%.
Наш углубленный анализ мирового рынка программного обеспечения для сопоставления данных клинических испытаний включает следующие сегменты:
Конечный пользователь |
|
Компоненты |
|
Режим развертывания |
|

Vishnu Nair
Руководитель глобального бизнес-развитияНастройте этот отчет в соответствии с вашими требованиями — свяжитесь с нашим консультантом для получения персонализированных рекомендаций и вариантов.
Региональный анализ рынка программного обеспечения для сопоставления клинических испытаний:
Анализ рынка Северной Америки
К концу 2035 года доля рынка программного обеспечения для сопоставления данных клинических испытаний в Северной Америке составит около 56,2% от общего объема продаж. Такие факторы, как принятие систем сопоставления данных испытаний лекарственных препаратов биотехнологическими и фармацевтическими организациями, государственные стратегии и внедрение программного обеспечения для сопоставления данных пациентов, а также программного обеспечения для сопоставления данных клинических испытаний, значительно способствуют расширению рынка в регионе. Например, в сентябре 2024 года Национальный институт здравоохранения (NIH) запустил ряд инициатив, включая «Базовые экспериментальные исследования с участием людей» (BESH), обзоры, финансирование и практики на основе клинических испытаний, формы информации о людях, шаблоны протоколов, а также обучение и ресурсы, необходимые для развития рынка.
Рынок программного обеспечения для сопоставления результатов клинических испытаний в США набирает обороты благодаря разработке соответствующих руководящих принципов административными органами. Например, Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) в своем отчете за сентябрь 2022 года предложило включить в раздел 201(h) Федерального закона о пищевых продуктах, лекарственных средствах и косметических средствах (FD&C Act) программное обеспечение, предназначенное для поддержки принятия решений при диагностике, лечении, профилактике, излечении или смягчении последствий заболеваний или других состояний здоровья. Кроме того, согласно разделу 520(o)(1)(E), медицинские системы визуализации, такие как рентгеновские аппараты, компьютерная томография (КТ), магнитно-резонансная томография (МРТ) и ультразвуковое исследование (УЗИ), подходят для медицинских целей. Таким образом, внедрение руководящих принципов обеспечивает положительное влияние на рост рынка.
Рынок программного обеспечения для сопоставления результатов клинических испытаний в Канаде демонстрирует значительный рост благодаря государственным инвестициям и вкладу исследователей. Согласно отчёту Канадских институтов исследований здравоохранения за июль 2023 года, правительство Канады инвестировало 250 миллионов долларов США в поддержку финансирования клинических испытаний в рамках инициативы по укреплению Стратегии Канады в области биопроизводства и наук о жизни. Кроме того, в феврале 2024 года исследователи из Института исследований рака Онтарио разработали PMATCH – автоматизированную систему для сопоставления результатов клинических испытаний прецизионной медицины с подходящими онкологическими пациентами. Таким образом, благодаря всем этим разработкам и финансированию рынок имеет больше возможностей для роста и расширения.
Статистика рынка Азиатско-Тихоокеанского региона
Рынок программного обеспечения для клинических испытаний в Азиатско-Тихоокеанском регионе (АТР) является самым быстрорастущим регионом и, как ожидается, продемонстрирует значительный рост в прогнозируемые сроки благодаря большому количеству пациентов. Кроме того, различные организации стремятся разместить в регионе свои научно-исследовательские и опытно-конструкторские разработки для поддержки расширения рынка. Это объясняется ростом числа ИТ-проектов в сфере здравоохранения, развивающейся экономикой и полной модернизацией инфраструктуры здравоохранения, особенно в развивающихся странах, включая Индию и Китай, что свидетельствует о росте рынка.
Рынок программного обеспечения для сопоставления клинических испытаний в Индии ожидает существенного роста, поскольку эти испытания легко внедряются для оценки методов лечения онкологических больных. Например, согласно статье, опубликованной NLM в феврале 2024 года, NexCAR19 — первая в стране CAR-T-клеточная терапия, одобренная Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) на основе двух клинических испытаний с участием 64 пациентов с запущенной лейкемией. Согласно результатам испытаний, у 67% пациентов наблюдалось значительное снижение уровня рака (объективный ответ), а примерно у половины рак полностью исчез (полный ответ). Таким образом, благодаря развитию инновационных методов лечения ожидается успешное развитие рынка в стране.
Рынок программного обеспечения для сопоставления клинических испытаний в Китае приобретает все большую известность благодаря наличию инноваций и достижений в оценке клинических аспектов пациентов, страдающих редкими заболеваниями. Согласно статье NLM за февраль 2024 года, было проведено ретроспективное исследование 1053 стационарных пациентов с диагнозом гепатоцеллюлярная карцинома в отношении оценки искусственного интеллекта в системе сопоставления клинических испытаний (CTMS). Исследование выявило приемлемый уровень межэкспертной надежности в диапазоне от 0,65 до 0,88 с уровнем точности от 92,9% до 98,0%. Кроме того, чувствительность составила от 51,9% до 83,5%, специфичность от 99,0% до 99,1%, положительная прогностическая ценность от 75,7% до 85,1% и отрицательная прогностическая ценность от 97,4% до 98,9%.
Ключевые игроки рынка программного обеспечения для сопоставления клинических испытаний:
- Адварра
- Обзор компании
- Бизнес-стратегия
- Основные предложения продуктов
- Финансовые показатели
- Ключевые показатели эффективности
- Анализ рисков
- Недавнее развитие
- Региональное присутствие
- SWOT-анализ
- Antidote Technologies, Inc.
- Аксенчер
- Клиническая разработка IBM
- Мобильное приложение для клинических испытаний
- SSS Международные клинические исследования
- Арис Глобал
- Кларио
- Bsi Business Systems Integration AG
- Корпорация Microsoft
- Офни Системс
- Оракул
- ИКВИА
- Syneos Health
Компании, занимающие лидирующие позиции на рынке программного обеспечения для сопоставления результатов клинических испытаний, стремительно набирают популярность благодаря растущему спросу исследователей на аналитику данных в режиме реального времени. Кроме того, достижения в области искусственного интеллекта (ИИ) меняют ключевые этапы разработки клинических испытаний, стремясь к повышению совокупного показателя успешности. Исходя из этого, в январе 2024 года Accenture объявила о тактических инвестициях через Accenture Ventures в QuantHealth, что позволит фармацевтическим и биотехнологическим организациям быстро и экономично разрабатывать методы лечения для пациентов. Это свидетельствует об оптимистичном подходе к эффективному и продуктивному развитию рынка.
Более того, благодаря эксклюзивной технологии искусственного интеллекта, обученной на массиве данных из 350 миллионов пациентов, обширным графикам, основанным на биомедицинских знаниях, и данным клинических испытаний, платформа моделирования QuantHealth может прогнозировать результаты испытаний с высокой точностью. Это позволяет дополнительно оценивать вариации протоколов и определять оптимальный дизайн испытаний для достижения успеха, помогая командам исследователей и разработчиков точнее и быстрее прогнозировать результаты клинических испытаний, а также принимать решения о продолжении испытаний, оптимизировать когорты, возможности повторного использования препаратов и учитывать другие важные факторы. Все эти факторы способствуют развитию рынка на мировой арене.
Вот список некоторых ключевых игроков:
Последние события
- В январе 2025 года компания Syneos Health подписала соглашение с ACTIVATO о расширении компетенции в области проведения клинических исследований в широком спектре терапевтических областей в Японии. Целью этого является ускорение внедрения клинических разработок на этом быстрорастущем и меняющемся рынке.
- В июне 2024 года компания IQVIA объявила о запуске One Home for Sites — новейшей технологической платформы, которая выполняет функции единого входа и единой панели управления для ключевых систем и задач, необходимых клиническому исследовательскому центру для выполнения всех проводимых им клинических испытаний.
- В мае 2024 года компания Oracle достигла успехов в своей глобальной системе рандомизации и управления поставками клинических испытаний (RTSM) за счет улучшения регионализации, доступа и оказания помощи пользователям в соблюдении нормативных требований, специфичных для каждой страны, а также повышения надежности и прозрачности испытаний с начала до завершения.
- Report ID: 7333
- Published Date: Aug 26, 2025
- Report Format: PDF, PPT
- Ознакомьтесь с предварительным обзором ключевых рыночных тенденций и инсайтов
- Ознакомьтесь с примерами таблиц данных и разбивками по сегментам
- Оцените качество наших визуальных представлений данных
- Оцените структуру нашего отчёта и методологию исследования
- Получите представление об анализе конкурентной среды
- Поймите, как представлены региональные прогнозы
- Оцените глубину профилирования компаний и бенчмаркинга
- Предварительный просмотр того, как практические инсайты могут поддержать вашу стратегию
Изучите реальные данные и анализ
Часто задаваемые вопросы (FAQ)
Программное обеспечение для сопоставления клинических испытаний Объем рыночного отчета
Бесплатный образец включает текущий и исторический объем рынка, тенденции роста, региональные графики и таблицы, профили компаний, прогнозы по сегментам и многое другое.
Связаться с нашим экспертом
Авторские права © 2026 Research Nester. Все права защищены.




