Prospettive di mercato per il trattamento delle malattie rare:
Il mercato del trattamento delle malattie rare ha superato i 230,13 miliardi di dollari nel 2025 e si prevede che raggiungerà i 695,83 miliardi di dollari entro il 2035, con un tasso di crescita annuo composto (CAGR) di circa l'11,7% nel periodo di previsione, ovvero tra il 2026 e il 2035. Nel 2026, il valore del settore del trattamento delle malattie rare è stimato in 254,36 miliardi di dollari.

Il mercato globale dei trattamenti per le malattie rare è caratterizzato da un bacino di pazienti limitato ma diversificato, con oltre 300 milioni di persone in tutto il mondo affette da tali patologie nel 2024, come riportato dalla Global Rare Disease Commission (GRDC). In contesti chiave, tra cui Stati Uniti, Giappone ed Europa, la demografia target è piuttosto ridotta, ma l'epidemiologia cumulativa continua a crescere grazie al miglioramento della capacità diagnostica e dell'ereditarietà delle mutazioni genetiche. Di conseguenza, circa il 70% di queste malattie si manifesta tra i bambini. L'ampia gamma di queste condizioni alimenta anche la domanda in questo settore, dove sono stati identificati oltre 7.000 tipi di malattie rare in tutto il mondo fino al 2024, con un potenziale di oltre 10.000 e 300 nuove descrizioni di malattie genetiche rare aggiunte ogni anno alle principali basi di conoscenza.
Inoltre, indicando la panoramica finanziaria dei prezzi applicati dai pagatori sul mercato, l'Institute for Clinical and Economic Review (ICER) del 2022 ha rivelato che un prezzo annuo di 100.000 dollari per un farmaco orfano per una popolazione limitata di 10.000 pazienti affetti da queste patologie può generare un fatturato annuo di 1 miliardo di dollari. Il rapporto ha inoltre evidenziato che il costo complessivo del trattamento di queste patologie per individuo supera spesso 1 milione di dollari ogni anno, a causa dell'elevato prezzo dei farmaci orfani certificati e delle terapie geniche e cellulari . Queste cifre indicano un'inflazione nei costi di prodotti e servizi per utenti finali e consumatori, insieme alle opportunità redditizie offerte da prodotti farmaceutici di fascia alta.
Chiave Trattamento delle malattie rare Riepilogo delle Analisi di Mercato:
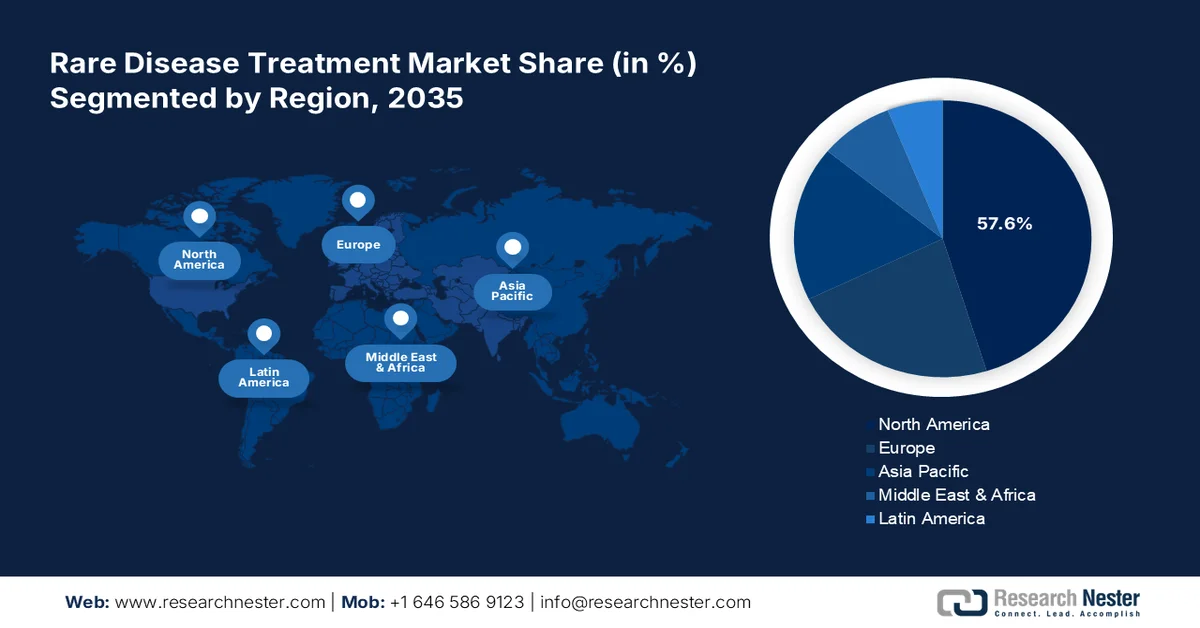
Punti salienti regionali:
- Si prevede che il Nord America deterrà una quota del 57,6% durante l'arco di tempo valutato, trainato da una maggiore prevalenza di malattie rare e da politiche governative di supporto.
- Il mercato dell'Asia-Pacifico è destinato a registrare una crescita significativa durante il periodo di previsione, grazie all'espansione della capacità di cura delle malattie rare e all'aumento degli investimenti nel settore sanitario.
Informazioni sui segmenti:
- Si prevede che il segmento dei prodotti biologici rappresenterà una quota del 53,8% durante il periodo analizzato, grazie alla crescente adozione della medicina di precisione e dei programmi biosimilari guidati dal governo.
- Il segmento delle patologie ematologiche è destinato a detenere una quota di fatturato del 45,4% tra il 2026 e il 2035, spinto dall'elevata prevalenza, dai tassi di mortalità e dalla crescente adozione di terapie geniche e cellulari.
Principali tendenze di crescita:
- Progressi nella diagnosi e nella comprensione delle malattie
- Aumento degli investimenti in ricerca e sviluppo e nell'espansione della pipeline
Sfide principali:
- Limitazioni infrastrutturali e di accessibilità
- Elevata pressione sui prezzi da parte dei pagatori
Attori principali: Roche Holding AG, Novartis AG, Johnson & Johnson, Pfizer Inc., Sanofi SA, Takeda Pharmaceutical Co., Amgen Inc., Biogen Inc., Alexion, Vertex Pharmaceuticals, Regeneron Pharmaceuticals, CSL Behring, Sarepta Therapeutics, UCB SA, Ipsen, Chugai Pharmaceutical, Kyowa Kirin, Dr. Reddy's Laboratories, Samsung Biologics
Globale Trattamento delle malattie rare Mercato Previsioni e prospettive regionali:
Proiezioni di crescita e dimensioni del mercato:
- Dimensioni del mercato nel 2025: 230,13 miliardi di USD
- Dimensioni del mercato nel 2026: 254,36 miliardi di USD
- Dimensioni previste del mercato: 695,83 miliardi di USD entro il 2035
- Previsioni di crescita: CAGR dell'11,7% (2026-2035)
Dinamiche regionali chiave:
- Regione più grande: Nord America (quota del 57,6% entro il 2035)
- Regione in più rapida crescita: Asia Pacifico
- Paesi dominanti: Stati Uniti, Germania, Cina, Giappone, Corea del Sud
- Paesi emergenti: India, Singapore, Thailandia, Australia, Messico
Last updated on : 12 March, 2026
Mercato dei trattamenti per le malattie rare: fattori di crescita e sfide
Fattori di crescita
- Progressi nella diagnostica e nella comprensione delle malattie: secondo un articolo del 2025 del National Institute of Health (NIH), l'80% delle diverse patologie rare è classificato come genetico, di cui il 70% e il 3% si manifestano durante l'infanzia e il periodo neonatale. Ciò dimostra l'importante ruolo dell'espansione esponenziale e dei progressi nel settore del sequenziamento del genoma come importante fattore di crescita del mercato. A dimostrazione di ciò, nel 2022, l'NLM ha pubblicato una meta-analisi, evidenziando che i tassi diagnostici aggregati del sequenziamento dell'intero esoma (WES) e del sequenziamento del genoma intero (WGS) erano superiori rispetto ai metodi convenzionali, pari rispettivamente a 0,3 e 0,4, aprendo nuove possibilità per casi precedentemente non trattati.
Risparmio sui costi grazie al sequenziamento genomico rapido nella pratica clinica (2022)
Paese | Metodo di sequenziamento | Risultati chiave |
Australia | WES rapido | Risparmio di 408.090 USD sui costi derivanti da procedure evitate e giorni di degenza in ospedale |
Hong Kong | WES rapido | Ridotti 566 giorni di degenza ospedaliera e risparmiati 1,03 milioni di USD |
NOI | WGS rapido | Risparmio netto sui costi di 128.555 USD grazie alla riduzione dei giorni di degenza |
Fonte: NLM
- Crescenti investimenti in R&S ed espansione della pipeline : organizzazioni pubbliche e private in tutto il mondo stanno investendo massicciamente in ricerche approfondite per ampliare i campi di applicazione dei portafogli di prodotti esistenti. Ogni anno, oltre 10 miliardi di dollari vengono destinati esclusivamente a queste coorti in tutto il mondo nel mercato del trattamento delle malattie rare. D'altro canto, anche il successo commerciale delle innovazioni derivanti da questi sforzi sta segnando traguardi. Un esempio è il lancio di Attruby (acoramidis) per il trattamento della cardiomiopatia amiloide transtiretinica (ATTR-CM) nel novembre 2024, che ha generato 36,7 milioni di dollari di vendite per BridgeBio Pharma solo nel mercato statunitense.
- Maggiore supporto da parte delle autorità governative : la recente riforma della governance pubblica e della certificazione sta garantendo progressi futuri e una sostanziale espansione per i produttori sul mercato, assegnando sussidi, incentivi e approvazioni accelerate. Ciò crea un ambiente favorevole per questo settore, prevenendo al contempo perdite finanziarie e di valore del marchio grazie al risparmio sui costi legati a lunghi processi di conformità e alla scadenza dei brevetti. Un traguardo importante è stato raggiunto in questo ambito con l'autorizzazione per oltre 20 terapie geniche da parte della FDA negli ultimi anni. Ad esempio, nel settembre 2024, Sanofi ha ottenuto l'autorizzazione ODD dalla FDA per il suo Dupixent, un farmaco per il trattamento del pemfigoide bolloso.
Modelli demografici nei principali scenari del mercato dei trattamenti per le malattie rare
Panoramica dell'incidenza e della prevalenza delle malattie rare (MR) negli Stati Uniti (2023)
Regione/Categoria | Tasso di prevalenza stimato |
Stati Uniti nel complesso | 1 persona su 10 |
Massachusetts | Colpisce circa il 10% della popolazione |
Stato di Washington | 700-800 mila persone acquisiscono RD |
Fibrosi cistica | 0,06% |
Sindrome di Ehlers-Danlos | 0,15% |
Sindrome di Turner | 0,02% |
Fonte: FDA, DOH Washington e ISPOR
Progetti di sviluppo recenti/in corso relativi al mercato del trattamento delle malattie rare
Sperimentazioni cliniche attuali/recenti/in corso sui farmaci RD
Nome del farmaco | Indicazione | Sponsor | Fase di studio | Note chiave | Cronologia |
Venglustat | Malattia di Gaucher di tipo 3 | Sanofi Genzyme | Fase 3 | Terapia orale di riduzione del substrato; valutazione della sicurezza a lungo termine | Attivo (termina nel 2026) |
Hurlerase (vestronidasi alfa) | Mucopolisaccaridosi VII | Ultragenix | Fase 4 | Terapia enzimatica sostitutiva nei pazienti pediatrici | In corso dal 2023 |
Luxturna | Malattia retinica ereditaria | Spark Therapeutics | Follow-up/Fase 4 | Terapia genica per la distrofia retinica associata alla mutazione RPE65 | Follow-up a lungo termine in corso |
Elivaldogene autotemcel | Leucodistrofia metacromatica | Orchard Therapeutics | Fase 3 | Terapia genica autologa, singola infusione | Attivo (Completamento 2025) |
Zynteglo | Beta-talassemia | Biografia di Bluebird | Fase 3/Approvato | Terapia genica, trasduzione di cellule staminali autologhe | Studi approvati e in corso |
Rottaviano | Emofilia A | BioMarin | Fase 3 | Terapia genica per la carenza del fattore VIII | Attivo (termina nel 2026) |
Amondys 45 | distrofia muscolare di Duchenne | Sarepta Therapeutics | Fase 3 | Oligonucleotide antisenso che salta gli esoni | In corso (2023-2025) |
Olipudasi alfa | Deficit di sfingomielinasi acida | Sanofi Genzyme | Fase 3 | Terapia enzimatica sostitutiva per la malattia di Niemann-Pick | Completato di recente |
Libmeldy | Leucodistrofia metacromatica | Orchard Therapeutics | Fase 2/3 | Terapia genica; approvazione EMA, approvazione USA in attesa | Registrazione in corso |
Fonte: Clinicaltrials.gov
Sfide
- Limitazioni infrastrutturali e di accessibilità: diverse economie, in particolare le regioni meno servite, incontrano difficoltà nell'accesso a prodotti e servizi adeguati dal mercato. La mancanza di risorse, infrastrutture, protocolli di standardizzazione e capacità diagnostiche sufficienti crea nel complesso lacune nell'accesso dei pazienti, il che si traduce in una limitata adozione in questo settore. A sottolineare lo stesso problema, il rapporto ICER ha rivelato che il 90% dei casi colpiti non disponeva di un trattamento specifico per la malattia approvato dalla FDA fino al 2022.
- Elevata pressione sui prezzi da parte degli enti pagatori : uno studio NLM del 2024 ha classificato Zolgensma come farmaco per il trattamento dell'atrofia muscolare spinale (SMA) come un farmaco dal prezzo elevato a causa del suo costo di 2,1 milioni di dollari a dose. Di conseguenza, una parte significativa degli enti pagatori tende a imporre rigidi controlli sui prezzi di tali farmaci e spesso esclude queste opzioni dai propri piani di rimborso. Ciò non solo riduce il tasso di accessibilità economica e di adozione nel mercato dei trattamenti per le malattie rare, ma riduce anche la redditività per i produttori di terapie avanzate.
Dimensioni e previsioni del mercato dei trattamenti per le malattie rare:
| Attribut du rapport | Détails |
|---|---|
|
Anno base |
2025 |
|
Anno di previsione |
2026-2035 |
|
CAGR |
11.7% |
|
Dimensione del mercato dell'anno base (2025) |
230,13 miliardi di dollari |
|
Dimensione del mercato prevista per l'anno (2035) |
695,83 miliardi di dollari |
|
Ambito regionale |
|
Segmentazione del mercato del trattamento delle malattie rare:
Analisi del segmento del tipo di farmaco
Si prevede che il segmento dei farmaci biologici rappresenterà la quota maggiore del mercato, pari al 53,8%, durante il periodo analizzato. Questa leadership è attribuibile principalmente alla crescente popolarità della medicina di precisione nei casi di patologie difficili da trattare. Inoltre, in quanto parte di questa categoria, i biosimilari stanno diventando candidati idonei per i programmi governativi che promuovono l'accessibilità economica, rendendoli risorse ampiamente accettate e commercializzate per questo settore. Inoltre, la reputazione del segmento come gold standard per la conformità può essere esemplificata dall'approvazione da parte della FDA di Bkemv e Soliris come biosimilari intercambiabili per patologie rare nel maggio 2024.
Analisi del segmento delle malattie
Il segmento delle patologie ematologiche è destinato a detenere la quota di fatturato più elevata, pari al 45,4%, tra il 2026 e il 2035. L'elevata prevalenza e i tassi di mortalità di queste patologie, come l'anemia falciforme, l'emofilia e l'emoglobinuria parossistica notturna, in particolare tra i bambini, sono i principali fattori di crescita alla base di questa predominanza. Secondo uno studio sul Global Burden of Disease (GBD), il numero totale di nascite di neonati e persone affette da anemia falciforme è aumentato del 13,7% e del 41,4% a livello mondiale dal 2000 al 2021. D'altro canto, l'efficacia clinicamente comprovata delle terapie geniche e cellulari attrae maggiori investimenti nello sviluppo di nuovi farmaci per questa disciplina medica.
Analisi del segmento di pazienti
Si prevede che la fascia di età pediatrica diventerà il segmento di pazienti leader del mercato entro la fine del 2035, con una quota del 67,9%. Secondo una pubblicazione del 2023 del Journal of Pediatric Nursing, il 50-75% di tutte le malattie rare si verifica nei bambini. Inoltre, un altro dato del NLM dello stesso anno ha rivelato che i decessi per età dovuti all'anemia falciforme hanno rappresentato 81.100 casi tra i bambini di età inferiore ai 5 anni dal 2000 al 2021, una cifra superiore rispetto alla mortalità per causa specifica. Questi dati evidenziano il motivo per cui la maggior parte dell'attività del settore si concentra in questo segmento, consolidandone la posizione di leadership nel settore.
La nostra analisi approfondita del mercato include i seguenti segmenti:
Segmento | Sottosegmento |
Tipo di farmaco |
|
Malattie |
|
Paziente |
|
Via di somministrazione |
|
Canale di distribuzione |
|

Vishnu Nair
Responsabile dello sviluppo commerciale globalePersonalizza questo rapporto in base alle tue esigenze — contatta il nostro consulente per approfondimenti e opzioni personalizzate.
Mercato del trattamento delle malattie rare - Analisi regionale
Approfondimenti sul mercato nordamericano
Si prevede che il Nord America dominerà il mercato con una quota del 57,6% nell'arco di tempo considerato. La maggiore incidenza di malattie rare rispetto ad altre regioni del Pacifico rappresenta il principale fattore di crescita in questo scenario. La presenza di aziende leader e di politiche governative di supporto rappresenta inoltre un asset trainante per la regione in questo settore. A riprova di tale supporto, un rapporto della FDA del 2024 ha evidenziato i beneficiari e l'impatto positivo dell'Orphan Drug Act sul futuro sviluppo di farmaci per le malattie rare nel mercato statunitense. L'Orphan Drug Act consente un'esenzione fino a 3 milioni di dollari dalla tassa d'uso per i farmaci da prescrizione e 7 anni di esclusiva di mercato estesa per i nuovi farmaci approvati dalla FDA.
Il crescente bacino di pazienti negli Stati Uniti richiede l'espansione dello sviluppo e della capacità produttiva nel mercato del trattamento delle malattie rare. Ciò è testimoniato dal rapporto della FDA del 2024, che indica che il numero di persone affette da malattie rare ha raggiunto i 30 milioni nel Paese. Inoltre, gli Stati Uniti ospitano un sistema medico avanzato che offre infrastrutture adeguate per usufruire di strumenti e servizi diagnostici di nuova generazione, alimentando così l'espansione nella regione. Inoltre, le tempestive approvazioni dei prodotti, l'emergere di terapie basate su CRISPR e l'elevata consapevolezza pubblica negli Stati Uniti stanno alimentando il settore.
In Canada , circa 1 persona su 12 è affetta da una malattia rara, con conseguente urgente necessità di trattamenti efficaci e misure preventive. D'altro canto, per contrastare il divario di accesso, nel 2023 l'organo di governo del Paese ha lanciato la Strategia Nazionale per i Farmaci ad Alto Costo per le Malattie Rare, che sovvenziona l'acquisto di farmaci, garantendo al contempo l'accessibilità economica per i pazienti affetti da malattie rare e la redditività per i produttori. Inoltre, i farmaci disponibili sul mercato rappresentano circa un decimo delle vendite farmaceutiche in Canada, a dimostrazione della presenza di un contesto favorevole.
Approfondimenti sul mercato Asia-Pacifico
Si prevede che il mercato dell'area Asia-Pacifico registrerà una crescita significativa durante il periodo di previsione. Tale ritmo di crescita in questo settore è in gran parte attribuito alla forte attenzione all'espansione della capacità di cura delle malattie rare e all'aumento degli investimenti nel settore sanitario pubblico e privato. In particolare, in Cina, India, Vietnam e Indonesia, la crescente tendenza a produrre il massimo volume di farmaci biologici sta alimentando notevolmente il settore nell'area APAC. Inoltre, la semplificazione degli studi clinici e l'aggiornamento dei percorsi normativi stanno consentendo la commercializzazione su larga scala di opzioni terapeutiche precoci per contrastare la mortalità dovuta alla progressione della malattia.
Il Giappone è uno dei centri di innovazione più popolari e una base di consumatori esigente nel mercato APAC. La crescente enfasi del Paese sulla medicina di precisione e l'ambizioso obiettivo di superare la situazione di perdita di farmaci stanno spingendo il Paese a stanziare un robusto budget sanitario per questa categoria. Gli sforzi del governo per rafforzare questa categoria sono ulteriormente testimoniati dalle politiche dell'Orphan Drug System, che offre un'esclusiva di mercato decennale, sussidi per la ricerca e sviluppo che coprono il 50% dei costi di sperimentazione clinica e una revisione più rapida di 6 mesi rispetto ai farmaci standard.
In Cina , il mercato è in costante crescita, grazie al crescente numero di casi di malattie rare e alla presenza di un sistema sanitario centralizzato. Inoltre, i miglioramenti nei processi di acquisizione e conformità degli ultimi anni stanno attraendo investimenti su larga scala e una maggiore partecipazione da parte di aziende nazionali ed estere del settore. A riprova di ciò, le riforme normative del 2017 in Cina hanno portato al lancio di oltre 50 farmaci multinazionali per il trattamento delle malattie rare, sulla scia dell'aumento delle approvazioni di farmaci orfani nel 2022, passate da 3 all'anno prima della riforma a oltre 30.
Opportunità realizzabili in paesaggi chiave
Paese | Note chiave |
Corea del Sud | Rimborso del 100% per 167 malattie rare designate |
Giappone | Ha stanziato il 4% del bilancio sanitario nazionale per la ricerca sulle malattie incurabili |
India | Una popolazione di pazienti di 70 milioni, di cui solo il 5% correttamente diagnosticato |
Fonte: Rapporto di ricerca Nester
Approfondimenti sul mercato europeo
Si prevede che il mercato europeo dei trattamenti per le malattie rare occuperà una posizione di rilievo tra il 2026 e il 2035. I quadri di rimborso ben strutturati e gli incentivi normativi sono i principali fattori di crescita di questo settore, alimentando la costante espansione della regione. Con un bacino di 36 milioni di pazienti affetti da malattie rare, il panorama sta inoltre promuovendo un ambiente commerciale interessante per i prodotti, secondo la relazione del Parlamento europeo del 2025. Inoltre, gli sforzi governativi a beneficio del mercato includono il lancio dell'Alleanza europea per la ricerca sulle malattie rare (ERDERA) nell'ottobre 2024, che finanzierà la ricerca sulla prevenzione, la diagnosi e il trattamento delle malattie rare con 447,3 milioni di dollari fino al 2035.
In Germania , si prevede che il mercato sarà leader in Europa grazie alla sua solida infrastruttura sanitaria che soddisfa il crescente numero di pazienti. Il Paese dispone inoltre di un'ampia rete di centri specializzati, tra cui l'ACHSE, che supporta la diagnosi precoce, il trattamento e l'assistenza ai pazienti. Inoltre, con la crescente attenzione allo sviluppo di farmaci avanzati e biologici di nuova generazione, si prevede che il Paese espanderà rapidamente questo settore nei prossimi anni.
Il mercato del trattamento delle malattie rare in Francia è in gran parte trainato dall'HAS e dalla solidarietà. Gli sforzi a livello nazionale per rafforzare le strutture sanitarie esistenti per l'intervento precoce e la diagnosi stanno inoltre generando un'impennata redditizia in questo settore. Nei prossimi anni, si prevede che i crescenti investimenti pubblici e privati nelle terapie geniche e cellulari rimodelleranno le pipeline esistenti nel Paese, attirando al contempo un maggior numero di investitori globali disposti a investire le proprie risorse in questo settore.
Opportunità realizzabili per il mercato
Iniziativa | Note chiave | Cronologia |
Reti di riferimento europee (ERN) | 1.619 centri specializzati dislocati in 382 ospedali, per affrontare malattie e condizioni rare, a bassa prevalenza e complesse che richiedono un'assistenza sanitaria altamente specializzata | 2017-2024 |
Azione congiunta sull'integrazione degli Ern nei sistemi sanitari nazionali (JARDIN) | Ha ricevuto 17,6 milioni di dollari dal programma EU4Health e 4,4 milioni di dollari dagli Stati membri dell'UE per facilitare un maggiore accesso dei pazienti | 2024-2027 |
Sistema di gestione dei pazienti clinici 2.0 | La Commissione europea ha lanciato una nuova piattaforma informatica per offrire un supporto migliore alle ERN, riducendo la necessità di spostamenti dei pazienti | 2024 |
Fonte: Parlamento europeo
Attori del mercato del trattamento delle malattie rare:
- Roche Holding AG
- Panoramica aziendale
- Strategia aziendale
- Offerte di prodotti chiave
- Performance finanziaria
- Indicatori chiave di prestazione
- Analisi del rischio
- Sviluppo recente
- Presenza regionale
- Analisi SWOT
- Novartis AG
- Johnson & Johnson
- Pfizer Inc.
- Sanofi SA
- Takeda Pharmaceutical Co.
- Amgen Inc.
- Biogen Inc.
- Alessio
- Vertex Pharmaceuticals
- Regeneron Pharmaceuticals
- CSL Behring
- Sarepta Therapeutics
- UCB SA
- Ipsen
- Chugai Pharmaceutical
- Kyowa Kirin
- Laboratori del Dr. Reddy
- Samsung Biologics
Il mercato globale dei trattamenti per le malattie rare è altamente consolidato, con diversi colossi biofarmaceutici come Pfizer, Roche, Takeda e Sanofi che controllano una quota considerevole del mercato. Queste aziende sono fortemente concentrate sul rafforzamento dei loro portafogli in questa categoria attraverso l'acquisizione di designazioni di farmaci orfani, l'innovazione nella terapia genica e cellulare e l'espansione strategica nei territori regionali per mantenere il loro predominio sulla generazione di fatturato netto in questo settore. D'altro canto, diversi attori chiave dell'area Asia-Pacifico stanno debuttando attraverso percorsi di biosimilari e partnership pubblico-private.
Ecco un elenco dei principali attori che operano sul mercato:
Sviluppi recenti
- Nel settembre 2025, Alexion ha annunciato che Koselugo (selumetinib) ha ottenuto la raccomandazione per l'approvazione nell'Unione Europea (UE) per il trattamento dei neurofibromi plessiformi (PN) sintomatici e inoperabili nei pazienti adulti affetti da neurofibromatosi di tipo 1 (NF1).
- Nel giugno 2025, CSL Behring ha ricevuto l'approvazione della FDA per Andembry , il primo trattamento profilattico mirato al fattore XIIa per l'angioedema ereditario (HAE), disponibile in monosomministrazione mensile per pazienti dai 12 anni in su. Il suo innovativo meccanismo d'azione, supportato da rigorosi studi clinici, lo posiziona come un'opzione rivoluzionaria in un mercato competitivo.
- Report ID: 6667
- Published Date: Mar 12, 2026
- Report Format: PDF, PPT
- Esplora un’anteprima delle principali tendenze di mercato e degli approfondimenti
- Rivedi tabelle di dati campione e suddivisioni per segmento
- Vivi la qualità delle nostre rappresentazioni visive dei dati
- Valuta la struttura del nostro rapporto e la metodologia di ricerca
- Dai uno sguardo all’analisi del panorama competitivo
- Comprendi come vengono presentate le previsioni regionali
- Valuta la profondità del profilo aziendale e del benchmarking
- Anteprima di come gli insight attuabili possano supportare la vostra strategia
Esplora dati e analisi reali
Domande frequenti (FAQ)
Trattamento delle malattie rare Ambito del rapporto di mercato
Il campione gratuito include le dimensioni attuali e storiche del mercato, le tendenze di crescita, grafici e tabelle regionali, profili aziendali, previsioni per segmento e altro ancora.
Contatta il nostro esperto
Copyright © 2026 Research Nester. Tutti i diritti riservati.




