Prospettive di mercato dei biosimilari di Adalimumab:
Il mercato dei biosimilari di adalimumab è stato stimato in 897,85 milioni di dollari nel 2025 e si prevede che raggiungerà gli 8,1 miliardi di dollari entro il 2035, registrando un CAGR di circa il 24,6% durante il periodo di previsione, ovvero tra il 2026 e il 2035. Nel 2026, il mercato dei biosimilari di adalimumab è stimato in 1,1 miliardi di dollari.

Adalimumab è l'anticorpo monoclonale approvato dalla FDA, comunemente noto come Humira, indicato per il trattamento di numerose patologie infiammatorie e immunitarie. Questi farmaci hanno dimostrato immunogenicità, sicurezza ed efficacia, trainando così la crescita del mercato a livello globale. Secondo l'articolo del NLM di ottobre 2023, il mercato ha guadagnato un'enorme popolarità in Europa, con il 35% dei pazienti passati al biosimilare di adalimumab. Inoltre, l'articolo ha anche evidenziato che il 90,5% dei pazienti in tutti i Paesi preferisce l'uso della penna Humira rispetto al 18,2% che preferisce la penna Imraldi, favorendo così l'espansione del mercato.
Inoltre, il mercato dei biosimilari di adalimumab è in espansione, poiché è stato riconosciuto come il farmaco più venduto sin dalla sua approvazione. Inoltre, l'articolo del NLM di dicembre 2024 ha condotto uno studio trasversale sulla strategia di prezzo dei biosimilari di adalimumab. L'utilizzo complessivo di questo anticorpo è stato stimato in 1 milione di prescrizioni al trimestre, con un aumento dell'1,35% nel 2023. Le vendite nette sono state di 5,0 miliardi di dollari, scese a 2,8 miliardi di dollari. Inoltre, il prezzo netto per prescrizione è stato ridotto da 5.007 dollari a 2.837 dollari. D'altro canto, il prezzo netto di Humira è variato tra 3.452 e 4.793 dollari, di fatto inferiore a quello di altri biosimilari, dimostrandosi quindi un approccio prolifico per la domanda di mercato.
Chiave Adalimumab biosimilare Riepilogo delle Analisi di Mercato:
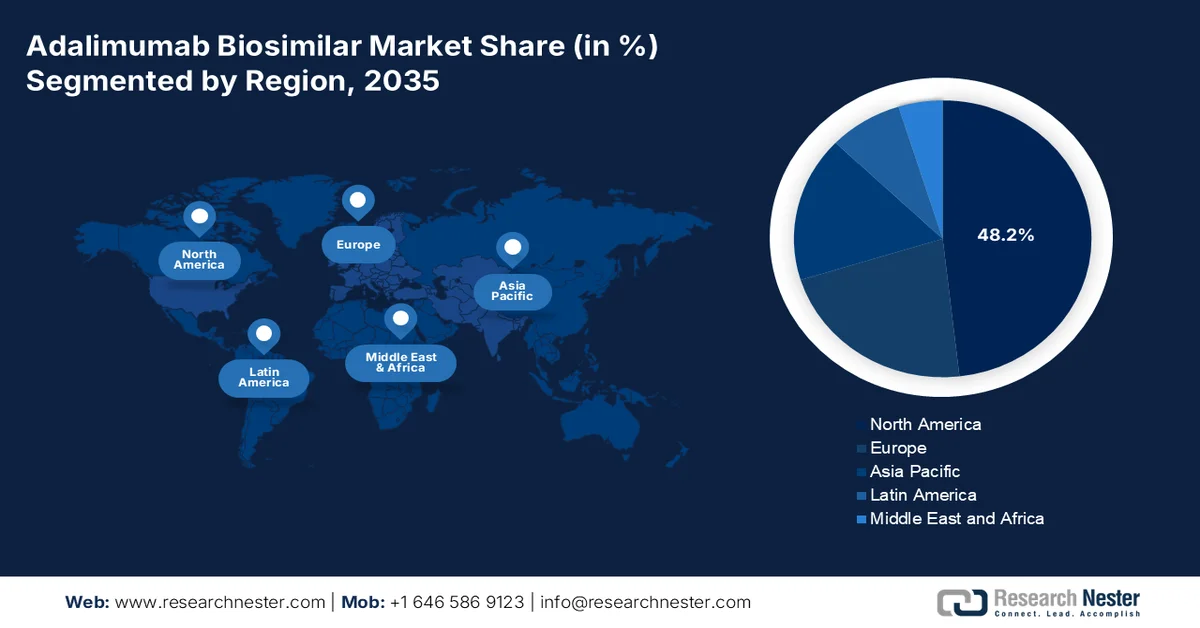
Punti salienti regionali:
- Si prevede che il Nord America acquisirà una quota di fatturato superiore al 48,2% del mercato dei biosimilari dell'adalimumab entro il 2035, grazie a una solida infrastruttura sanitaria, a politiche di rimborso favorevoli e alla crescente prevalenza di malattie autoimmuni.
- Si prevede che l'area Asia-Pacifico diventerà la regione in più rapida crescita nel mercato dei biosimilari dell'adalimumab entro il 2035, spinta dall'aumento del reddito disponibile, dall'ampliamento del bacino di pazienti e da quadri normativi di supporto.
Approfondimenti sui segmenti:
- Si prevede che il segmento Exemptia acquisirà una quota di mercato superiore al 36,8% dei biosimilari di adalimumab entro il 2035, grazie alla sua strategia di prezzo conveniente e alla comprovata efficacia nella gestione delle condizioni autoimmuni.
- Si prevede che il segmento delle farmacie ospedaliere si assicurerà una quota significativa del mercato dei biosimilari dell'adalimumab entro il 2035, grazie ai forti interventi dei farmacisti clinici e agli elevati tassi di accettazione del trattamento in ambito ospedaliero.
Principali tendenze di crescita:
- Aumento dell'incidenza di malattie non trasmissibili
- Concentrarsi su soluzioni mediche convenienti
Sfide principali:
- Processo di produzione complicato
- Rigide politiche di regolamentazione
Attori principali: TIVIC Health, BASF SE, Cala Health, Inc., Abbott, Spark Biomedical, Inc., GENERAL ELECTRIC, BIOTRONIK, Soterix Medical Inc, SetPoint Medical, Bruker Corporation, Biolinq, Royal Philips.
Globale Adalimumab biosimilare Mercato Previsioni e prospettive regionali:
Proiezioni di crescita e dimensioni del mercato:
- Dimensioni del mercato nel 2025: 897,85 milioni di USD
- Dimensioni del mercato nel 2026: 1,1 miliardi di USD
- Dimensioni previste del mercato: 8,1 miliardi di USD entro il 2035
- Previsioni di crescita: CAGR del 24,6% (2026-2035)
Dinamiche regionali chiave:
- Regione più grande: Nord America (quota del 48,2% entro il 2035)
- Regione in più rapida crescita: Asia Pacifico
- Paesi dominanti: Stati Uniti, Germania, Svizzera, India, Corea del Sud
- Paesi emergenti: Cina, India, Giappone, Corea del Sud, Brasile
Last updated on : 25 February, 2026
Mercato dei biosimilari di Adalimumab: fattori di crescita e sfide
Fattori di crescita
Aumento dell'incidenza di patologie non trasmissibili: la crescita del mercato dei biosimilari di adalimumab è fortemente alimentata dall'aumento della prevalenza di malattie rare. Come affermato nel rapporto dell'OMS del dicembre 2024, nel 2021 43 milioni di persone hanno sofferto di patologie non trasmissibili e il 18% di loro è deceduto prima dei 70 anni. Inoltre, l'82% dei decessi si è verificato in Paesi a basso e medio reddito. Pertanto, con l'aumento di queste patologie, si è verificata un'enorme domanda di opzioni terapeutiche economicamente vantaggiose, che sta avendo un impatto positivo sul mercato globale a livello internazionale.
Concentrarsi su soluzioni mediche economicamente vantaggiose: la domanda di biosimilare di adalimumab è in crescita continua e sia i pazienti che gli operatori sanitari lo stanno adottando sempre più spesso per soddisfare le esigenze mediche più idonee. Ciò ha portato a un aumento della produzione e della produzione di farmaci a base di adalimumab, con un'inevitabile espansione del mercato. Inoltre, l'assunzione di questi farmaci è appropriata e costituisce un'alternativa efficace alle costose opzioni terapeutiche convenzionali, generando così un'impennata nei paesi in via di sviluppo.
Sfide
Processo di produzione complesso: la procedura di produzione degli anticorpi può essere complessa, il che ostacola l'espansione del biosimilare di adalimumab a livello globale. Ciò si traduce in ingenti spese di produzione e probabili sfide che aumentano le difficoltà nel mantenere la qualità dei farmaci. Questo, a sua volta, si traduce in una cattiva gestione della salute, che peggiora le condizioni dei pazienti e limita la commercializzazione dei farmaci nel mercato esistente.
Politiche regolatorie rigorose: si prevede che lo sviluppo del mercato dei biosimilari di adalimumab incontrerà limitazioni dovute alla presenza di rigide strategie amministrative. Queste tendono a impedire l'espansione del mercato a livello nazionale, limitando così il processo produttivo. Il rispetto di queste politiche richiede finanziamenti ingenti, soprattutto in attività di ricerca e sviluppo. Ciò rappresenta anche una sfida per i produttori e le organizzazioni che devono apportare contributi adeguati al mercato.
Dimensioni e previsioni del mercato dei biosimilari di Adalimumab:
| Attribut du rapport | Détails |
|---|---|
|
Anno base |
2025 |
|
Anno di previsione |
2026-2035 |
|
CAGR |
24,6% |
|
Dimensione del mercato dell'anno base (2025) |
897,85 milioni di dollari |
|
Dimensione del mercato prevista per l'anno (2035) |
8,1 miliardi di dollari |
|
Ambito regionale |
|
Segmentazione del mercato dei biosimilari di Adalimumab:
Analisi del segmento di prodotto
Si prevede che il segmento Exemptia conquisterà una quota di mercato dei biosimilari di adalimumab superiore al 36,8% entro il 2035. Questo risultato è stato prontamente accettato dai professionisti medici grazie alla sua formulazione innovativa, all'efficacia nel trattamento delle patologie autoimmuni, all'approccio di prezzo conveniente e alle soluzioni economicamente vantaggiose. Secondo l'articolo del NLM di marzo 2020, i pazienti hanno ricevuto deliberatamente una terapia biologica con l'utilizzo di exemptia, con una dose iniziale di 80 mg seguita da 40 mg per quasi 16 settimane. Questo trattamento ha avuto successo senza l'assenza di effetti collaterali, il che fornisce prospettive ottimistiche per il segmento.
Analisi del segmento del canale di distribuzione
In base al canale di distribuzione, si prevede che il segmento delle farmacie ospedaliere acquisirà una quota redditizia nel mercato dei biosimilari di adalimumab durante il periodo di previsione. Questo segmento è cruciale e dimostra un'esposizione efficace grazie al suo posizionamento standard nell'ecosistema sanitario complessivo. Come affermato nell'articolo di NLM di gennaio 2020, è stato condotto uno studio su 42 farmacisti clinici, in cui sono stati valutati 104.728 pazienti. Hanno avviato una media rettificata di 1.221 interventi con un tasso di accettazione del 91,5%, 700 follow-up e visite di controllo, 325 raccomandazioni di dimissione e 273 riconciliazioni farmacologiche, alimentando così la crescita del segmento.
La nostra analisi approfondita del mercato globale dei biosimilari dell'adalimumab include i seguenti segmenti:
Prodotto |
|
Canale di distribuzione |
|

Vishnu Nair
Responsabile dello sviluppo commerciale globalePersonalizza questo rapporto in base alle tue esigenze — contatta il nostro consulente per approfondimenti e opzioni personalizzate.
Mercato dei biosimilari di Adalimumab - Analisi regionale
Approfondimenti sul mercato nordamericano
Entro il 2035, il mercato nordamericano dei biosimilari di adalimumab è destinato a conquistare una quota di fatturato superiore al 48,2%. Questa crescita è alimentata da diversi fattori, tra cui sistemi sanitari e medici solidi, politiche di rimborso standard e consapevolezza di uno stile di vita sano. Inoltre, nella regione si registra un crescente carico di malattie autoimmuni, tra cui la malattia infiammatoria intestinale e l'artrite reumatoide, che determina un aumento della domanda di adalimumab, offrendo così un'opportunità prolifica per l'evoluzione del mercato.
Negli Stati Uniti, il mercato dei biosimilari di adalimumab offre enormi opportunità di crescita grazie alla disponibilità di farmaci biosimilari. Ad esempio, nel maggio 2024, Teva Pharmaceuticals ha dichiarato l'accessibilità di SIMLANDI iniettabile nel Paese. Si tratta di un biosimilare sostituibile a Humira per il trattamento di diverse tipologie di artrite, tra cui l'artrite idiopatica giovanile, l'artrite reumatoide dell'adulto, la spondilite anchilosante dell'adulto e l'artrite psoriasica dell'adulto. Inoltre, è indicato per il trattamento del morbo di Crohn, della psoriasi a placche dell'adulto, della colite ulcerosa dell'adulto, dell'idrosadenite suppurativa dell'adulto e dell'uveite dell'adulto, favorendo così l'espansione del mercato.
La domanda di mercato dei biosimilari di adalimumab in Canada sta registrando un incremento dovuto all'aumento delle vendite di farmaci biologici. Secondo il rapporto del Governo canadese di maggio 2022, le vendite complessive sono triplicate, passando dai 3,3 miliardi di dollari degli anni precedenti a 10 miliardi di dollari. Inoltre, i farmaci biologici rappresentano il 33,9% delle vendite farmaceutiche nel Paese, rappresentando la terza quota più alta nell'OCSE e superando la media del 27,4%. Inoltre, la popolazione spende 262 dollari all'anno in farmaci biologici, il che favorisce una prolifica opportunità di crescita del mercato.
Approfondimenti sul mercato APAC
La regione Asia-Pacifico è destinata a diventare la regione in più rapida crescita nel mercato dei biosimilari di adalimumab durante il periodo di previsione. Fattori come l'aumento del reddito disponibile, la spesa medica e l'aumento del bacino di pazienti sono di fatto responsabili dell'espansione del mercato nella regione. Inoltre, la presenza di contributi organizzativi e di politiche normative sta rapidamente trainando il mercato nella regione, soprattutto in paesi come India e Cina.
Il mercato dei biosimilari di adalimumab in India sta guadagnando sempre più visibilità grazie all'utilizzo di soluzioni ecografiche in combinazione con il trattamento con adalimumab. Ad esempio, nel gennaio 2023, FUJIFILM Sonosite, Inc. ha annunciato il lancio nel Paese del più recente sistema ecografico Sonosite PX. Offre una nitidezza d'immagine avanzata grazie a un'innovativa tecnologia di imaging proprietaria che fornisce livelli nitidi di applicazioni procedurali e diagnostiche durante il processo di trattamento. Pertanto, la presenza della tecnologia è anche un fattore trainante per la crescita del mercato nel Paese.
Il mercato cinese dei biosimilari di adalimumab è in espansione grazie all'approvazione di diversi biosimilari basati su anticorpi. Secondo l'articolo di Biologicals del febbraio 2024, il Paese ha approvato con successo 31 biosimilari, tra cui 2 versioni di Tocilizumab e Denosumab, 3 versioni di Trastuzumab, Rituximab e Infliximab, 7 versioni di Adalimumab e 10 versioni di Bevacizumab. La China National Medical Products Administration (NMPA) ha svolto un ruolo fondamentale nell'approvazione di questi biosimilari, che stanno contribuendo in modo significativo all'evoluzione del mercato nel Paese.
Attori del mercato dei biosimilari di Adalimumab:
- Alvotech
- Panoramica aziendale
- Strategia aziendale
- Offerte di prodotti chiave
- Performance finanziaria
- Indicatori chiave di prestazione
- Analisi del rischio
- Sviluppo recente
- Presenza regionale
- Analisi SWOT
- ADVANZ PHARMA
- Alfred E. Tiefenbacher
- Amgen Inc.
- Boehringer Ingelheim International GmbH
- Glenmark
- Gruppo Zydus
- Torrent Pharmaceuticals Ltd.
- Emcure Pharmaceuticals Ltd
- AET BioTech
- Coherus Biosciences
- Biocon Biologics Ltd
- FUJIFILM Sonosite, Inc.
- Teva Pharmaceuticals
- Mylan NV
- Samsung Bioepis Co., Ltd.
- Organon & Co.
Le principali organizzazioni stanno implementando numerose strategie per avere un impatto positivo sul mercato globale dei biosimilari di adalimumab. Queste strategie includono la commercializzazione del prodotto attraverso collaborazioni, espansione delle infrastrutture, investimenti, integrazione dei servizi, fusioni e acquisizioni. Ad esempio, nel giugno 2024, Alvotech e ADVANZ PHARMA hanno stretto una partnership per l'efficace commercializzazione e fornitura del biosimilare di Eylea (aflibercept) di Alvotech, previsto per il mercato. Si tratta di un farmaco biologico ampiamente utilizzato per la diagnosi di patologie oculari che possono portare alla perdita della vista o alla cecità, come la degenerazione maculare senile (AMD) umida, l'edema maculare e la retinopatia diabetica.
Ecco l'elenco di alcuni giocatori chiave:
Sviluppi recenti
- Nell'aprile 2024, Samsung Bioepis Co., Ltd. ha notificato l'inizio della sperimentazione clinica di fase 3 per SB27, uno studio multicentrico, randomizzato, in doppio cieco, a gruppi paralleli, per confrontare l'efficacia, la sicurezza, la farmacocinetica e l'immunogenicità tra SB27 e Keytruda nei pazienti con carcinoma polmonare non a piccole cellule non squamoso metastatico.
- Nell'agosto 2022, Organon & Co. e Samsung Bioepis Co., Ltd. hanno ricevuto l'approvazione della FDA statunitense per HADLIMA, un biosimilare che sarà disponibile in siringa preriempita e autoiniettore; l'autoiniettore è stato progettato specificamente pensando al paziente.
- Report ID: 7551
- Published Date: Feb 25, 2026
- Report Format: PDF, PPT
- Esplora un’anteprima delle principali tendenze di mercato e degli approfondimenti
- Rivedi tabelle di dati campione e suddivisioni per segmento
- Vivi la qualità delle nostre rappresentazioni visive dei dati
- Valuta la struttura del nostro rapporto e la metodologia di ricerca
- Dai uno sguardo all’analisi del panorama competitivo
- Comprendi come vengono presentate le previsioni regionali
- Valuta la profondità del profilo aziendale e del benchmarking
- Anteprima di come gli insight attuabili possano supportare la vostra strategia
Esplora dati e analisi reali
Domande frequenti (FAQ)
Adalimumab biosimilare Ambito del rapporto di mercato
Il campione gratuito include le dimensioni attuali e storiche del mercato, le tendenze di crescita, grafici e tabelle regionali, profili aziendali, previsioni per segmento e altro ancora.
Contatta il nostro esperto
Copyright © 2026 Research Nester. Tutti i diritti riservati.




