Perspectives du marché de l'externalisation de la pharmacovigilance :
Le marché de l'externalisation de la pharmacovigilance dépassait 5,1 milliards USD en 2025 et devrait dépasser 20,81 milliards USD d'ici 2035, avec un TCAC de plus de 15,1 % sur la période de prévision, soit entre 2026 et 2035. En 2026, la taille du secteur de l'externalisation de la pharmacovigilance est estimée à 5,79 milliards USD.

Alors que le nombre de patients atteints de maladies non transmissibles et potentiellement mortelles augmente dans le monde, les découvertes cliniques se multiplient. Par conséquent, les entreprises pharmaceutiques investissent de plus en plus dans le marché de l'externalisation de la pharmacovigilance pour maintenir leur compétence. Selon un rapport de 2022 de la Fédération internationale des associations de fabricants de produits pharmaceutiques (IFPMA), seul un composé sur 5 000 à 10 000 testés est reconnu comme efficace. Les traitements mis au point nécessitent en outre 10 à 15 ans pour être soumis à de nombreux tests de sécurité rigoureux. Il s'agit d'un investissement important et à long terme, où les services d'évaluation contractuels permettent d'optimiser le processus en réduisant les dépenses et les délais, compte tenu de la demande croissante dans ce secteur.
Nombre de médicaments spécifiés en cours de développement dans le monde (2021)
|
État de santé |
Nombre de médicaments |
|
Cancer |
3 148 |
|
Immunologie |
1 677 |
|
Neurologie |
1 688 |
|
Maladies infectieuses |
1 488 |
Source : IFPMA 2022
Le marché actuel de l'externalisation de la pharmacovigilance se concentre sur les partenariats commerciaux stratégiques et les efforts de réduction des coûts. Alors que la tendance à l'établissement d'une norme unifiée pour les essais cliniques gagne du terrain, de plus en plus d'entreprises, en quête de mondialisation, privilégient une assistance externe proposant des services rationalisés pour une commercialisation efficace et ponctuelle. Selon la NLM, le coût de développement d'un nouveau médicament se situait entre 314 millions et 4,4 milliards de dollars, selon l'étude de juin 2024. Cependant, ce prix dépend fortement du domaine thérapeutique, des données et des hypothèses de modélisation. Afin de réduire le fardeau économique des payeurs de médicaments plus importants En matière de tarification, l'option tierce devient une priorité pour une entreprise afin d'équilibrer ses dépenses totales pour le développement d'un seul médicament.
Présentation classifiée des prix de pharmacovigilance (PV) (2022)
|
Type de procédure ou de service |
Prix standardisé par procédure (in) USD) |
|
Évaluations individuelles des rapports périodiques de sécurité actualisés (PSUR) |
26 447,9 |
|
Évaluation des études de sécurité post-autorisation imposées (PASS) (en cas de présence de plusieurs États membres) |
58 312,2 |
|
Évaluation des orientations en pharmacovigilance |
2 42 858,3 |
|
Service annuel (Technologies de l'information en pharmacovigilance et veille de la littérature médicale sélectionnée) |
90,6 |
Source : Agence européenne des médicaments
Clé Externalisation de la pharmacovigilance Résumé des informations sur le marché:
Points forts régionaux :
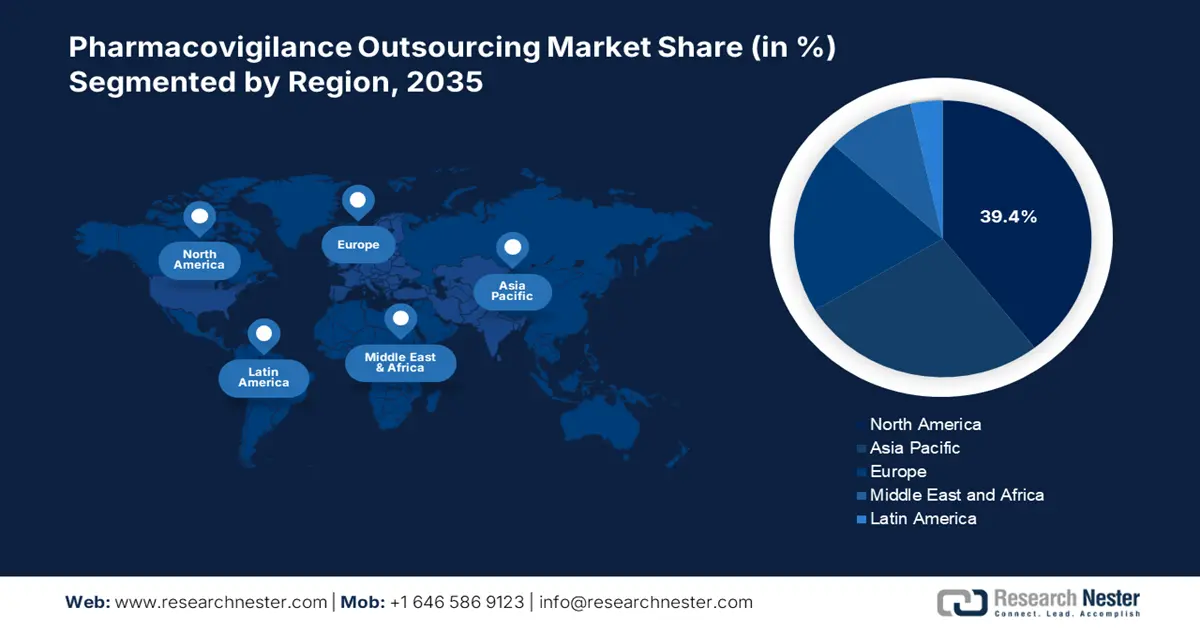
- L'Amérique du Nord détient 39,4 % du marché de l'externalisation de la pharmacovigilance, grâce à des découvertes de médicaments en cours et à d'importants investissements en R&D pharmaceutique, consolidant son leadership grâce à l'innovation d'ici 2035.
Analyses sectorielles :
- Le secteur de l'industrie pharmaceutique devrait enregistrer le taux de croissance annuel composé (TCAC) le plus élevé entre 2026 et 2035, grâce à un environnement commercial mondial bien établi pour les produits pharmaceutiques.
- Le secteur des CRO devrait détenir une part de marché de 71,5 % d'ici 2035, grâce à un afflux important de capitaux dans la R&D pharmaceutique, stimulant la demande d'externalisation.
Principales tendances de croissance :
- Critères réglementaires stricts pour la commercialisation
- Efficacité en termes de délais de commercialisation et de conformité
Principaux défis :
- Préoccupations concernant la confidentialité des données et les risques de violation
- Variabilité de la conformité et de la cohérence
- Acteurs clés :IBM Corporation, Oracle Corporation, Novartis, Accenture, IQVIA, Ergomed.
Mondial Externalisation de la pharmacovigilance Marché Prévisions et perspectives régionales:
Taille du marché et projections de croissance :
- Taille du marché 2025 : 5,1 milliards USD
- Taille du marché 2026 : 5,79 milliards USD
- Taille du marché projetée : 20,81 milliards USD d'ici 2035
- Prévisions de croissance : TCAC de 15,1 % (2026-2035)
Dynamiques régionales clés :
- La plus grande région : Amérique du Nord (part de 39,4 % d'ici 2035)
- Région à la croissance la plus rapide : Asie-Pacifique
- Pays dominants : États-Unis, Chine, Allemagne, Royaume-Uni et Japon
- Pays émergents : Chine, Inde, Brésil, Russie, Mexique
Last updated on : 26 August, 2025
Moteurs de croissance et défis du marché de l'externalisation de la pharmacovigilance :
Moteurs de croissance
- Critères réglementaires stricts pour la commercialisation : Face aux préoccupations croissantes concernant la sécurité des patients, les cadres réglementaires internationaux, tels que la PDMA, la FDA, le MHLW et l'Union européenne, incitent les entreprises à réaliser diverses études cliniques afin d'obtenir une assurance complète avant l'approbation. Le marché de l'externalisation de la pharmacovigilance a évolué avec la dynamique et les critères actuels de ces organismes d'autorisation, offrant une expérience marketing simplifiée. Cela incite davantage de pionniers de l'industrie pharmaceutique à investir dans ce secteur. Par exemple, en septembre 2022, AmerisourceBergen a investi 1,3 milliard de dollars dans l'acquisition de PharmaLex Holding, un fournisseur mondial de services de pharmacovigilance, afin de captiver le vaste réseau de fabricants biopharmaceutiques du secteur.
- Efficacité en termes de délais de commercialisation et de conformité : La pénétration rapide de l'IA et de l'automatisation des laboratoires a stimulé la productivité sur le marché de l'externalisation de la pharmacovigilance. À ce propos, en juillet 2024, OMNY Health a lancé une plateforme de données afin de renforcer les capacités de ses partenaires utilisant l'IA, tels qu'ArisGlobal. Cet outil est conçu pour optimiser la validation des signaux de sécurité de ces prestataires de services de pharmacovigilance en identifiant l'efficacité des médicaments et la réponse des patients grâce à des données concrètes. L'utilisation croissante de ces technologies avancées améliore l'efficacité en matière de livraison rapide et d'optimisation budgétaire, ce qui accroît la popularité de ce secteur auprès des leaders de la pharmacovigilance et élargit la clientèle.
Défis
- Préoccupations concernant la confidentialité des données et les risques de violation : Recruter des professionnels du marché de l'externalisation de la pharmacovigilance implique le partage d'une grande quantité de données sensibles, ce qui augmente le risque de fuite et d'utilisation abusive. L'utilisation d'informations confidentielles, notamment concernant les patients, pose souvent des problèmes pour garantir une confidentialité et une sécurité totales. De plus, les agences de protection des données reconnues mondialement, telles que le RGPD et l'HIPPA, peuvent limiter et compliquer les opérations dans ce domaine. Cela peut dissuader les participants d'investir et de mobiliser leurs précieuses ressources.
- Variabilité de la conformité et de la cohérence : Les critères de conformité varient d'une région à l'autre, ce qui peut créer une incertitude dans la navigation au sein de différents environnements réglementaires. Par conséquent, l'harmonisation entre plusieurs scénarios devient un défi pour le marché de l'externalisation de la pharmacovigilance. Cela peut également entraîner des retards, des erreurs et des dépenses indésirables, ce qui dilue l'intérêt pour la mondialisation et limite l'exposition du secteur. De plus, la difficulté de maintenir un profil de qualité cohérent face à une telle dynamique changeante peut freiner les progrès dans ce secteur.
Taille et prévisions du marché de l'externalisation de la pharmacovigilance :
| Attribut du rapport | Détails |
|---|---|
|
Année de base |
2025 |
|
Période de prévision |
2026-2035 |
|
TCAC |
15,1% |
|
Taille du marché de l'année de base (2025) |
5,1 milliards de dollars américains |
|
Taille du marché prévue pour l'année (2035) |
20,81 milliards USD |
|
Portée régionale |
|
Segmentation du marché de l'externalisation de la pharmacovigilance :
Prestataires de services (organismes de recherche sous contrat (CRO), externalisation des processus métier (BPO))
Selon les prestataires de services, le segment des organismes de recherche sous contrat (CRO) devrait dominer environ 71,5 % du marché de l'externalisation de la pharmacovigilance d'ici fin 2035. L'afflux de capitaux en forte hausse dans la R&D pharmaceutique alimente ce segment. L'expansion mondiale des entreprises biopharmaceutiques contribue également à cette progression. À cet égard, la Fédération internationale des fabricants de produits pharmaceutiques (IFPRI) L'IFPMA (International Pharmaceutical Association) a indiqué que les organismes de recherche du monde entier avaient investi 198 milliards de dollars US en R&D jusqu'en 2020. Elle a également souligné leur contribution à l'économie mondiale de 1 838 milliards de dollars US d'ici 2022. Ces chiffres témoignent de la demande croissante d'assistance de la part des organismes de recherche sous contrat (ORC).
Utilisateurs finaux (industrie pharmaceutique, organismes de recherche, autres)
En termes d'utilisateurs finaux, l'industrie pharmaceutique devrait générer les revenus les plus élevés du marché de l'externalisation de la pharmacovigilance tout au long de la période de prévision. Le contexte commercial mondial bien établi pour les produits associés stimule considérablement la croissance de ce segment. Selon l'OEC, le commerce mondial des produits pharmaceutiques, y compris les produits chimiques, les médicaments, les vaccins et les produits spéciaux, représentait 854,0 milliards USD en 2023. Cela signifie le besoin croissant de solutions régionales de conformité et de marketing, garantissant une marge bénéficiaire stable dans cette catégorie. De plus, la popularité des services contractuels gagne déjà du terrain dans ce secteur, ce qui offre aux leaders un environnement commercial pré-embelli.
Notre analyse approfondie du marché mondial de l'externalisation de la pharmacovigilance couvre les segments suivants :
|
Prestataires de services |
|
|
Utilisateurs finaux |
|
|
Service |
|

Vishnu Nair
Responsable du développement commercial mondialPersonnalisez ce rapport selon vos besoins — contactez notre consultant pour des informations et des options personnalisées.
Analyse régionale du marché de l'externalisation de la pharmacovigilance :
Analyse du marché nord-américain
L'Amérique du Nord devrait dominer le marché de l'externalisation de la pharmacovigilance avec plus de 39,4 % de parts de marché d'ici 2035. Les découvertes de médicaments en cours constituent l'un des principaux moteurs de ce secteur. À ce propos, un rapport de 2022 du SiRM a identifié l'Amérique du Nord comme le plus grand investisseur en R&D pharmaceutique. Il a également indiqué que 68,0 %, 46,0 %, 67,0 % et 45,0 % des investissements en capital-risque, dans les secteurs biopharmaceutique, public et à but non lucratif ont été réalisés dans cette région. Cela témoigne du leadership de la région en matière de développement de nouvelles thérapies innovantes, qui nécessitent des solutions de gestion de la sécurité rigoureuses pour garantir un approvisionnement et une accessibilité suffisants.
Les États-Unis connaissent une augmentation massive des cas d'effets secondaires graves liés aux médicaments, ce qui incite les autorités sanitaires nationales à prioriser et à promouvoir l'importance du marché de l'externalisation de la pharmacovigilance. Dans un article de mai 2021, la NLM a reconnu que les effets indésirables des médicaments (EIM) constituaient la quatrième cause de mortalité dans le pays. De plus, la politique commerciale ouverte du pays en matière d'acceptation des produits étrangers souligne également l'urgente nécessité d'une surveillance post-commercialisation. À cet égard, l'OEC a indiqué que les États-Unis se classaient au premier rang des importateurs de produits et de biens pharmaceutiques, avec 170 milliards USD, et 47,3 milliards USD en 2023. Le Canada renforce son marché de l'externalisation de la pharmacovigilance grâce à une gouvernance solide en matière de réglementation des normes de sécurité. Les organismes de réglementation de ce pays sont très actifs pour garantir le bien-être des patients à tous les niveaux, y compris lors des évaluations de l'efficacité des médicaments. Par exemple, en mai 2020, le Réseau canadien pour l'innocuité et l'efficacité des médicaments (RSEMD) a alloué un budget annuel de 10 millions USD à la recherche de preuves post-commercialisation de l'efficacité et de la sécurité des médicaments. Ce financement a été consacré à soutenir Santé Canada dans la surveillance et la prise de décisions ciblées concernant les médicaments à usage humain, créant ainsi de nouvelles opportunités pour les leaders du marché.
Statistiques du marché Asie-Pacifique
Le marché de l'externalisation de la pharmacovigilance en Asie-Pacifique est voué à une production accrue et devrait connaître la croissance la plus rapide au cours de la période évaluée. Cette région abrite de nombreux producteurs et développeurs de médicaments de renommée internationale, ce qui contribue à la création d'une large clientèle pour ce secteur. Ce paysage émergent de découvertes cliniques incite les prestataires de services à améliorer la qualité et l'efficacité de leurs offres, apportant ainsi de la diversité à ce secteur. De plus, les pays en développement de cette région accordent une grande importance à la réduction de la prévalence des effets indésirables. De plus, la complexité des cadres réglementaires et la poursuite des essais cliniques incitent les entreprises à investir dans ce domaine.
L'Inde a développé l'un des systèmes de réglementation de sécurité les plus stricts, ce qui stimule la croissance du marché de l'externalisation de la pharmacovigilance. Les autorités publiques et privées mettent en place proactivement des mesures préventives et des outils promotionnels dans tout le pays pour lutter contre les effets indésirables fréquents des médicaments. Par exemple, en septembre 2023, Bharat Serums and Vaccines Limited (BSV) a lancé une application mobile, BSV AER, permettant de signaler les effets indésirables. Cet outil s'appuie sur le système de pharmacovigilance développé par l'entreprise, offrant une solution de réponse rapide aux professionnels de santé, aux patients et aux entreprises pharmaceutiques.
La Chine offre des perspectives d'investissement plus importantes pour le marché de l'externalisation de la pharmacovigilance grâce à sa participation fréquente aux essais cliniques. Au cours de la dernière décennie, le pays a réalisé des progrès remarquables dans le développement de réseaux locaux de recherche et développement et de production liés aux médicaments, ce qui représente une importante base de consommateurs pour les prestataires de services de PV. Selon la NLM, la part des études cliniques sans indication d'action (NAI) pour les approbations de la FDA en Chine a augmenté de 37,0 % entre 2016 et 2023, témoignant d'une amélioration considérable de la qualité des inspections du pays. Un autre rapport de l'OMS indique que la Chine a enregistré le plus grand nombre d'essais cliniques au monde, avec 41 834 (22,5 %), entre 2022 et 2024.
Principaux acteurs du marché de l'externalisation de la pharmacovigilance :
- IBM Corporation
- Présentation de l'entreprise
- Stratégie commerciale
- Principales offres de produits
- Performance financière
- Indicateurs clés de performance
- Analyse des risques
- Évolution récente
- Présence régionale
- Analyse SWOT
- Clintec
- Covance
- Oracle Corporation
- Novartis
- iGATE Corporation
- Accenture
- iMED Global Corporation
- Bioclinique
- MarksMan Healthcare
- Symogène
- Ergomed
- IQVIA
- Parexel
- Medpace Holdings
- SIRO Clinpharm
- EVERSANA
Les principaux acteurs du marché de l'externalisation de la pharmacovigilance visent désormais la mondialisation. Par exemple, en décembre 2022, Alphanumeric Systems a lancé une offre de services de pharmacovigilance à plusieurs niveaux destinée aux pionniers des sciences de la vie. Ce nouveau portefeuille englobait la gestion des dossiers, les services de déploiement de stratégies, la gestion des informations médicales et des dossiers, la veille réglementaire, le suivi qualité et les audits. L'entreprise investit continuellement dans les nouvelles technologies pour accroître la productivité de ses services et améliorer la disponibilité dans ce domaine. À cet égard, en décembre 2023, Thermo Fisher Scientific a commercialisé CorEvidence, sa plateforme de data lake cloud, élément clé de son activité de recherche clinique sur les PPD. Cet outil est conçu pour améliorer la qualité du traitement des dossiers de pharmacovigilance et la gestion des données de sécurité. Ces acteurs clés sont :
Développements récents
- En octobre 2024, EVERSANA a choisi Oracle Argus Cloud Service pour optimiser sa plateforme de services de pharmacovigilance. L'entreprise souhaitait améliorer l'expérience client grâce à une gestion simplifiée de la sécurité, une conformité réglementaire et une efficacité opérationnelle.
- En septembre 2024, Oracle a lancé un nouveau service de recherche cloud, CancerMPact Treatment Architecture Trends, destiné aux entreprises pharmaceutiques et biotechnologiques. Cet outil est conçu pour accompagner les clients dans leurs stratégies de développement et de commercialisation pour l'approbation de nouveaux médicaments ciblant les tumeurs malignes.
- Report ID: 7363
- Published Date: Aug 26, 2025
- Report Format: PDF, PPT
- Découvrez un aperçu des principales tendances du marché et des insights
- Passez en revue des tableaux de données d’échantillon et des analyses par segment
- Découvrez la qualité de nos représentations visuelles de données
- Évaluez la structure de notre rapport et notre méthodologie de recherche
- Jetez un coup d’œil à l’analyse du paysage concurrentiel
- Comprenez comment les prévisions régionales sont présentées
- Évaluez la profondeur des profils d’entreprise et du benchmarking
- Visualisez comment des insights exploitables peuvent soutenir votre stratégie
Explorez des données et des analyses réelles
Questions fréquemment posées (FAQ)
Externalisation de la pharmacovigilance Portée du rapport de marché
L’échantillon gratuit comprend la taille actuelle et historique du marché, les tendances de croissance, des graphiques et tableaux régionaux, des profils d’entreprises, des prévisions par segment, et plus encore.
Contactez notre expert
Droits d’auteur © 2026 Research Nester. Tous droits réservés.




