Perspectives du marché de l'amifampridine :
Le marché de l'amifampridine était évalué à 162 millions de dollars en 2025 et devrait atteindre 349,7 millions de dollars d'ici fin 2035, avec un taux de croissance annuel composé (TCAC) de 8 % sur la période de prévision, soit de 2026 à 2035. En 2026, la taille du marché de l'amifampridine est estimée à 174,9 millions de dollars.

Le marché mondial de l'amifampridine connaît des transformations importantes dues à son utilisation croissante dans le traitement du syndrome myasthénique de Lambert-Eaton (SMLE) et à l'augmentation des autorisations de mise sur le marché de médicaments orphelins. Le SMLE se divise généralement en deux sous-types : auto-immun (SMLE-A) et paranéoplasique (SMLE-P). Environ 50 % des cas de SMLE sont associés à une affection maligne sous-jacente, notamment un cancer du poumon à petites cellules (CPPC). Dans le contexte de la charge de morbidité, des études suggèrent que le SMLE survient chez environ 3 % des patients atteints de CPPC et, inversement, environ 40 à 70 % des personnes chez qui un SMLE est diagnostiqué sont également atteintes de CPPC. Bien que les taux d'incidence et de prévalence du SMLE à l'échelle mondiale soient incertains, une étude populationnelle publiée par Frontiers en août 2025 a apporté quelques éclaircissements. Les Pays-Bas ont enregistré une prévalence de 2,3 cas par million d'habitants et un taux d'incidence de 0,5 cas par million d'habitants, tandis que les États-Unis ont rapporté un taux de prévalence de 2,6 cas par million d'habitants. À l'échelle mondiale, la prévalence estimée du syndrome de Lambert-Eaton est de 2,8 cas par million d'habitants, ce qui le classe parmi les maladies rares.
Turquie : Résumé épidémiologique de la population de patients atteints du syndrome de Lambert-Eaton (2015-2024)
Paramètre | Données rapportées |
Cas confirmés de LEMS (2015-2024) | 159 |
Population nationale (2024) | 85 664 944 |
Âge médian au moment du diagnostic | 60 ans (de 16 à 88 ans) |
Âge moyen ± écart-type | 58,1 ± 14,9 ans |
Répartition par sexe | Femmes : 55,3 % (n = 88) ; Hommes : 44,7 % (n = 71) |
Cas P-LEMS | 59,7 % (n = 95) |
Cas A-LEMS | 40,3 % (n = 64) |
Association SCLC (au sein du P-LEMS) | 55,8 % (n = 53) |
Incidence annuelle (2015–2024) | 0,09 à 0,30 par million (0,27/million en 2024) |
Prévalence globale (2024) | 1,11 par million |
Prévalence de l'A-LEMS (2024) | 0,60 par million |
Prévalence du P-LEMS (2024) | 0,51 par million |
Mortalité | A-LEMS : 23,4 % ; P-LEMS : 58,9 % |
Utilisation des médicaments (sur ordonnance) | Pyridostigmine : 65,4 % ; Amifampridine : 24,5 % |
Répartition géographique | Le plus haut de la mer Noire, de la mer Égée et de l'Anatolie centrale |
Source : Institut statistique turc, Frontiers
Résumé des essais cliniques
Des essais cliniques ont démontré l'efficacité de la 3,4-diaminopyridine (3,4-DAP), ou amifampridine, pour améliorer la transmission neuromusculaire et la force musculaire. Plusieurs études ont mis en évidence une amélioration des scores rapportés par les patients par rapport au placebo. Ces résultats ont conduit à l'obtention d'autorisations réglementaires auprès d'organismes tels que la FDA américaine et l'EMA. L'amifampridine s'est imposée comme le traitement de référence du syndrome de Lambert-Eaton (LEMS), et des études sont actuellement menées pour optimiser ses formulations et élargir ses applications neuromusculaires. Son développement représente une avancée majeure dans le traitement pharmacologique des maladies rares, offrant une meilleure fonctionnalité et une meilleure qualité de vie aux patients atteints de troubles invalidants de la transmission neuromusculaire.
1. Phosphate d'amifampridine pour le traitement des syndromes myasthéniques congénitaux
Champ | Détails |
Identifiant ClinicalTrials.gov | NCT02562066 |
Résumé | Étude croisée randomisée, en double aveugle, contrôlée, ambulatoire, à deux périodes et deux traitements, visant à évaluer l'efficacité et l'innocuité du phosphate d'amifampridine chez les patients (âgés de 2 ans et plus) présentant certains sous-types génétiques de CMS ayant démontré un bénéfice durable en ouvert (phosphate d'amifampridine) ou des antécédents de bénéfice durable. |
État du recrutement | Complété |
Conditions / Indication | Syndromes myasthéniques congénitaux |
Intervention(s) | Médicament : phosphate d’amifampridine (voie orale) – poursuite de l’étude versus placebo (étude en aveugle pendant les périodes de croisement) |
Phase | Phase 3 |
Type d'études | interventionnel |
Tranche d'âge (admissible) | Minimum : 2 ans ; Maximum : 70 ans |
Effectif / Taille de l'échantillon | Non fourni dans l'extrait |
Exigence de rodage clé | Phase d'escalade thérapeutique/de rodage en ouvert et non masquée pouvant durer jusqu'à 4 semaines, jusqu'à l'obtention d'une dose/fréquence stable pendant 7 jours avant la randomisation. |
Objectif principal / Point final (implicite) | Évaluer l'efficacité et l'innocuité du phosphate d'amifampridine par rapport à un placebo dans le syndrome métabolique. (Le texte exact du critère d'évaluation principal n'est pas fourni dans l'extrait.) |
Critères d'exclusion | 1. Sous-types de CMS : déficit en acétylcholinestérase, syndrome des canaux lents, déficit en LRP4, déficit en plectine. 2. Anomalies de la conduction cardiaque à l'ECG de dépistage. 3. Trouble convulsif. 4. Tests de la fonction hépatique anormaux lors du dépistage. 5. Tests de la fonction rénale anormaux lors du dépistage. 6. Valeurs anormales des électrolytes lors du dépistage. 7. Grossesse/allaitement ou projet de grossesse. 8. Toute infection systémique cliniquement significative non traitée. 9. Traitement par un autre médicament/dispositif/produit biologique expérimental dans les 30 jours précédant la sélection. 10. Toute autre affection médicale susceptible d’interférer avec le risque ou d’en augmenter le risque, selon l’enquêteur. 11. Antécédents d’allergie aux substances contenant de la pyridine ou aux excipients de l’étude. |
Contact principal / Lieu | Hôpital pour enfants de Boston |
Date de téléchargement/enregistrement | 2021-04-02 |
Source : Hôpital pour enfants de Boston
2. Phosphate d'amifampridine
Section | Détails |
Date de l'autorisation | 31 juillet 2020 |
Parrainer | KYE Pharmaceuticals Inc. |
État d'approbation de Santé Canada | NOC |
Voie d'examen de Santé Canada | Examen prioritaire |
Comparateur | Placebo (études de sevrage) |
Objectif thérapeutique | Amélioration de la qualité de vie liée à la santé (QVLS) et des activités fonctionnelles de la vie quotidienne (AVQ) |
Méthodes d’évaluation (selon un expert clinique de l’ACMTS) | Réponse subjective du patient ; examen neurologique objectif ; 3TUG (Triple Timed-Up-and-Go) ou QMGS ; étude électrophysiologique (amplitude CMAP avant/après contraction volontaire maximale). |
Essais cliniques pivots inclus | 1. LMS-002 2. LMS-003 |
Conception de l'étude | Études de sevrage de phase III, multicentriques, randomisées, en double aveugle et contrôlées par placebo |
Objectif principal | Évaluer l'innocuité et l'efficacité du phosphate d'amifampridine chez les patients adultes atteints de syndrome de Lambert-Eaton (LEMS). |
Points saillants de l'admissibilité | Patients adultes atteints de LEMS confirmé ; naïfs à l'amifampridine, une amélioration QMGS ≥ 3 points était requise pendant la période de rodage ; tous les patients nécessitaient ≥ 91 jours d'amifampridine antérieure et ≥ 7 jours de dosage stable. |
Utilisation continue | Les patients répondeurs devraient poursuivre le traitement à vie. Les patients non répondeurs l'interrompent selon des critères subjectifs et objectifs combinés (réponse du patient, examen neurologique, 3TUG/QMGS, électrophysiologie). |
Conclusion (implicite) de l'ACMTS | Le phosphate d'amifampridine démontre une efficacité statistiquement significative par rapport au placebo dans les études de sevrage du syndrome de Lambert-Eaton ; les améliorations des résultats fonctionnels et les bénéfices rapportés par les patients confirment sa pertinence clinique ; profil de sécurité acceptable. |
Source : NCBI, CADTH (Agence canadienne des médicaments et des technologies de la santé) – Revue clinique, 2024
Clé Amifampridine Résumé des informations sur le marché:
Points saillants régionaux :
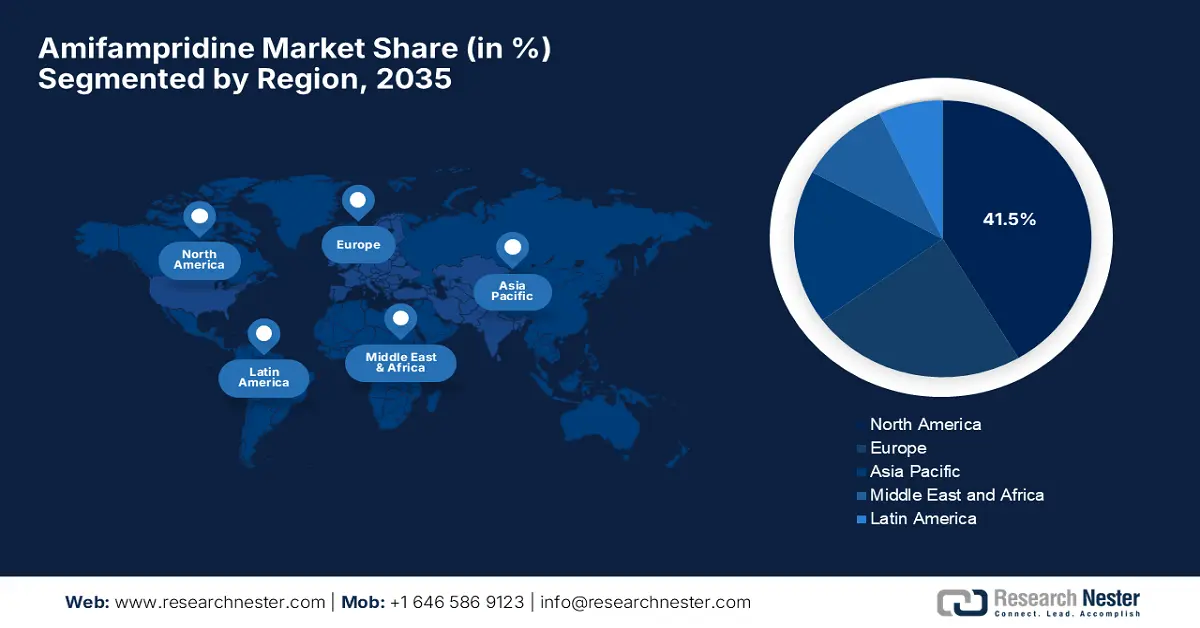
- Le marché nord-américain de l'amifampridine devrait représenter une part d'environ 41,5 % d'ici 2035, grâce à une infrastructure médicale solide et à une sensibilisation croissante aux maladies neuromusculaires.
- Le marché Asie-Pacifique devrait connaître une croissance significative entre 2026 et 2035, en raison de l'augmentation des cas de maladies neuromusculaires et d'un meilleur accès aux traitements.
Analyse du segment :
- Le segment générique devrait représenter la part la plus importante (75,4 %) du marché de l'amifampridine d'ici 2035, sous l'effet de la demande croissante de solutions thérapeutiques abordables.
- Le segment de la myasthénie grave devrait représenter une part lucrative entre 2026 et 2035, en raison de la prévalence croissante de cette maladie traitable par l'amifampridine.
Principales tendances de croissance :
- Priorité à la réduction du coût des médicaments pour garantir leur accessibilité financière.
- Augmentation des investissements dans les activités de recherche
Principaux défis :
- Coûts de traitement élevés et obstacles réglementaires
Acteurs clés : Catalyst Pharmaceuticals (États-Unis), BioMarin Pharmaceutical (États-Unis), Jacobus Pharmaceutical (États-Unis), Medunik Canada (Canada), ORSPEC Pharma (Australie), Shilpa Medicare (Inde), SERB SA (France), Tiefenbacher Pharmaceuticals (Allemagne), Chiracon GmbH (Allemagne), Zydus Cadila (Inde), Apotex (Canada), Sandoz (Suisse), Teva Pharmaceuticals (Israël).
Mondial Amifampridine Marché Prévisions et perspectives régionales:
Taille du marché et projections de croissance :
- Taille du marché en 2025 : 162 millions de dollars américains
- Taille du marché en 2026 : 174,9 millions de dollars américains
- Taille du marché prévue : 349,7 millions de dollars américains d'ici 2035
- Prévisions de croissance : TCAC de 8 % (2026-2035)
Dynamiques régionales clés :
- Principale région : Amérique du Nord (part de marché de 41,5 % d’ici 2035)
- Région à la croissance la plus rapide : Asie-Pacifique
- Pays dominants : États-Unis, Allemagne, France, Japon, Chine
- Pays émergents : Inde, Malaisie, Corée du Sud, Brésil, Mexique
Last updated on : 3 November, 2025
Marché de l'amifampridine - Facteurs de croissance et défis
Facteurs de croissance
- Priorité à la réduction du coût des médicaments pour améliorer leur accessibilité : L’analyse des prix des payeurs réalisée par le NCBI en juillet 2022 indique que le traitement par Firdapse coûte environ 51 993 USD par an et par patient au Canada. L’ACMTS prévoit qu’une réduction supplémentaire des coûts est essentielle pour favoriser la pénétration du marché et atteindre le seuil de consentement à payer de 50 000 USD. Selon l’examen clinique de l’ACMTS de 2020, le prix soumis du phosphate d’amifampridine était de 21,90 USD par comprimé de 10 mg, soit 20 % de moins que le coût public de l’amifampridine base. À la dose quotidienne habituelle de 61,5 mg, le traitement par phosphate d’amifampridine et par base coûte respectivement 51 993 USD et 65 051 USD par patient et par an. Les économies annuelles réalisées grâce au phosphate d’amifampridine s’élèvent à 13 058 USD par patient, hors frais d’ordonnance et majorations.
Résumé des résultats de l'évaluation économique du promoteur (KYE Pharmaceuticals Inc.)
Médicament | Coût total des médicaments ($) | Coûts supplémentaires des médicaments ($) | Coût total ($) | Coûts supplémentaires ($) |
Phosphate d'amifampridine | 51 993 | Référence | 55 220 | Référence |
Amifampridine | 65 051 | –13 058 | 69 062 | –13 841 |
Source : Revue clinique de l'ACMTS
- Augmentation des investissements dans la recherche : Un autre facteur majeur de croissance du marché de l’amifampridine réside dans la hausse des investissements en recherche et développement. À cet égard, le secteur biopharmaceutique, fortement axé sur la recherche, a consacré environ 198 milliards de dollars américains à la R&D à l’échelle mondiale en 2020. Selon le rapport 2022 de la Fédération internationale des fabricants et associations pharmaceutiques (IFPMA), les effets indirects, directs et induits cumulés de la contribution de ce secteur au PIB mondial s’élèvent à 1 838 milliards de dollars américains. Comparées à celles des autres secteurs de haute technologie, les dépenses annuelles de l’industrie biopharmaceutique sont environ 8,1 fois supérieures à celles des industries aérospatiales et de défense, 7,2 fois supérieures à celles du secteur chimique et 1,2 fois supérieures à celles du secteur des logiciels et des services informatiques.
Dépenses en R&D biopharmaceutique
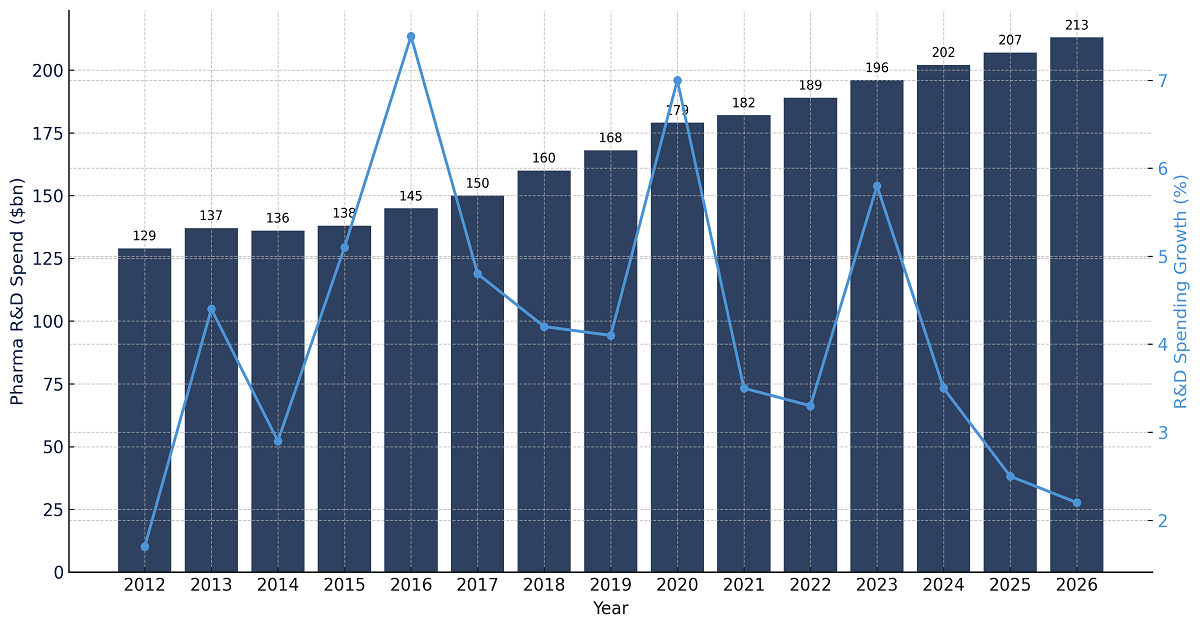
Source : IFPMA
Défis
- Coûts de traitement élevés et obstacles réglementaires : il s’agit là d’un des principaux freins à l’entrée sur le marché de l’amifampridine dans la quasi-totalité des pays. Les coûts élevés des traitements de pointe les rendent inabordables pour les populations des régions où les prix sont un facteur déterminant. Les contraintes budgétaires constituent un obstacle majeur à la pénétration du marché dans tous les pays. Outre l’existence de réglementations strictes garantissant la sécurité thérapeutique, celles-ci peuvent également freiner la constitution d’une clientèle importante pour l’amifampridine. Ces difficultés réglementaires entraînent des retards d’entrée sur le marché, fréquemment observés dans des régions clés comme le Japon et le Canada.
Taille et prévisions du marché de l'amifampridine :
| Attribut du rapport | Détails |
|---|---|
|
Année de base |
2025 |
|
Année prévisionnelle |
2026-2035 |
|
TCAC |
8% |
|
Taille du marché de l'année de référence (2025) |
162 millions de dollars américains |
|
Taille du marché prévisionnelle pour l'année 2035 |
349,7 millions de dollars américains |
|
Portée régionale |
|
Segmentation du marché de l'amifampridine :
Analyse de segmentation par type
Le segment des génériques devrait représenter la plus grande part de marché, soit 75,4 %, d'ici fin 2035. Cette domination s'explique par la demande croissante de solutions thérapeutiques abordables dans le monde entier. Les médicaments génériques constituent la base de traitements économiques, rendant les soins accessibles à un plus grand nombre de consommateurs et représentant une alternative idéale aux médicaments de marque. Par exemple, les Centers for Medicare & Medicaid Services (CMS) ont mis en place des programmes visant à encourager l'utilisation des génériques, tant pour les patients que pour les professionnels de santé, contribuant ainsi à la réduction des dépenses médicales et, par conséquent, à la croissance de ce segment.
Analyse du segment d'application
Le segment de la myasthénie grave devrait représenter une part importante du marché de l'amifampridine au cours de la période de prévision. La croissance de ce segment est attribuable à l'augmentation des cas de cette maladie, potentiellement traitables par l'amifampridine grâce à sa grande efficacité. De plus, l'amifampridine est considérée comme très efficace pour améliorer l'état de santé des patients en réduisant les hospitalisations, ce qui explique son utilisation généralisée sur divers marchés à travers le monde.
Notre analyse approfondie du marché comprend les segments suivants :
Segment | Sous-segments |
Taper |
|
Application |
|
Utilisateur final |
|
Données démographiques des patients |
|

Vishnu Nair
Responsable du développement commercial mondialPersonnalisez ce rapport selon vos besoins — contactez notre consultant pour des informations et des options personnalisées.
Marché de l'amifampridine - Analyse régionale
Aperçu du marché nord-américain
Le marché nord-américain devrait représenter environ 41,5 % du marché mondial d'ici fin 2035. La croissance de la région s'explique par la solidité de son infrastructure médicale, la sensibilisation accrue aux maladies neuromusculaires et un cadre réglementaire rigoureux. Par ailleurs, la région bénéficie d'investissements importants de la part des organismes de santé publics et privés en faveur des maladies rares. Elle abrite un grand nombre de centres de neurologie qui facilitent le diagnostic précoce, permettant ainsi d'offrir des solutions fiables aux patients dont les besoins médicaux ne sont pas satisfaits.
Les États-Unis dominent le marché nord-américain de l'amifampridine grâce aux investissements des organismes de santé publique dans la prise en charge des maladies neuromusculaires rares. Par exemple, les Centers for Medicare & Medicaid Services (CMS) ont considérablement augmenté les dépenses de santé consacrées aux traitements neuromusculaires. De plus, ils ont annoncé l'élargissement de la couverture des thérapies pour les maladies rares, incluant l'amifampridine, afin d'améliorer l'accès des patients aux soins. Par ailleurs, les National Institutes of Health ont alloué des fonds importants à la recherche, témoignant de la vigueur du marché. Le tableau ci-dessous présente les dépenses totales consacrées à la recherche biopharmaceutique, y compris sur l'amifampridine, en 2020.
Dépenses de R&D aux États-Unis, 2020
Fonction | Dollars (millions de dollars américains) | Partager (%) |
Pré-humain / Pré-clinique | 13 604,0 | 14,9% |
Phase I | 6 968,3 | 7,6% |
Phase II | 8 429,4 | 9,3% |
Phase III | 24 773,1 | 27,2% |
Approbation | 3 932,5 | 4,3% |
Phase IV | 10 512,4 | 11,5% |
Non classé | 22 906,6 | 25,1% |
Recherche et développement total | 91 126,3 | 100,0% |
Source : IFPMA
Le marché canadien de l'amifampridine présente un fort potentiel, porté par une vaste clientèle et des initiatives de financement gouvernementales. Les dépenses facturées au Canada pour les médicaments génériques et biosimilaires s'élevaient à 27,4 milliards de dollars américains et devraient atteindre 32 à 36 milliards de dollars américains d'ici fin 2026, soit une croissance annuelle composée de 3 à 6 %, soulignant ainsi l'importance économique de ce secteur. De plus, les ministères provinciaux de la Santé, comme ceux de l'Ontario et de la Colombie-Britannique, ont accru leurs investissements, ce qui se traduit chaque année par des bénéfices pour les patients atteints du syndrome de Lambert-Eaton. Ces facteurs devraient donc stimuler le marché canadien et offrir des perspectives de croissance prometteuses d'ici 2035.
Perspectives du marché APAC
Le marché Asie-Pacifique devrait connaître une croissance significative au cours de la période prévisionnelle, en raison de l'augmentation des cas de maladies neuromusculaires, de l'amélioration de l'accès aux traitements et des investissements substantiels des gouvernements de la région dans le secteur de la santé. Par ailleurs, cette croissance est tributaire du développement de pays comme le Japon, la Chine, l'Inde, la Malaisie et la Corée du Sud. Ces facteurs contribuent à la dynamique du marché, avec pour objectif d'améliorer la prise en charge des patients et, par conséquent, de stimuler l'expansion du secteur.
Le marché indien offre des perspectives de croissance remarquables, portées par la demande croissante d'amifampridine. En 2023, par exemple, les dépenses de santé du pays ont atteint 2,1 % du PIB, une part considérable étant allouée au système de santé et aux initiatives thérapeutiques. L'Inde a connu une forte augmentation des dépenses liées aux maladies rares, en raison du déséquilibre persistant entre l'offre et la demande de traitements. On dénombre environ 8 000 maladies rares en Inde, dont seulement 5 % bénéficient d'un traitement, touchant ainsi près d'un cinquième de la population.
Le marché chinois de l'amifampridine bénéficie d'une visibilité accrue grâce au soutien important des autorités chinoises. Des facteurs tels que des politiques administratives favorables créent un environnement commercial propice aux acteurs nationaux. Les dépenses publiques consacrées aux maladies rares en Chine ont considérablement augmenté ces cinq dernières années, témoignant d'une prise de conscience croissante de la nécessité de prendre en charge ces pathologies complexes. Par ailleurs, la Chine est le premier exportateur de composés d'aniline, principalement utilisés pour la production d'amifampridine. Selon l'OEC, la valeur des exportations de composés d'aniline s'élevait à 2,57 milliards de dollars en 2023, et l'excédent commercial à 1,83 milliard de dollars, confirmant la position dominante de la Chine dans la production et les exportations mondiales de ces produits.
Aperçu du marché européen
Au cours de la période prévisionnelle, le marché européen de l'amifampridine devrait connaître des opportunités de croissance lucratives grâce à la dynamique de développement de pays comme l'Allemagne et la France, qui représentent les parts de revenus les plus importantes.
Le marché allemand bénéficie d'un soutien considérable grâce à des mesures thérapeutiques innovantes et des politiques de remboursement qui visent à positionner le pays comme un acteur majeur en Europe. Par ailleurs, l'adoption de traitements de pointe et la recherche médicale contribuent également à la croissance des entreprises dans la région.
Le marché français est promis à une forte croissance, grâce à son engagement en faveur de l'excellence des services de santé et d'un meilleur accès aux soins. De plus, il bénéficie d'un soutien gouvernemental maximal pour la prise en charge des maladies rares, et le remboursement des médicaments permet d'accompagner l'utilisation accrue de ces traitements. Enfin, les entreprises pharmaceutiques françaises contribuent activement au développement et à l'amélioration des traitements associés.
Principaux acteurs du marché de l'amifampridine :
- Catalyst Pharmaceuticals (États-Unis)
- Présentation de l'entreprise
- Stratégie d'entreprise
- Principaux produits proposés
- Performance financière
- Indicateurs clés de performance
- Analyse des risques
- Développements récents
- Présence régionale
- Analyse SWOT
- BioMarin Pharmaceutical (États-Unis)
- Jacobus Pharmaceutical (États-Unis)
- Medunik Canada (Canada)
- ORSPEC Pharma (Australie)
- Shilpa Medicare (Inde)
- SERB SA (France)
- Tiefenbacher Pharmaceuticals (Allemagne)
- Chiracon GmbH (Allemagne)
- Zydus Cadila (Inde)
- Apotex (Canada)
- Sandoz (Suisse)
- Teva Pharmaceuticals (Israël)
- Catalyst Pharmaceuticals, Inc. est une société biopharmaceutique en phase de commercialisation, basée à Coral Gables, en Floride. L'entreprise se spécialise dans l'acquisition de licences, le développement et la commercialisation de traitements pour les maladies rares. Son produit phare, FIRDAPSE, est le seul traitement fondé sur des preuves et approuvé par la FDA pour les patients adultes atteints du syndrome de Lambert-Eaton (LEMS). Catalyst Pharmaceuticals a lancé la commercialisation du produit en janvier 2019, après son approbation par la FDA en novembre 2018.
- BioMarin Pharmaceutical Inc. est une société de biotechnologie américaine basée à San Rafael, en Californie, spécialisée dans les traitements des maladies rares et orphelines. BioMarin développe, acquiert et commercialise des thérapies pour les affections graves ou rares. Son portefeuille de produits comprend des thérapies de remplacement enzymatique, des médicaments orphelins à petites molécules et des médicaments neuromusculaires. Sa stratégie privilégie les incitations réglementaires (désignations de médicaments orphelins, périodes d'exclusivité) et un déploiement mondial pour les indications des maladies rares.
- Jacobus Pharmaceutical Company, Inc. est une société pharmaceutique américaine privée dont le siège social est situé à Princeton/Plainsboro, dans le New Jersey. Elle est spécialisée dans le développement et la fabrication de médicaments pour les maladies rares, souvent à base de petites molécules. Jacobus est notamment connue pour la production et la distribution de l'amifampridine (également appelée 3,4-diaminopyridine ou 3,4-DAP) sous le nom de marque Ruzurgi, en particulier pour les enfants et adolescents (de 6 à 16 ans) atteints du syndrome myasthénique de Lambert-Eaton (SMLE).
- Fondée en décembre 2009, Médunik Canada est une filiale du Groupe pharmaceutique Duchesnay (GPD). Sa mission est d’améliorer la santé et la qualité de vie des Canadiens atteints de maladies rares en collaborant avec des entreprises internationales pour commercialiser des médicaments orphelins au Canada. Le siège social de Médunik Canada est situé au Québec, au Canada, et fait partie du réseau du GPD.
- Orspec Pharma se présente comme une société pharmaceutique spécialisée dans l'accès aux médicaments pour les patients atteints de maladies rares ou ayant des besoins spécifiques. Présente en Asie-Pacifique, elle se concentre sur l'approvisionnement nominatif, l'enregistrement des médicaments orphelins et les programmes d'accès précoce. Son siège social semble être situé en Australie (West Gosford, Nouvelle-Galles du Sud), et ses activités couvrent les marchés de la région Asie-Pacifique.
Voici une liste des principaux acteurs opérant sur le marché mondial :
Les entreprises du marché de l'amifampridine mettent l'accent sur plusieurs actions stratégiques pour renforcer leur présence mondiale. Des sociétés comme Catalyst Pharmaceuticals et BioMarin Pharmaceutical ont bénéficié d'une forte visibilité grâce à l'innovation et à la commercialisation de Firdapse. Par ailleurs, Medunik Canada et Jacobus Pharmaceutical ont facilité l'accès des patients à Ruzurgi, un médicament destiné aux enfants. Enfin, ces entreprises privilégient également le développement de leur portefeuille de produits, le financement d'initiatives et la promotion d'une saine concurrence.
Développements récents
- En août 2025, Catalyst Pharmaceuticals, Inc. a annoncé que la société et son concédant de licence SERB SA avaient signé un accord à l'amiable avec Lupin Pharmaceuticals, Inc. et Lupin Ltd. qui met fin au litige en matière de brevets intenté par Catalyst et SERB en réponse à la demande abrégée de nouveau médicament (ANDA) de Lupin visant à obtenir l'approbation pour le lancement d'une version générique des comprimés de FIRDAPSE 10 mg.
- En janvier 2025, Tiefenbacher Pharmaceuticals a annoncé le lancement de l'amifampridine en Europe. Ce médicament générique est destiné au traitement du syndrome myasthénique de Lambert-Eaton sur l'ensemble du continent européen, assurant ainsi une présence significative sur le marché.
- Report ID: 7694
- Published Date: Nov 03, 2025
- Report Format: PDF, PPT
- Découvrez un aperçu des principales tendances du marché et des insights
- Passez en revue des tableaux de données d’échantillon et des analyses par segment
- Découvrez la qualité de nos représentations visuelles de données
- Évaluez la structure de notre rapport et notre méthodologie de recherche
- Jetez un coup d’œil à l’analyse du paysage concurrentiel
- Comprenez comment les prévisions régionales sont présentées
- Évaluez la profondeur des profils d’entreprise et du benchmarking
- Visualisez comment des insights exploitables peuvent soutenir votre stratégie
Explorez des données et des analyses réelles
Questions fréquemment posées (FAQ)
Amifampridine Portée du rapport de marché
L’échantillon gratuit comprend la taille actuelle et historique du marché, les tendances de croissance, des graphiques et tableaux régionaux, des profils d’entreprises, des prévisions par segment, et plus encore.
Contactez notre expert
Droits d’auteur © 2026 Research Nester. Tous droits réservés.




