Perspectives du marché des dispositifs de thérapie cellulaire allogénique :
Le marché des dispositifs de thérapie cellulaire allogénique représentait plus de 494,62 millions USD en 2025 et devrait atteindre 4,91 milliards USD d'ici 2035, avec un taux de croissance annuel composé (TCAC) d'environ 25,8 % sur la période 2026-2035. En 2026, le marché des dispositifs de thérapie cellulaire allogénique devrait atteindre 609,47 millions USD.

Le marché des dispositifs de thérapie cellulaire allogénique connaît un essor considérable dans le domaine médical, notamment dans le traitement du cancer, des maladies auto-immunes et des affections dégénératives. De plus, les progrès de la médecine régénérative, le financement accru des essais cliniques et la prévalence croissante des maladies chroniques nécessitent de nouvelles approches thérapeutiques. Par exemple, en mars 2023, TCR Therapeutics Inc. et Adaptimmune Therapeutics plc ont annoncé la signature d'un accord définitif prévoyant la fusion d'Adaptimmune et de TCR², dans le cadre d'une transaction entièrement en actions, pour former une entreprise leader en thérapie cellulaire spécialisée dans le traitement des tumeurs solides.
De plus, les collaborations des entreprises de biotechnologie avec d'autres organismes de recherche favoriseront l'innovation en matière d'approvisionnement et de traitement des cellules, ainsi que de mécanismes d'administration, stimulant ainsi la demande pour ces produits. Grâce à ces avancées et à la prise de conscience croissante du potentiel thérapeutique des interventions à base de cellules allogéniques, le marché des dispositifs de thérapie cellulaire allogénique devrait connaître une croissance future. Par exemple, en juin 2023, Lonza et Vertex Pharmaceuticals Incorporated ont annoncé la création d'une coentreprise pour soutenir la production de la gamme de traitements expérimentaux à base de cellules souches de Vertex. Plus précisément, les programmes VX-880 et VX-264, actuellement en essais cliniques, sont destinés à aider les personnes atteintes de diabète de type 1 (DT1).
De plus, les avancées réglementaires et la mise en place de bonnes pratiques et d'installations de fabrication pour ces traitements, qui les placent dans les normes de sécurité et de qualité, contribuent à la croissance de ce marché. Par exemple, en décembre 2024, BioCentriq a signé un bail à long terme avec National Business Parks pour une usine de fabrication de thérapie cellulaire de pointe. Celle-ci comprendra un investissement de 12 millions de dollars américains en équipements, en améliorations des systèmes d'exploitation et en modernisation des installations. Cela consolidera la position de BioCentriq dans le secteur en pleine expansion de la thérapie cellulaire et renforcera sa capacité à offrir des solutions complètes de développement, de fabrication et de contrôle qualité.
Clé Dispositifs de thérapie cellulaire allogénique Résumé des informations sur le marché:
Points forts régionaux :
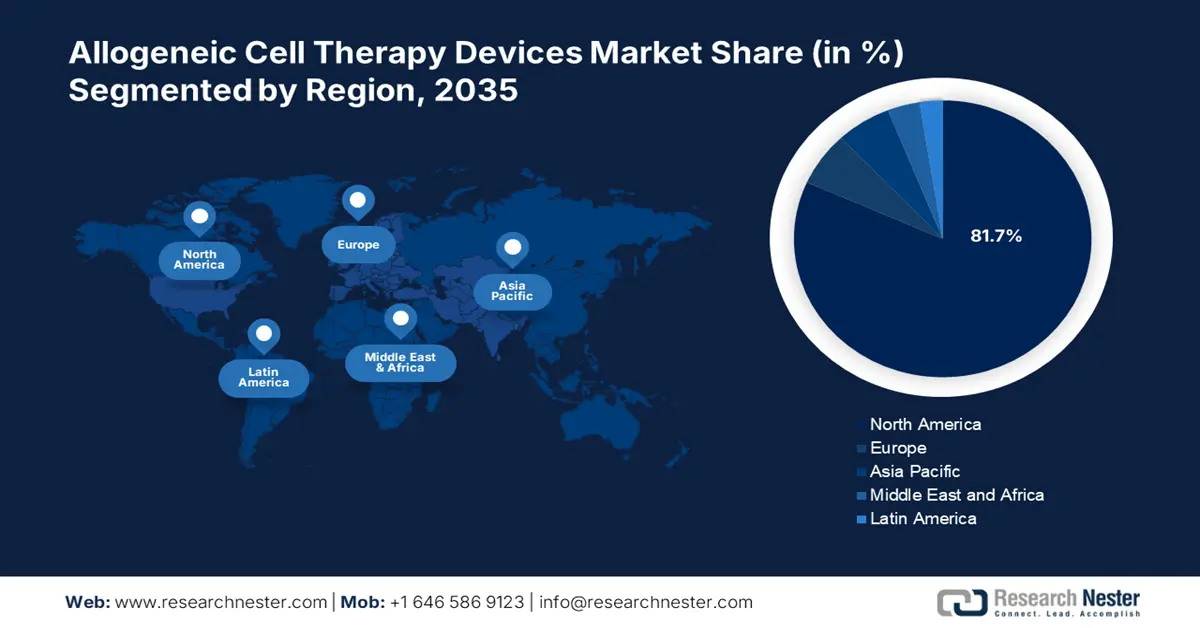
- Le marché nord-américain des dispositifs de thérapie cellulaire allogénique représentera 81,70 % du marché d'ici 2035, grâce à la présence d'acteurs pharmaceutiques majeurs et aux innovations en matière de thérapies cellulaires.
- Le marché Asie-Pacifique connaîtra une croissance lucrative au cours de la période de prévision 2026-2035, grâce au développement croissant de la médecine personnalisée et des thérapies cellulaires dans la région.
Analyses sectorielles :
- Le segment des thérapies par cellules souches sur le marché des dispositifs de thérapie cellulaire allogénique devrait atteindre une part de marché de 51,20 % d’ici 2035, grâce aux progrès des technologies de fabrication et de traitement qui améliorent l’évolutivité.
Principales tendances de croissance :
- Simplification du processus d'approbation
- Investissements et consortiums de recherche
Défis majeurs :
- Paysage concurrentiel
Acteurs clés : Atara Biotherapeutics, Mallinckrodt Pharmaceuticals, STEMPEUTICS RESEARCH PVT LTD, Biosolution Co., Ltd., MEDIPOST Co., Ltd., et plus encore.
Mondial Dispositifs de thérapie cellulaire allogénique Marché Prévisions et perspectives régionales:
Taille du marché et projections de croissance :
- Taille du marché 2025 : 494,62 millions USD
- Taille du marché 2026 : 609,47 millions USD
- Taille du marché projetée : 4,91 milliards USD d'ici 2035
- Prévisions de croissance : TCAC de 25,8 % (2026-2035)
Dynamiques régionales clés :
- Plus grande région : Amérique du Nord (part de 81,7 % d’ici 2035)
- Région à la croissance la plus rapide : Asie-Pacifique
- Pays dominants : États-Unis, Allemagne, Chine, Japon, Royaume-Uni
- Pays émergents : Chine, Inde, Japon, Corée du Sud, Singapour
Last updated on : 18 September, 2025
Moteurs de croissance et défis du marché des dispositifs de thérapie cellulaire allogénique :
Moteurs de croissance
- Processus d'approbation simplifié : Il améliore le parcours des thérapies innovantes vers le milieu clinique. Les agences réglementaires, dont la FDA américaine, ouvrent la voie à un examen plus rapide des produits allogéniques démontrant un potentiel clinique significatif. Ces mécanismes simplifiés réduisent les délais de mise sur le marché des thérapies innovantes tout en diminuant les coûts de développement associés. Le tableau ci-dessous présente :
Produits de thérapie cellulaire et génique approuvés
Produits approuvés et nom commercial | Fabricant | Année |
ABECMA (idécabtagène vicleucel) | Celgene Corporation, une société Bristol-Myers Squibb | 2024 |
ADSTILADRIN (nadofaragene firadenovecvcng) | Ferring Pharmaceuticals A/S | 2024 |
ALLOCORD (HPC, sang de cordon) | Centre médical pour enfants SSM Cardinal Glennon | 2019 |
AMTAGVI (lifileucel) | Iovance Biotherapeutics, Inc. | 2024 |
BEQVEZ (fidanacogène elaparvovec-dzkt) | Pfizer, Inc. | 2024 |
BREYANZI (lisocabtagène maraleucel) | Juno Therapeutics, Inc., une société Bristol-Myers Squibb | 2024 |
CARVYKTI (ciltacabtagene autoleucel) | Janssen Biotech, Inc. | 2024 |
CASGEVY (exagammglogène autotemcel [exacel]) | Vertex Pharmaceuticals Incorporated | |
Ducord, sang de cordon HPC | Faculté de médecine de l'Université Duke | |
ELEVIDYS (delandistrogene moxeparvovec-rokl) | Sarapeta Therapeutics, Inc. |
Source : Food & Drug Administration des États-Unis
- Investissements et consortiums de recherche : Ces initiatives renforcent considérablement la capacité d'innovation et de développement. De plus, les consortiums de recherche favorisent l'interdisciplinarité dans la collaboration entre le monde universitaire, les acteurs industriels et les établissements de santé, en partageant connaissances, ressources et expertise. Par exemple, en décembre 2024, afin d'accélérer le développement clinique de sa thérapie allogénique différenciée à base de cellules tueuses naturelles (NK), Indapta Therapeutics, Inc. a annoncé la clôture d'un nouveau tour de financement de 22,5 millions de dollars américains. Ainsi, l'augmentation des investissements et des collaborations de recherche oriente le marché des dispositifs de thérapie cellulaire allogénique vers de meilleurs résultats pour les patients.
Défis
- Rejet immunitaire et réaction du greffon contre l'hôte : La réaction du greffon contre l'hôte (RCH) continue d'influencer les résultats pour les patients et l'efficacité du marché des dispositifs de thérapie cellulaire allogénique. L'incidence de ces réactions à médiation immunitaire nécessite une compatibilité rigoureuse des donneurs et des receveurs, ainsi que des protocoles de prétraitement détaillés afin de réduire les risques. De plus, ces défis impacteront également la confiance des cliniciens et l'acceptation des patients, ce qui impactera la pénétration du marché et l'adoption plus large des thérapies allogéniques. Pour assurer une croissance durable des dispositifs de thérapie cellulaire allogénique, il est essentiel de surmonter ces obstacles immunologiques et d'améliorer les résultats cliniques.
- Paysage concurrentiel : Sur le marché des dispositifs de thérapie cellulaire allogénique, la concurrence croissante représente un défi majeur, car le secteur est très dynamique, avec un grand nombre d'acteurs en compétition pour les parts de marché et l'acceptation clinique. Cette explosion des thérapies allogéniques et autologues favorise une concurrence féroce entre les entreprises, susceptible d'entraîner des baisses de prix et une réduction des marges bénéficiaires, limitant ainsi le potentiel de programmes innovants rentables. Un marché saturé risque de compliquer la différenciation de la proposition de valeur pour obtenir l'approbation réglementaire et la validation clinique, les entreprises étant confrontées à une forte concurrence. Par conséquent, un positionnement stratégique et des partenariats solides deviennent indispensables pour mener à bien cette dynamique concurrentielle.
Taille et prévisions du marché des dispositifs de thérapie cellulaire allogénique :
| Attribut du rapport | Détails |
|---|---|
|
Année de base |
2025 |
|
Période de prévision |
2026-2035 |
|
TCAC |
25,8% |
|
Taille du marché de l'année de référence (2025) |
494,62 millions USD |
|
Taille du marché prévue pour l'année (2035) |
4,91 milliards USD |
|
Portée régionale |
|
Segmentation du marché des dispositifs de thérapie cellulaire allogénique :
Thérapie
Sur le marché des dispositifs de thérapie cellulaire allogénique, le segment des thérapies par cellules souches devrait représenter plus de 51,2 % du chiffre d'affaires d'ici 2035. L'utilisation de la thérapie par cellules souches offre une flexibilité dans les protocoles thérapeutiques, améliorant ainsi les résultats pour les patients et augmentant l'utilité clinique. Les progrès des technologies de fabrication et de traitement ont simplifié la mise en œuvre des thérapies par cellules souches, rendant les pratiques évolutives et cohérentes tout en réduisant les risques de sécurité. Par exemple, en décembre 2024, la FDA américaine a approuvé Ryoncil, une thérapie allogénique à base de cellules stromales mésenchymateuses (CSM) issues de donneurs. Elle est conçue pour traiter les enfants de deux mois et plus atteints de réaction aiguë du greffon contre l'hôte (R-aGVHD) réfractaire aux stéroïdes. Ryoncil est le premier traitement à base de CSM approuvé par la FDA.
Domaines thérapeutiques
Sur la base des domaines thérapeutiques, le segment des troubles hématologiques sur le marché des dispositifs de thérapie cellulaire allogénique devrait connaître des perspectives de croissance remarquables d'ici 2035. Cela s'explique principalement par la forte prévalence de ces affections, notamment la leucémie, le lymphome et plusieurs anémies, qui nécessitent des traitements innovants. La greffe allogénique de cellules souches hématopoïétiques (GCSH) est désormais un traitement courant qui promet la guérison de ces tumeurs malignes en remplaçant les cellules sanguines malades par des cellules saines provenant de donneurs grâce à des dispositifs efficaces. Par exemple, en octobre 2024, Agappe a dévoilé la série Mispa i200, un analyseur CLIA immunologique basé sur AE, ainsi que son équipement d'hématologie de la série HX, une première en son genre, fabriqué en interne. Cet appareil visait à améliorer la rapidité et la précision des analyses sanguines.
Notre analyse approfondie du marché mondial des dispositifs de thérapie cellulaire allogénique comprend les segments suivants :
Thérapie |
|
Domaines thérapeutiques |
|

Vishnu Nair
Responsable du développement commercial mondialPersonnalisez ce rapport selon vos besoins — contactez notre consultant pour des informations et des options personnalisées.
Analyse régionale du marché des dispositifs de thérapie cellulaire allogénique :
Aperçu du marché nord-américain
D'ici 2035, le marché nord-américain des dispositifs de thérapie cellulaire allogénique devrait représenter plus de 81,7 % des revenus. La forte présence des principaux acteurs pharmaceutiques permet des modifications génétiques précises des cellules donneuses afin d'améliorer leurs propriétés thérapeutiques et de réduire le risque de rejet immunitaire. De plus, les récents développements des technologies d'édition génomique, telles que CRISPR/Cas9, ont ouvert de nouvelles perspectives pour les thérapies cellulaires allogéniques.
Les facteurs qui propulsent la croissance rentable du marché américain des dispositifs de thérapie cellulaire allogénique sont les innovations dans le développement de médicaments et l'avancement des traitements NVEL utilisant la thérapie cellulaire pour lutter contre les maladies chroniques. Par exemple, en août 2022, Global Blood Therapeutics, Inc. et Pfizer Inc. ont annoncé la conclusion d'un accord définitif pour l'acquisition de GBT par Pfizer. Cette acquisition a permis la découverte, le développement et la distribution de traitements révolutionnaires qui redonnent espoir aux communautés de patients défavorisés, à commencer par la drépanocytose.
Le marché canadien des dispositifs de thérapie cellulaire allogénique connaît une croissance importante grâce aux investissements et à un écosystème réglementaire souple. Par exemple, en juillet 2024, le gouvernement canadien investit dans un écosystème des sciences de la vie solide, résilient et dynamique, capable de gérer les crises médicales actuelles et à venir. Afin de garantir aux Canadiens l'accès aux technologies médicales les plus récentes, plus de 2,2 milliards de dollars américains ont été investis depuis mars 2020 pour renforcer les capacités nationales de biofabrication et de sciences de la vie.
Aperçu du marché de l'Asie-Pacifique
Le marché des dispositifs de thérapie cellulaire allogénique en Asie-Pacifique prend de l'ampleur et devrait connaître une croissance fulgurante sur la période 2026-2035. Les études cliniques se sont multipliées grâce à l'essor de la médecine personnalisée. De plus, les thérapies cellulaires, notamment celles utilisant des cellules génétiquement modifiées, permettent de proposer des traitements personnalisés ciblant le patrimoine génétique de chaque patient. Cette analyse individualisée transforme la prise en charge des soins en augmentant l'efficacité des traitements et en réduisant les effets secondaires.
Le marché indien des dispositifs de thérapie cellulaire allogénique est en pleine expansion grâce à une réglementation de plus en plus stricte, fruit de l'accessibilité croissante aux technologies et instruments sophistiqués d'ingénierie cellulaire. Par exemple, Bioserve India a annoncé en juillet 2024 le lancement de ses produits de pointe à base de cellules souches en Inde. Le marché indien bénéficiera des avancées en matière de découverte thérapeutique et de médecine régénérative, ainsi que des avancées en recherche scientifique et en développement de médicaments, grâce à ces nouveaux produits REPROCELL.
Le marché chinois des dispositifs de thérapie cellulaire allogénique connaît un essor remarquable grâce aux collaborations stratégiques entre entreprises visant à développer l'expertise et à optimiser les compétences. Par exemple, en janvier 2025, Terumo Blood and Cell Technologies et l'Institut d'inspection des dispositifs médicaux et des emballages pharmaceutiques du Shandong ont signé un protocole d'accord portant sur un partenariat stratégique. Ce partenariat vise à établir une plateforme complète intégrant la production, le monde universitaire, la recherche et les applications afin d'améliorer la communication et la collaboration au sein du secteur des dispositifs médicaux.
Acteurs du marché des dispositifs de thérapie cellulaire allogénique :
- Tego Science Inc.
- Présentation de l'entreprise
- Stratégie d'entreprise
- Offres de produits clés
- Performance financière
- Indicateurs clés de performance
- Analyse des risques
- Développement récent
- Présence régionale
- Analyse SWOT
- Centre médical pour enfants SSM Cardinal Glennon
- Centre de sang de cordon de Cleveland
- Faculté de médecine de l'Université Duke
- Centre du sang de New York
- Clinimmune Labs, banque de sang de cordon de l'Université du Colorado
- Banque de sang de cordon MD Anderson
- Centres de transfusion sanguine communautaires LifeSouth, Inc.
- Bloodworks Nord-Ouest
- Atara Biotherapeutics
- Mallinckrodt Pharmaceuticals
- STEMPEUTICS RESEARCH PVT LTD
- Biosolution Co., Ltd.
- MEDIPOST Co., Ltd.
Les entreprises leaders du marché des dispositifs de thérapie cellulaire allogénique redoublent d'efforts pour créer et lancer de nouvelles thérapies cellulaires pour diverses indications. Les entreprises disposant de solides portefeuilles de produits et de ressources rivalisent pour obtenir les autorisations de mise sur le marché afin de bénéficier d'un avantage concurrentiel dans des applications spécifiques. De plus, elles concluent des alliances et des accords de licence pour préserver leur position sur un marché très concurrentiel. Par exemple, en mai 2023, Johnson & Johnson et Cellular Biomedicine Group ont signé un partenariat mondial et un accord de licence pour développer des traitements CAR-T de nouvelle génération.
Voici la liste de certains acteurs clés du marché des dispositifs de thérapie cellulaire allogénique :
Développements récents
- En février 2024, Atara Biotherapeutics, Inc. a développé des traitements révolutionnaires pour les maladies auto-immunes et les patients atteints de cancer en utilisant sa nouvelle plateforme de cellules T allogéniques du virus d'Epstein-Barr (EBV).
- En novembre 2023, BioCardia, Inc. a annoncé que la FDA avait approuvé l'essai clinique de phase III de thérapie cellulaire autologue CardiAMP pour le traitement des patients atteints d'insuffisance cardiaque ischémique.
- En octobre 2023, Nkarta, Inc. a signalé que la FDA avait approuvé une demande IND pour étudier NKX019, son candidat à la thérapie cellulaire CAR NK allogénique dirigée contre CD19, pour traiter la néphrite lupique.
- Report ID: 7161
- Published Date: Sep 18, 2025
- Report Format: PDF, PPT
- Découvrez un aperçu des principales tendances du marché et des insights
- Passez en revue des tableaux de données d’échantillon et des analyses par segment
- Découvrez la qualité de nos représentations visuelles de données
- Évaluez la structure de notre rapport et notre méthodologie de recherche
- Jetez un coup d’œil à l’analyse du paysage concurrentiel
- Comprenez comment les prévisions régionales sont présentées
- Évaluez la profondeur des profils d’entreprise et du benchmarking
- Visualisez comment des insights exploitables peuvent soutenir votre stratégie
Explorez des données et des analyses réelles
Questions fréquemment posées (FAQ)
Dispositifs de thérapie cellulaire allogénique Portée du rapport de marché
L’échantillon gratuit comprend la taille actuelle et historique du marché, les tendances de croissance, des graphiques et tableaux régionaux, des profils d’entreprises, des prévisions par segment, et plus encore.
Contactez notre expert
Droits d’auteur © 2026 Research Nester. Tous droits réservés.




