Marktausblick für biosimilare monoklonale Antikörper:
Der Markt für biosimilare monoklonale Antikörper hatte im Jahr 2025 ein Volumen von 13,99 Milliarden US-Dollar und wird bis 2035 voraussichtlich 109,99 Milliarden US-Dollar übersteigen. Im Prognosezeitraum von 2026 bis 2035 wird eine jährliche Wachstumsrate (CAGR) von über 22,9 % verzeichnet. Im Jahr 2026 wird der Branchenwert für biosimilare monoklonale Antikörper auf 16,87 Milliarden US-Dollar geschätzt.

Der Markt für die Herstellung und Produktion von antikörperbasierten Medikamenten als Behandlungslösungen entwickelt sich in der Pharmaindustrie rasant. Die Nachfrage nach wirtschaftlich rentablen biologischen Therapien und die steigenden Gesundheitskosten machen Biosimilars zudem zu einer Alternative zu teuren konventionellen Medikamenten. Laut einem im Januar 2024 von der NLM veröffentlichten Artikel steigen die Kosteneinsparungen durch Biosimilars, insbesondere in den USA, mit voraussichtlichen Kosten von 104 Milliarden US-Dollar zwischen 2020 und 2024 im Vergleich zu 19 Milliarden US-Dollar zwischen 2015 und 2019. Die Kosteneffizienz von Biosimilars macht sie verfügbar und fördert das globale Marktwachstum.
Das Wachstum der Arzneimittelproduktion treibt die Expansion des Marktes für biosimilare monoklonale Antikörper weltweit stark voran. Zudem hat die Einführung von Biosimilars die Kosten für Biologika sowohl in den USA als auch weltweit effektiv gesenkt. Auf dieser Grundlage wurde in 57 Regionen und Ländern eine analytische Studie zur Preisgestaltung von Biologika nach der Aufnahme von Biosimilars durchgeführt und im Juni 2024 von der NLM veröffentlicht. Die Studie ergab eine Senkung des Durchschnittspreises für Trastuzumab um 438 USD, für Infliximab um 112 USD und für Bevacizumab um 110 USD. Darüber hinaus führte die Markteinführung von Biosimilars jedes Jahr zu weiteren Preissenkungen pro Dosis, nämlich 49 USD für Adalimumab, 290 USD für Filgrastim, 21 USD für Infliximab und 189 USD für Trastuzumab.
Schlüssel Biosimilarer monoklonaler Antikörper Markteinblicke Zusammenfassung:
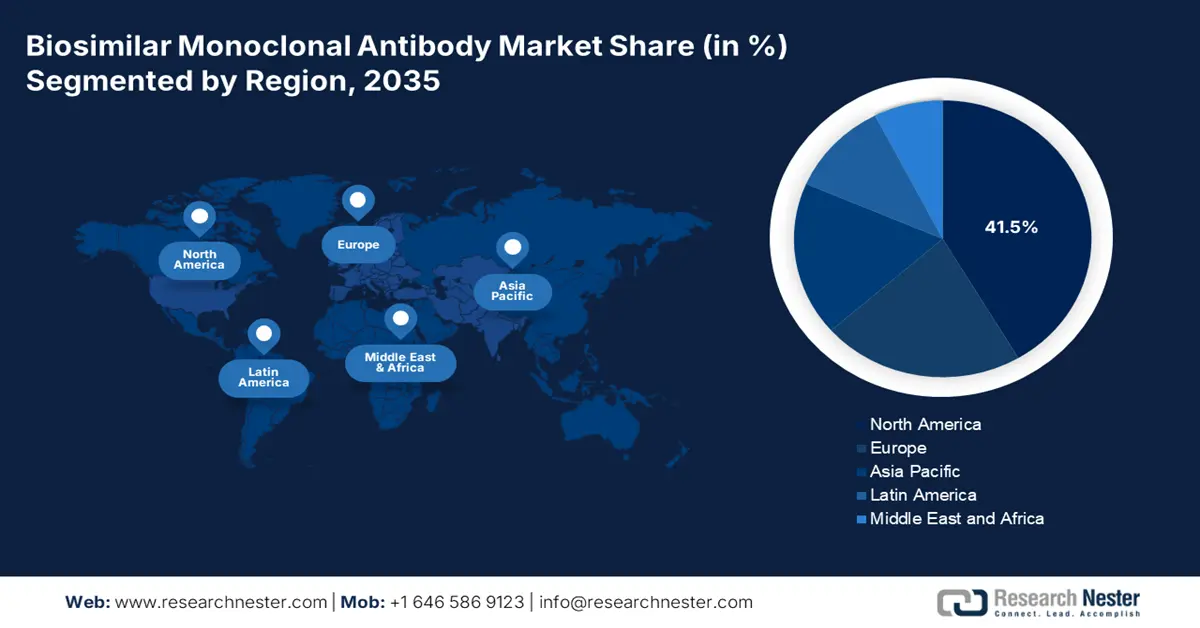
Regionale Highlights:
- Der nordamerikanische Markt für biosimilare monoklonale Antikörper wird bis 2035 einen Marktanteil von 41,50 % erreichen. Die hohe Präsenz von Gesundheitseinrichtungen ermöglicht eine Marktexpansion zur Versorgung der Patienten.
Segmenteinblicke:
- Das Onkologie-Segment im Markt für biosimilare monoklonale Antikörper wird voraussichtlich bis 2035 einen Marktanteil von 50,80 % erreichen. Der Einsatz monoklonaler Antikörper in der Krebstherapie verbessert den Zugang der Patienten zu Behandlungen.
- Das Infliximab-Segment im Markt für biosimilare monoklonale Antikörper wird voraussichtlich bis 2035 einen Marktanteil von 38,60 % erreichen. Der Marktanteil wird durch die breite Anwendung in der Behandlung von Autoimmunerkrankungen und die hohen klinischen Remissionsraten getrieben.
Wichtige Wachstumstrends:
- Patientenabbruch
- Einführung neuer Behandlungen
Wichtige Herausforderungen:
- Voraussetzungen für klinische Studien
- Strenge regulatorische Vorgaben
Hauptakteure: Pfizer Inc., Amgen Inc., Sandoz International GmbH (Novartis), Celltrion, Inc., Samsung Bioepis Co., Ltd., Biocon Limited, Mylan N.V. (Viatris), Dr. Reddy’s Laboratories Ltd., Coherus BioSciences, Inc., Shanghai Henlius Biotech, Inc.
Global Biosimilarer monoklonaler Antikörper Markt Prognose und regionaler Ausblick:
Marktgröße und Wachstumsprognosen:
- Marktgröße 2025: 13,99 Milliarden USD
- Marktgröße 2026: 16,87 Milliarden USD
- Prognostizierte Marktgröße: 109,99 Milliarden USD bis 2035
- Wachstumsprognosen: 22,9 % CAGR (2026–2035)
Wichtige regionale Dynamiken:
- Größte Region: Nordamerika (41,5 % Anteil bis 2035)
- Am schnellsten wachsende Region: Asien-Pazifik
- Dominierende Länder: USA, Deutschland, China, Indien, Japan
- Schwellenländer: China, Indien, Brasilien, Mexiko, Südkorea
Last updated on : 18 September, 2025
Wachstumstreiber und Herausforderungen auf dem Markt für biosimilare monoklonale Antikörper:
Wachstumstreiber
- Patientenabbruch: Dies unterstützt Pharmaunternehmen bei der Entwicklung von Biosimilar-Alternativen und schafft lukrative Geschäftsmöglichkeiten für den Markt für biosimilar-monoklonale Antikörper. Dies führt dazu, dass Biosimilar-Hersteller in den Markt eintreten und einen Wettbewerb schaffen, der eine Reihe wesentlicher Vorteile mit sich bringt. Darüber hinaus wurde in einem 2021 von der NLM veröffentlichten Artikel festgestellt, dass die Bereitstellung verständlicher, transparenter und auf die Bedürfnisse der Patienten zugeschnittener Informationen, unterstützt durch audiovisuelles Material, eine geeignete Strategie ist, um Patienten auf die Verfügbarkeit von Biosimilars aufmerksam zu machen und somit die Marktbelebung positiv zu beeinflussen.
- Einführung neuartiger Behandlungen: Diese therapeutische Lösung hat sich als wirksamer als herkömmliche Behandlungsoptionen erwiesen, was den Markt für biosimilare monoklonale Antikörper belebt. So birgt beispielsweise die Verwendung von Daratumumab, einem monoklonalen Antikörper, zur Behandlung des multiplen Myeloms ein um 43 % geringeres Risiko für Krankheitsverlauf oder Tod, wie das Memorial Sloan Kettering Cancer Center im Februar 2025 feststellte. Dadurch sorgt diese neuartige Behandlung dafür, dass mehr Patienten eine Transplantation erhalten – ein komplexes Verfahren, das einen langen Krankenhausaufenthalt erfordert – und das Marktwachstum international positiv fördert.
Herausforderungen
- Voraussetzungen für klinische Studien: Die Grundlagen klinischer Studien stellen ein großes Hindernis für die Expansion des Marktes für biosimilare monoklonale Antikörper dar. Die Behörden schreiben anspruchsvolle klinische Studien für die Entwicklung von Biosimilars vor, um deren Wirksamkeit und Sicherheit zu bestätigen. Diese Studien erfordern einen erheblichen Ressourcen-, Zeit- und Finanzaufwand. Die steigenden Anforderungen an klinische Studien übersteigen nicht nur den Zeitrahmen für die Produktentwicklung, sondern stellen auch eine finanzielle Belastung dar, die potenzielle Hersteller vom Markteintritt abhalten könnte.
- Strenge regulatorische Vorgaben: Kritische Vorschriften erschweren die Patientenrekrutierung und führen zu verzögerten Zulassungen, einem hemmenden Faktor für den Markt für biosimilare monoklonale Antikörper. Darüber hinaus erhöht der Bedarf an umfangreichen Vergleichsstudien den Zeit- und Kostenaufwand für die Zulassung der neuesten Biosimilars. Obwohl sie kostengünstigere Alternativen zur biologischen Referenz darstellen, ist der Entwicklungsprozess nach wie vor überteuert. Der Ersatz einer biologischen Referenz durch ein Biosimilar ohne medizinische Intervention hemmt zudem das globale Marktwachstum.
Marktgröße und Prognose für biosimilare monoklonale Antikörper:
| Berichtsattribut | Einzelheiten |
|---|---|
|
Basisjahr |
2025 |
|
Prognosezeitraum |
2026–2035 |
|
CAGR |
22,9 % |
|
Marktgröße im Basisjahr (2025) |
13,99 Milliarden US-Dollar |
|
Prognostizierte Marktgröße im Jahr 2035 |
109,99 Milliarden US-Dollar |
|
Regionaler Geltungsbereich |
|
Marktsegmentierung für biosimilare monoklonale Antikörper:
Anzeige
Im Markt für biosimilare monoklonale Antikörper wird das Onkologiesegment bis Ende 2035 voraussichtlich einen Umsatzanteil von über 50,8 % ausmachen. Der Einsatz monoklonaler Antikörper in der Krebstherapie ist der Hauptgrund für das Wachstum dieses Segments. Laut WHO-Bericht vom Februar 2025 forderte Krebs im Jahr 2020 10 Millionen Todesopfer, und krebsbedingte Infektionen wie Hepatitis und das humane Papillomavirus (HPV) sind für etwa 30 % der Krebsfälle in Ländern mit niedrigem und unterem mittlerem Einkommen verantwortlich. Der Einsatz von Biosimilars zur Eindämmung des Krebsaufkommens führte jedoch zu einem Anstieg der Patientenzahl mit Zugang zu Krebsbehandlungen und -medikamenten um 44 %, wie es im NLM-Artikel vom Dezember 2022 heißt.
Typ
Bis 2035 wird das Infliximab-Segment voraussichtlich den Marktanteil biosimilarer monoklonaler Antikörper mit einem Marktanteil von über 38,6 % dominieren. Infliximab ist ein weit verbreiteter monoklonaler Antikörper zur Behandlung zahlreicher Autoimmunerkrankungen und nimmt damit einen bedeutenden Anteil am Gesamtmarkt ein. Laut einer im September 2021 im Sage Journals veröffentlichten klinischen Studie lag die gepoolte klinische Remissionsrate bei erneuter Infliximab-Behandlung bei Patienten mit entzündlichen Darmerkrankungen (IBD) bei 85 %. Darüber hinaus konnte bei 87 % der Patienten mit Morbus Crohn eine Wiedereinführung von Infliximab erreicht werden, was sich positiv auf das Wachstum des Segments auswirkt.
Unsere eingehende Analyse des globalen Marktes für biosimilare monoklonale Antikörper umfasst die folgenden Segmente:
Anzeige |
|
Typ |
|
Endbenutzer |
|

Vishnu Nair
Leiter - Globale GeschäftsentwicklungPassen Sie diesen Bericht an Ihre Anforderungen an – sprechen Sie mit unserem Berater für individuelle Einblicke und Optionen.
Regionale Analyse des Marktes für biosimilare monoklonale Antikörper:
Markteinblicke Nordamerika
Der nordamerikanische Markt für biosimilare monoklonale Antikörper wird bis 2035 voraussichtlich einen Umsatzanteil von rund 41,5 % ausmachen. Laut dem Bericht der American Hospital Association vom Januar 2025 umfasst die Region 6.093 Gesundheitsinfrastrukturen, darunter 5.112 Gemeindekrankenhäuser, 207 Bundeszentren und 654 nicht-bundesstaatliche psychiatrische Krankenhäuser. Hinzu kommen 1.796 ländliche Gemeindekrankenhäuser, 3.316 städtische Krankenhäuser und 3.525 Gemeindekrankenhäuser im Verbund. Angesichts der großen Präsenz von Gesundheitseinrichtungen in der Region ergeben sich für den Markt daher zahlreiche Möglichkeiten, zu expandieren und Patienten bei der Überwindung von Krankheiten zu unterstützen.
Der US- Markt für biosimilare monoklonale Antikörper gewinnt aufgrund der Verfügbarkeit von Biosimilars zur Behandlung seltener Krankheiten an Bedeutung. Laut einem NLM-Artikel vom Februar 2020 wurden Rituximab , Trastuzumab und Bevacizumab aufgrund ihrer Wirksamkeit im Land zugelassen. Rituximab hilft bei Non-Hodgkin-Lymphomen und chronischer lymphatischer Leukämie; Trastuzumab bei Magen- und Brustkrebs; Bevacizumab bei Eierstock-, Gebärmutterhals-, Nieren-, Dickdarm-, Lungen- und Brustkrebs. Darüber hinaus hat die US-amerikanische FDA im Mai 2024 Jubbonti-Injektion als kompatibles Biosimilar zum in den USA zugelassenen Prolia und Wyost-Injektion als identisches Biosimilar zum in den USA zugelassenen Xgeva zugelassen und so zur Marktexpansion beigetragen.
Der Markt für biosimilare monoklonale Antikörper in Kanada verzeichnet ein deutliches Wachstum. Grund dafür ist die große Menge an Biosimilars, die im Land eingeführt werden. Dies erfordert die Entwicklung von Richtlinien und Strategien für ein effektives Management. Laut dem Health Canada-Bericht vom Januar 2025 sind die Benennung biologischer Arzneimittel, internationale Abkommen, Produktmonografien und die Einbindung von Interessengruppen einige der leitlinienbasierten Dokumente, die für die allgemeine Verabreichung von Biosimilars im Land erforderlich sind. All dies unterstützt Hersteller bei der legalen Herstellung von Biosimilars und fördert so das Marktwachstum.
Einblicke in den APAC-Markt
Der Markt für biosimilare monoklonale Antikörper in der Region Asien-Pazifik ist die am schnellsten wachsende Region und wird im Prognosezeitraum voraussichtlich ein lukratives Wachstum verzeichnen. Faktoren wie die hohe Bevölkerungszahl, steigende Gesundheitsausgaben und kostengünstige Therapielösungen treiben das Marktwachstum in der Region voran. Laut einem Bericht der Weltbankgruppe vom April 2024 betrugen die Gesundheitsausgaben gemessen am Bruttoinlandsprodukt im Geschäftsjahr 2021 beispielsweise 6,76 %. Dies macht die Verfügbarkeit und den Kauf von Biosimilars für Patienten in der Region erschwinglicher, was sich positiv auf das Marktwachstum auswirkt.
Der Markt für biosimilare monoklonale Antikörper in Indien erwartet ein starkes Wachstum, da regionale Organisationen die Verantwortung übernommen haben, durch intensive Forschung und Entwicklung die neuesten Biosimilars auf den Markt zu bringen. So brachte Enzene Biosciences im November 2023 Ranibizumab auf den Markt, ein Biosimilar zum innovativen Produkt Lucentis, das in Indien unter dem Markennamen Accentrix vertrieben wird. Es handelt sich um ein rekombinantes Produkt, das zur Therapie der neovaskulären altersbedingten Makuladegeneration (AMD) eingesetzt wird. Dieses Biosimilar ist das siebte Biosimilar des Unternehmens, das die Behandlungskosten für Tausende von Patienten im Land deutlich senken und so den Markt effektiv vorantreiben kann.
Der Markt für biosimilare monoklonale Antikörper in China gewinnt aufgrund intensiver Experimente und Expansion sowie politischer Unterstützung an Bedeutung. Laut dem Bericht der Generics and Biosimilars Initiative vom Februar 2023 haben sich diese Antikörper als zentrale Therapien zur Behandlung von Autoimmunerkrankungen erwiesen, da sie kostengünstig und im Land leicht erhältlich sind. Darüber hinaus verfügt China über eine große Anzahl von Biosimilars, darunter Bevacizumab und Adalimumab, die auf dem regionalen Markt leicht verfügbar sind und eine positive Entwicklung verzeichnen.
F&E-Projekte für beliebte Biosimilars in China
Biosimilar-Medikamente | Präklinisch | IND | Phase I | Phase II | Phase III | Geheimhaltungsvereinbarung | Gestartet | Gesamt |
Actemra | 1 | 2 | 4 | 7 | ||||
Cosentyx | 1 | 1 | ||||||
Darzalex | 1 | 1 | ||||||
Erbitux | 2 | 2 | 2 | 4 | 10 | |||
Herceptin | 2 | 2 | 6 | 1 | 11 | |||
Lemtrada | 1 | 1 | 2 | |||||
MabThera | 3 | 1 | 6 | 2 | 12 |
Quelle: Generika- und Biosimilars-Initiative Februar 2023
Marktteilnehmer für biosimilare monoklonale Antikörper:
- Roche
- Unternehmensübersicht
- Geschäftsstrategie
- Wichtige Produktangebote
- Finanzielle Leistung
- Wichtige Leistungsindikatoren
- Risikoanalyse
- Jüngste Entwicklung
- Regionale Präsenz
- SWOT-Analyse
- Novartis
- Pfizer
- Samsung Bioepis
- Amgen
- Mylan
- Teva Pharmaceutical Industries
- Biogen
- Celltrion
- Fresenius Kabi
- Sandoz
- Boehringer Ingelheim
- Merck
- Amneal Pharmaceuticals
- Biocon Biologics Ltd
- Celltrion
- Enzene Biosciences
Unternehmen, die den Markt für biosimilare monoklonale Antikörper dominieren, gewinnen aufgrund ihrer klinischen Wirksamkeit bei der Behandlung verschiedener Krankheiten, von denen Patienten weltweit betroffen sind, schnell an Bedeutung. Darüber hinaus spielen auch die zuständigen Behörden eine wichtige Rolle bei der Zulassung dieser Biosimilars. So erhielten beispielsweise Fresenius Kabi und Formycon im September 2024 von der US-amerikanischen FDA die Zulassung für das Biosimilar Otulfi (Ustekinumab-aauz). Dieses erwies sich als nützlich für die Behandlung von Morbus Crohn, Colitis ulcerosa, mittelschwerer bis schwerer Plaque-Psoriasis und aktiver Psoriasis-Arthritis und bietet somit optimistische Aussichten für ein globales Marktwachstum.
Hier ist die Liste einiger Schlüsselspieler:
Neueste Entwicklungen
- Im Februar 2025 meldete Celltrion der Europäischen Kommission (EK) die Zulassung von Biosimilars – Eydenzelt, ein Biosimilar zu Eylea zur Behandlung mehrerer Netzhauterkrankungen, sowie Stoboclo und Osenvelt, Biosimilars auf Basis von Prolia und Xgeva, die für alle Indikationen der Referenzprodukte verwendet werden.
- Im Dezember 2024 gab Biocon Biologics Ltd die Zulassung der US-amerikanischen Food and Drug Administration (FDA) für YESINTEK bekannt, ein Biosimilar zum Referenzprodukt Stelara. Dieser monoklonale Antikörper ist zur Behandlung von Morbus Crohn, Colitis ulcerosa, Plaque-Psoriasis und Psoriasis-Arthritis zugelassen.
- Report ID: 7276
- Published Date: Sep 18, 2025
- Report Format: PDF, PPT
- Entdecken Sie eine Vorschau auf die wichtigsten Markttrends und Erkenntnisse
- Prüfen Sie Beispiel-Datentabellen und Segmentaufgliederungen
- Erleben Sie die Qualität unserer visuellen Datendarstellungen
- Bewerten Sie unsere Berichtsstruktur und Forschungsmethodik
- Werfen Sie einen Blick auf die Analyse der Wettbewerbslandschaft
- Verstehen Sie, wie regionale Prognosen dargestellt werden
- Beurteilen Sie die Tiefe der Unternehmensprofile und Benchmarking
- Sehen Sie voraus, wie umsetzbare Erkenntnisse Ihre Strategie unterstützen können
Entdecken Sie reale Daten und Analysen
Häufig gestellte Fragen (FAQ)
Biosimilarer monoklonaler Antikörper Umfang des Marktberichts
Die kostenlose Stichprobe umfasst aktuelle und historische Marktgrößen, Wachstumstrends, regionale Diagramme und Tabellen, Unternehmensprofile, segmentweise Prognosen und mehr.
Kontaktieren Sie unseren Experten
Urheberrecht © 2026 Research Nester. Alle Rechte vorbehalten.




