Perspectivas del mercado de anticuerpos monoclonales biosimilares:
El mercado de anticuerpos monoclonales biosimilares se valoró en 13 990 millones de dólares en 2025 y se prevé que supere los 109 990 millones de dólares para 2035, registrando una tasa de crecimiento anual compuesta (TCAC) superior al 22,9 % durante el período de pronóstico, es decir, entre 2026 y 2035. Para 2026, el tamaño de la industria de anticuerpos monoclonales biosimilares se estima en 16 870 millones de dólares.

El mercado de la industria farmacéutica está en constante evolución para la fabricación y producción de fármacos basados en anticuerpos como soluciones terapéuticas. Además, la demanda de terapias biológicas económicamente viables y los costos de la atención médica están convirtiendo a los biosimilares en una alternativa a los costosos medicamentos convencionales. Según un artículo publicado en enero de 2024 por la NLM, el ahorro en costos de los biosimilares, especialmente en EE. UU., aumentó, con un costo previsto de 104 000 millones de dólares entre 2020 y 2024, en comparación con los 19 000 millones de dólares entre 2015 y 2019. Por lo tanto, la rentabilidad de los biosimilares los hace accesibles, lo que impulsa el crecimiento del mercado a nivel mundial.
El crecimiento de los medicamentos está impulsando considerablemente la expansión del mercado mundial de anticuerpos monoclonales biosimilares. Además, la entrada de biosimilares ha reducido eficazmente el coste de los productos biológicos, tanto en EE. UU. como a nivel mundial. Con base en esto, se realizó un estudio analítico en 57 regiones y países sobre el precio de los biológicos para el pagador tras la inclusión de biosimilares, publicado en junio de 2024 por la NLM. El estudio indicó una reducción del precio medio del trastuzumab en 438 USD, el infliximab en 112 USD y el bevacizumab en 110 USD. Además, el efecto de la entrada de biosimilares en el mercado condujo a nuevas reducciones en el precio por dosis cada año, representando 49 USD para adalimumab, 290 USD para filgrastim, 21 USD para infliximab y 189 USD para trastuzumab.
Clave Anticuerpo monoclonal biosimilar Resumen de Perspectivas del Mercado:
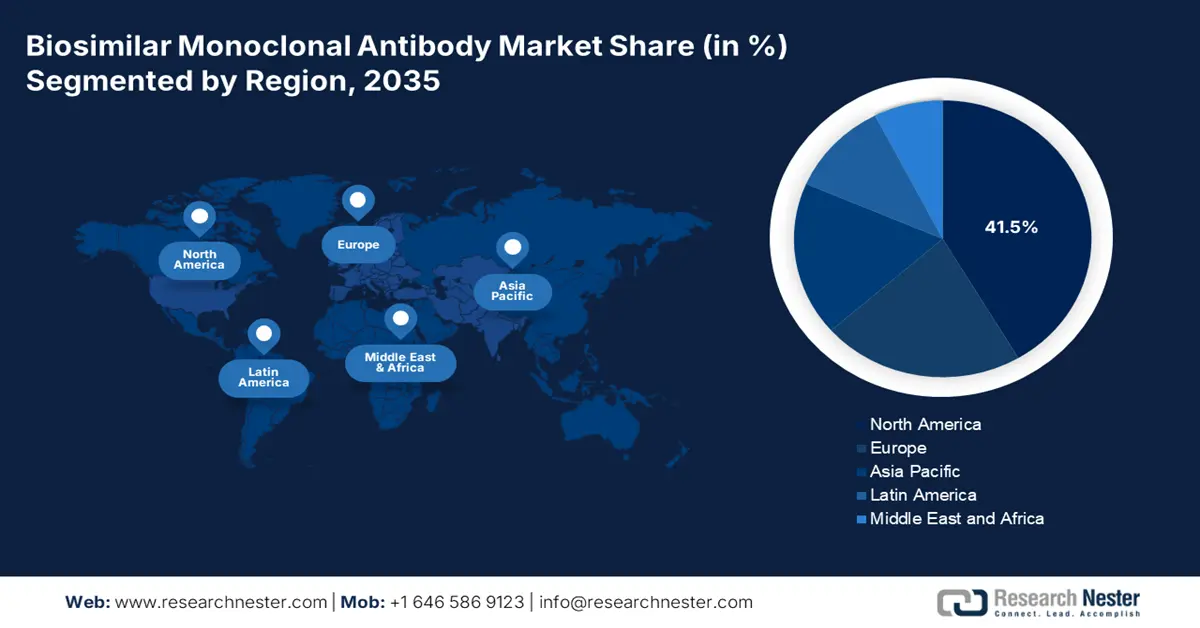
Aspectos destacados regionales:
- El mercado de anticuerpos monoclonales biosimilares de América del Norte representará el 41,50 % de la cuota de mercado para 2035, impulsado por una amplia presencia de centros de salud, lo que permitirá la expansión del mercado para atender a los pacientes.
Perspectivas del segmento:
- Se proyecta que el segmento de oncología en el mercado de anticuerpos monoclonales biosimilares alcance una participación del 50,80 % para 2035, impulsado por el uso de anticuerpos monoclonales para la terapia contra el cáncer, lo que aumenta el acceso de los pacientes a los tratamientos.
- Se proyecta que el segmento de infliximab en el mercado de anticuerpos monoclonales biosimilares alcance una participación del 38,60 % para 2035, impulsado por su amplio uso en el tratamiento de enfermedades autoinmunes y sus altas tasas de remisión clínica.
Tendencias clave de crecimiento:
- Interrupción de la atención por parte de pacientes
- Adopción de nuevos tratamientos
Principales desafíos:
- Requisitos para los ensayos clínicos
- Políticas regulatorias estrictas
Principales actores:Pfizer Inc., Amgen Inc., Sandoz International GmbH (Novartis), Celltrion, Inc., Samsung Bioepis Co., Ltd., Biocon Limited, Mylan N.V. (Viatris), Dr. Reddy's Laboratories Ltd., Coherus BioSciences, Inc., Shanghai Henlius Biotech, Inc.
Global Anticuerpo monoclonal biosimilar Mercado Pronóstico y perspectiva regional:
Proyecciones de tamaño y crecimiento del mercado:
- Tamaño del mercado en 2025: USD 13.990 millones
- Tamaño del mercado en 2026: USD 16.870 millones
- Tamaño proyectado del mercado: USD 109.99 mil millones para 2035
- Previsiones de crecimiento: 22,9 % CAGR (2026-2035)
Dinámicas regionales clave:
- Región más grande: América del Norte (participación del 41,5 % para 2035)
- Región de más rápido crecimiento: Asia Pacífico
- Países dominantes: Estados Unidos, Alemania, China, India, Japón
- Países emergentes: China, India, Brasil, México, Corea del Sur
Last updated on : 18 September, 2025
Impulsores y desafíos del crecimiento del mercado de anticuerpos monoclonales biosimilares:
Factores impulsores del crecimiento
- Finalización de la relación con el paciente: Esto facilita el desarrollo de alternativas biosimilares por parte de las organizaciones farmacéuticas, lo que crea una oportunidad de negocio lucrativa para impulsar el mercado de anticuerpos monoclonales biosimilares. Esto impulsa la entrada de fabricantes de biosimilares y la competencia, lo que genera diversas ventajas esenciales. Además, un artículo publicado por la NLM en 2021 afirmó que proporcionar información comprensible de forma transparente, adaptada a las necesidades de los pacientes y con el apoyo de material audiovisual, es una estrategia adecuada para que los pacientes conozcan la disponibilidad de biosimilares, lo que repercute positivamente en el desarrollo del mercado.
- Adopción de un tratamiento novedoso: Esta solución terapéutica ha demostrado ser más eficaz que las opciones de tratamiento convencionales, lo que está impulsando el mercado de anticuerpos monoclonales biosimilares. Por ejemplo, el uso de daratumumab, un anticuerpo monoclonal, para el tratamiento del mieloma múltiple reduce en un 43 % el riesgo de progresión de la enfermedad o muerte, según lo declarado por el Memorial Sloan Kettering Cancer Center en febrero de 2025. Por lo tanto, este tipo de tratamiento novedoso garantiza un aumento en el número de pacientes que se someten a un trasplante, un procedimiento complejo que requiere una larga estancia hospitalaria, lo que impulsa positivamente el crecimiento del mercado a nivel internacional.
Desafíos
- Requisitos previos para los ensayos clínicos: Los fundamentos de los ensayos clínicos constituyen un obstáculo importante para la expansión del mercado de anticuerpos monoclonales biosimilares. Las instituciones reguladoras exigen ensayos clínicos rigurosos para el desarrollo de biosimilares con el fin de confirmar la eficacia y seguridad del producto. Estos ensayos requieren una considerable asignación de recursos, tiempo e inversión financiera. Además, el aumento de los requisitos de los ensayos clínicos no solo prolonga el plazo de desarrollo del producto, sino que también supone una carga financiera que podría disuadir a los posibles fabricantes de entrar en el mercado.
- Políticas regulatorias estrictas: Regulaciones críticas dificultan el reclutamiento de pacientes, lo que resulta en un retraso en el ingreso, un factor limitante para el mercado de anticuerpos monoclonales biosimilares. Además, la necesidad de estudios comparativos exhaustivos incrementa el tiempo y el costo de aprobación de los biosimilares más recientes. Si bien son alternativas más económicas que el medicamento de referencia biológico, el proceso de desarrollo sigue siendo excesivamente costoso. Además, la sustitución de un medicamento de referencia biológico por un biosimilar sin intervención médica también obstaculiza el crecimiento del mercado a nivel mundial.
Tamaño y pronóstico del mercado de anticuerpos monoclonales biosimilares:
| Atributo del informe | Detalles |
|---|---|
|
Año base |
2025 |
|
Período de pronóstico |
2026-2035 |
|
Tasa de crecimiento anual compuesta (TCAC) |
22,9% |
|
Tamaño del mercado del año base (2025) |
13.990 millones de dólares |
|
Tamaño del mercado según pronóstico anual (2035) |
USD 109.99 mil millones |
|
Alcance regional |
|
Segmentación del mercado de anticuerpos monoclonales biosimilares:
Indicación
En el mercado de anticuerpos monoclonales biosimilares, se prevé que el segmento oncológico represente más del 50,8% de los ingresos para finales de 2035. El uso de anticuerpos monoclonales para el tratamiento del cáncer es la principal razón del crecimiento de este segmento. Según el informe de la OMS de febrero de 2025, el cáncer causó 10 millones de muertes en 2020, y las infecciones cancerosas, como la hepatitis y el virus del papiloma humano (VPH), son responsables de aproximadamente el 30% de los casos de cáncer en países de ingresos bajos y medianos-bajos. Sin embargo, el uso de biosimilares para controlar la incidencia del cáncer resultó en un aumento del 44% en el número de pacientes con acceso a tratamientos y medicamentos contra el cáncer, como se indica en el artículo de la NLM de diciembre de 2022.
Tipo
Para 2035, se prevé que el segmento de infliximab domine la cuota de mercado de anticuerpos monoclonales biosimilares, con una cuota de mercado superior al 38,6 %. Infliximab es un anticuerpo monoclonal ampliamente utilizado para el tratamiento de numerosas enfermedades autoinmunes, lo que lo convierte en una parte significativa del mercado global. Según un estudio clínico publicado por Sage Journals en septiembre de 2021, la tasa de remisión clínica combinada del retratamiento con infliximab en pacientes con enfermedad inflamatoria intestinal (EII) fue del 85 %. Además, se logró la reintroducción de infliximab en el 87 % de los pacientes con enfermedad de Crohn, lo que impactó positivamente en el crecimiento del segmento.
Nuestro análisis en profundidad del mercado global de anticuerpos monoclonales biosimilares incluye los siguientes segmentos:
Indicación |
|
Tipo |
|
Usuario final |
|

Vishnu Nair
Jefe de Desarrollo Comercial GlobalPersonalice este informe según sus necesidades: conéctese con nuestro consultor para obtener información y opciones personalizadas.
Análisis regional del mercado de anticuerpos monoclonales biosimilares:
Perspectivas del mercado de América del Norte
Se espera que el mercado norteamericano de anticuerpos monoclonales biosimilares represente una participación en los ingresos de aproximadamente el 41,5 % para 2035. Según el informe de la Asociación Americana de Hospitales de enero de 2025, la región comprende 6093 infraestructuras sanitarias, incluyendo 5112 hospitales comunitarios, 207 centros del gobierno federal y 654 hospitales psiquiátricos no federales. Además, el sistema cuenta con 1796 hospitales comunitarios rurales, 3316 hospitales urbanos y 3525 hospitales comunitarios. Por lo tanto, con la amplia presencia de centros de salud en la región, existe una amplia oportunidad para que el mercado se expanda y atienda a los pacientes para que superen las enfermedades.
El mercado estadounidense de anticuerpos monoclonales biosimilares ha estado ganando terreno debido a la presencia de biosimilares para el tratamiento de enfermedades raras. Según el artículo de la NLM de febrero de 2020, rituximab , trastuzumab y bevacizumab han sido aprobados en el país para su uso efectivo. Rituximab ayuda al linfoma no Hodgkin y la leucemia linfocítica crónica; trastuzumab atiende al cáncer de estómago y de mama; bevacizumab es útil para deshacerse del cáncer de ovario, cuello uterino, riñón, colorrectal, pulmón y mama. Además, la FDA de EE. UU. en mayo de 2024 aprobó la inyección de jubbonti como un biosimilar compatible con Prolia con licencia en EE. UU., y la inyección de Wyost como un biosimilar idéntico a Xgeva con licencia en EE. UU., contribuyendo así a la expansión del mercado.
El mercado de anticuerpos monoclonales biosimilares en Canadá está experimentando un crecimiento significativo debido a la gran cantidad de biosimilares que se están introduciendo en el país, lo que requiere la evolución de políticas y estrategias para una gestión eficaz. Según el informe de Health Canada de enero de 2025, la denominación de medicamentos biológicos, los acuerdos internacionales, las monografías de productos y la participación de las partes interesadas son algunos documentos orientativos necesarios para la administración general de biosimilares en el país. Todo esto ayuda a los fabricantes a seguir el proceso legal de producción de biosimilares, impulsando así el crecimiento del mercado de forma eficiente.
Perspectivas del mercado de Asia-Pacífico
El mercado de anticuerpos monoclonales biosimilares en APAC es la región de mayor crecimiento y se prevé un crecimiento lucrativo durante el período previsto. Factores como el crecimiento demográfico, el aumento del gasto sanitario y las soluciones terapéuticas rentables impulsan la expansión del mercado en la región. Por ejemplo, según el informe del Grupo Banco Mundial de abril de 2024, el gasto sanitario más reciente, basado en el producto interior bruto (PIB), representó el 6,76 % en el ejercicio 2021. Por lo tanto, esto facilita la disponibilidad y la adquisición de biosimilares para los pacientes de la región, lo que repercute positivamente en el crecimiento y la expansión del mercado.
Se espera un crecimiento sustancial del mercado de anticuerpos monoclonales biosimilares en India , ya que las organizaciones regionales han asumido la responsabilidad de presentar los biosimilares más recientes mediante una exhaustiva investigación y desarrollo. Por ejemplo, en noviembre de 2023, Enzene Biosciences lanzó Ranibizumab, un biosimilar del innovador producto Lucentis, comercializado bajo la marca Accentrix en India. Se trata de un recombinante que se utiliza como terapia para la degeneración macular neovascular relacionada con la edad (DMRE). Además, este biosimilar es el séptimo de la organización y puede reducir significativamente los costos de tratamiento para miles de pacientes del país, impulsando así el mercado de forma eficaz.
El mercado de anticuerpos monoclonales biosimilares en China está ganando terreno gracias a la experimentación y expansión extremas, junto con el apoyo político. Según el informe de la Iniciativa de Genéricos y Biosimilares de febrero de 2023, estos anticuerpos se convirtieron en terapias clave para el tratamiento de enfermedades autoinmunes, gracias a su bajo costo y fácil acceso en el país. Además, China cuenta con una gran cantidad de biosimilares, y de ellos, el bevacizumab y el adalimumab son productos de fácil acceso en el mercado regional, lo que impulsa un desarrollo positivo.
Proyectos de I+D de biosimilares populares en China
Medicamentos biosimilares | Preclínico | INDIANA | Fase I | Fase II | Fase III | Acuerdo de confidencialidad | Lanzado | Total |
Actemra | 1 | 2 | 4 | 7 | ||||
Cosentyx | 1 | 1 | ||||||
Darzalex | 1 | 1 | ||||||
Erbitux | 2 | 2 | 2 | 4 | 10 | |||
Herceptina | 2 | 2 | 6 | 1 | 11 | |||
Lemtrada | 1 | 1 | 2 | |||||
MabThera | 3 | 1 | 6 | 2 | 12 |
Fuente: Iniciativa de Genéricos y Biosimilares, febrero de 2023
Actores del mercado de anticuerpos monoclonales biosimilares:
- Roche
- Descripción general de la empresa
- Estrategia empresarial
- Ofertas de productos clave
- Desempeño financiero
- Indicadores clave de rendimiento
- Análisis de riesgos
- Desarrollo reciente
- Presencia regional
- Análisis FODA
- Novartis
- Pfizer
- Samsung Bioepis
- Amgen
- Mylan
- Industrias farmacéuticas Teva
- Biogen
- Celltrion
- Fresenius Kabi
- Sandoz
- Boehringer Ingelheim
- Merck
- Productos farmacéuticos Amneal
- Biocon Biologics Ltd
- Celltrion
- Enzene Biosciences
Las empresas que dominan el mercado de anticuerpos monoclonales biosimilares están ganando visibilidad rápidamente gracias a sus resultados clínicos, ideales para el tratamiento de diversas enfermedades que afectan a pacientes a nivel internacional. Además, los organismos administrativos también desempeñan un papel esencial en la aprobación de estos biosimilares. Por ejemplo, en septiembre de 2024, Fresenius Kabi y Formycon recibieron la aprobación de la FDA estadounidense para el biosimilar Otulfi (ustekinumab-aauz). Este demostró ser útil para el tratamiento de la enfermedad de Crohn, la colitis ulcerosa, la psoriasis en placas de moderada a grave y la artritis psoriásica activa, lo que ofrece una perspectiva optimista para la expansión global del mercado.
Aquí está la lista de algunos jugadores clave:
Desarrollos Recientes
- En febrero de 2025, Celltrion notificó a la Comisión Europea (CE) la aprobación de los biosimilares Eydenzelt, un biosimilar de Eylea para tratar múltiples trastornos de la retina, y Stoboclo y Osenvelt, biosimilares que hacen referencia a Prolia y Xgeva utilizados para todas las indicaciones de los productos de referencia.
- En diciembre de 2024, Biocon Biologics Ltd. declaró la aprobación de la Administración de Alimentos y Medicamentos de EE. UU. (FDA) para YESINTEK, un biosimilar del producto de referencia Stelara. Este anticuerpo monoclonal está aprobado para el tratamiento de la enfermedad de Crohn, la colitis ulcerosa, la psoriasis en placas y la artritis psoriásica.
- Report ID: 7276
- Published Date: Sep 18, 2025
- Report Format: PDF, PPT
- Explore una vista previa de las principales tendencias e ideas del mercado
- Revise tablas de datos de muestra y desgloses por segmento
- Experimente la calidad de nuestras representaciones visuales de datos
- Evalúe nuestra estructura de informe y metodología de investigación
- Obtenga una vista de la análisis del panorama competitivo
- Comprenda cómo se presentan las previsiones regionales
- Evalúe la profundidad del perfilado de empresas y análisis comparativo
- Vea cómo los insights accionables pueden respaldar su estrategia
Explore datos y análisis reales
Preguntas frecuentes (FAQ)
Anticuerpo monoclonal biosimilar Alcance del informe de mercado
La muestra gratuita incluye el tamaño del mercado actual e histórico, tendencias de crecimiento, gráficos y tablas regionales, perfiles de empresas, previsiones por segmento y más.
Conéctate con nuestro experto
Derechos de autor © 2026 Research Nester. Todos los derechos reservados.




