Prospettive di mercato del software per l'abbinamento delle sperimentazioni cliniche:
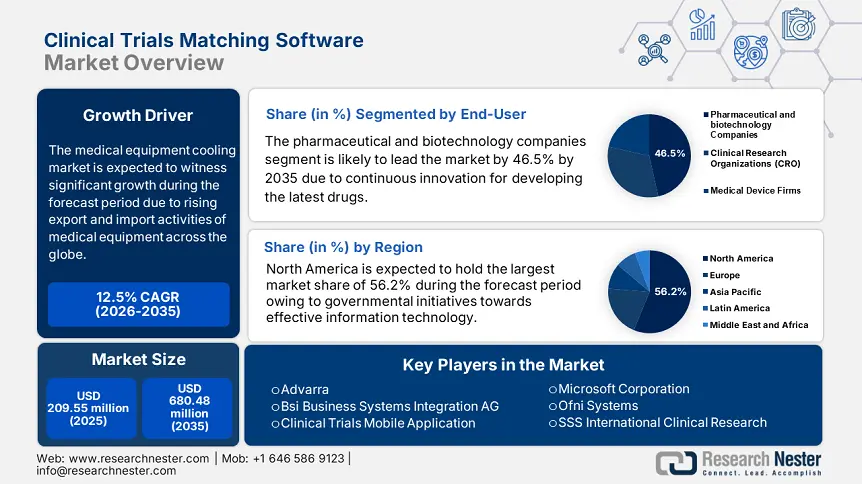
Il mercato dei software per l'abbinamento di studi clinici è stato stimato a 209,55 milioni di dollari nel 2025 e si prevede che raggiungerà i 680,48 milioni di dollari entro il 2035, con un CAGR di circa il 12,5% durante il periodo di previsione, ovvero tra il 2026 e il 2035. Nel 2026, il mercato dei software per l'abbinamento di studi clinici è stimato a 233,12 milioni di dollari.
L'implementazione di strumenti software automatizzati negli studi clinici garantisce un metodo efficiente per la rapida identificazione di pazienti potenzialmente idonei alla ricerca clinica, il che sta fortemente stimolando la crescita del mercato dei software per la gestione degli studi clinici. Secondo un articolo pubblicato da NLM nel febbraio 2023, uno studio clinico si compone di diverse fasi, tra cui la Fase 0, esplorativa, la Fase Ia, la Fase Ib e la Fase Ic, che costituiscono uno studio non terapeutico, la Fase II, la Fase IIa e la Fase IIb, che costituiscono uno studio esplorativo, la Fase III, che costituisce uno studio di conferma terapeutica, e la Fase IV, che costituisce uno studio post-approvazione. Pertanto, la combinazione di tutte queste fasi e l'inclusione di strumenti software innovativi sono sufficientemente efficaci da consentire l'espansione del mercato.
Il mercato dei software per la corrispondenza degli studi clinici è destinato a crescere grazie all'impiego di tecnologie e macchine di elaborazione per valutare la probabilità di studio, semplificare il reclutamento e la gestione dei partecipanti, consentire l'accesso a popolazioni diverse, razionalizzare la raccolta dei dati e semplificarne la gestione. Per questo motivo, l'implementazione di computer e set di strumenti negli studi clinici è estremamente comune, con conseguente aumento della loro domanda. Secondo il rapporto OEC del 2023, il valore del commercio globale di computer ammontava a 323 miliardi di dollari, con la Cina come principale esportatore con 158 miliardi di dollari e gli Stati Uniti come principale importatore con 93,2 miliardi di dollari.
Inoltre, l'utilizzo di set di strumenti negli studi clinici è utile per la gestione efficace delle operazioni, dei dati e della comunicazione durante l'intero ciclo di vita dello studio, favorendo lo sviluppo del mercato del software per la gestione degli studi clinici. Questi strumenti contribuiscono inoltre a facilitare i cambiamenti nella pratica clinica e possono includere strategie per l'implementazione delle linee guida, l'informazione delle policy e la fornitura di materiali di audit di qualità. Secondo il rapporto OEC del 2023, il commercio internazionale di set di strumenti è valutato a 1,29 miliardi di dollari, con la Cina come principale esportatore con 606 milioni di dollari e la Germania come principale importatore con 114 milioni di dollari, con un impatto positivo sulla crescita del mercato.
Confronto tra esportazione/importazione di computer e set di strumenti
Paesi | Computer | Set di strumenti | ||
Esportare | Importare | Esportare | Importare | |
Messico | 29,5 miliardi di dollari | - | - | - |
Taipei | 27,1 miliardi di dollari | - | 158,0 milioni di dollari | - |
Vietnam | 15,9 miliardi di dollari | - | - | - |
Stati Uniti | 15,3 miliardi di dollari | 93,2 miliardi di dollari | 59,6 milioni di dollari | 82,4 milioni di dollari |
Germania | - | 20,4 miliardi di dollari | 147,0 milioni di dollari | 114,0 milioni di dollari |
Hong Kong | - | 15,5 miliardi di dollari | - | - |
Paesi Bassi | - | 14,3 miliardi di dollari | 29,3 milioni di dollari | 68,4 milioni di dollari |
Regno Unito | - | 13,0 miliardi di dollari | - | - |
Russia | - | - | - | 114,0 milioni di dollari |
Francia | - | - | - | 93,7 milioni di dollari |
Fonte: OEC 2023
Chiave Software di abbinamento per studi clinici Riepilogo delle Analisi di Mercato:
Aspetti salienti regionali:
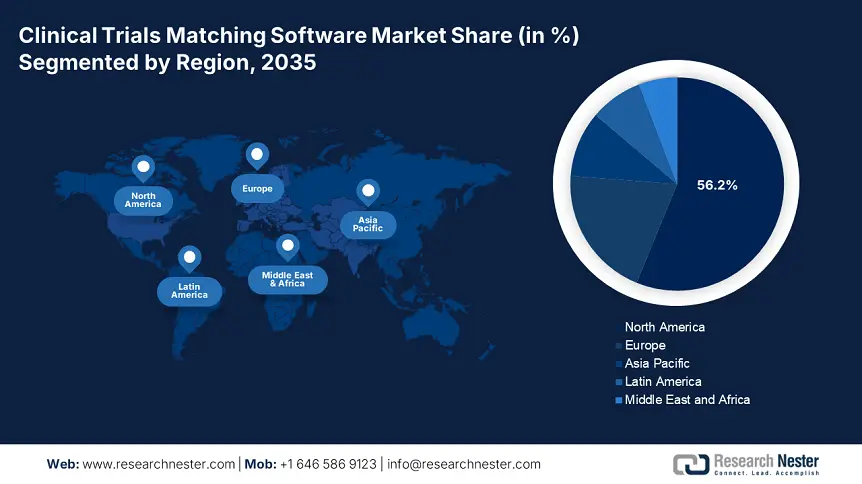
- Il Nord America detiene una quota del 56,20% nel mercato dei software per l'abbinamento degli studi clinici, trainata dall'accettazione dei sistemi di abbinamento degli studi farmacologici, dalle strategie governative e dalle iniziative del NIH, garantendo una forte crescita entro il 2035.
- Si prevede che il mercato dei software per l'abbinamento degli studi clinici nell'area Asia-Pacifico crescerà più rapidamente entro il 2035, grazie alla disponibilità di un gran numero di pazienti e all'aumento dei progetti IT in ambito sanitario.
Approfondimenti sul segmento:
- Si prevede che il segmento delle aziende farmaceutiche e biotecnologiche deterrà una quota di mercato superiore al 46,5% entro il 2035, trainato dall'elevato numero di sperimentazioni farmacologiche necessarie per il lancio del prodotto.
- Si prevede una crescita sostanziale del segmento software dal 2026 al 2035, attribuibile all'aumento dell'utilizzo e dell'adozione di sperimentazioni farmacologiche, all'implementazione di attività di ricerca e sviluppo e ai generosi contributi delle organizzazioni mediche.
Principali trend di crescita:
- Aumento delle attività di sperimentazione clinica
- Digitalizzazione nella ricerca
Principali sfide:
- Software costoso
- Formazione e adattamento insufficienti
- Attori principali: Advarra, Antidote Technologies, Inc., IBM Clinical Development, applicazione mobile per sperimentazioni cliniche.
Globale Software di abbinamento per studi clinici Mercato Previsioni e prospettive regionali:
Dimensioni del mercato e proiezioni di crescita:
- Dimensioni del mercato 2025: 209,55 milioni di USD
- Dimensioni del mercato 2026: 233,12 milioni di USD
- Dimensioni del mercato previste: 680,48 milioni di USD entro il 2035
- Previsioni di crescita: 12,5% CAGR (2026-2035)
Dinamiche regionali chiave:
- Regione più grande: Nord America (quota del 56,2% entro il 2035)
- Regione in più rapida crescita: Asia Pacifico
- Paesi dominanti: Stati Uniti, Germania, Giappone, Regno Unito, Francia
- Paesi emergenti: Cina, India, Brasile, Russia, Messico
Last updated on : 27 August, 2025
Fattori trainanti e sfide della crescita del mercato del software di abbinamento delle sperimentazioni cliniche:
Fattori di crescita
- Aumento delle attività di sperimentazione clinica: si prevede che il mercato del software di abbinamento per le sperimentazioni cliniche aumenterà grazie al miglioramento delle sperimentazioni cliniche a livello internazionale. Secondo il rapporto dell'OMS di dicembre 2024, gli Stati Uniti sono soggetti a un aumento di 186.497 sperimentazioni, seguiti da 135.747 in Cina, 74.031 in India, 65.167 in Giappone, 54.902 in Germania e molti altri. Ciò è dovuto alla crescente diffusione di tecnologie sanitarie avanzate, unita alla crescente domanda di farmaci innovativi con un'efficacia superiore, che amplificano rapidamente lo sviluppo e l'evoluzione del mercato.
- Digitalizzazione nella ricerca: l'integrazione di tecnologie sofisticate come l'acquisizione elettronica dei dati (EDC) e i sistemi di gestione degli studi clinici sta aumentando la domanda di software per la gestione degli studi clinici a livello globale. Secondo un articolo pubblicato da Mayo Clinic Proceedings nell'ottobre 2023, il 94% degli ospedali negli Stati Uniti utilizzava prontamente una cartella clinica elettronica (EHR) per fornire assistenza clinica, e questo rappresentava il 45% della popolazione regionale complessiva che includeva una cartella clinica nell'EHR. L'EHR era stato concepito principalmente come uno strumento per l'assistenza incentrata sul paziente, ma i ricercatori clinici ne hanno sfruttato l'adozione pressoché universale in vari aspetti degli studi.
Sfide
- Software costoso: l'elevato prezzo dei sistemi software di matching sta di fatto ostacolando la crescita del mercato dei software di matching per studi clinici. Alcuni aspetti del software, come l'avvio, il costo per utente, l'impegno contrattuale, i costi per studio, la manutenzione, la formazione, il supporto e l'integrazione del sistema, aumentano cumulativamente il costo complessivo necessario per l'implementazione di soluzioni software di matching per studi clinici. Inoltre, i costi di personalizzazione e configurazione vengono addebitati alle organizzazioni in base a specifici requisiti organizzativi e di ricerca.
- Formazione e adattamento insufficienti: gli operatori sanitari potrebbero non disporre della formazione essenziale per utilizzare in modo efficace gli strumenti avanzati di matching per gli studi clinici, limitandone i probabili benefici. Inoltre, gli studi clinici complessi spesso comprendono molteplici variabili e rigidi criteri di ammissibilità, rendendo problematico per i professionisti fornire soluzioni software per abbinare i pazienti in modo accurato ed efficiente. Ciò crea una lacuna nella conduzione complessiva degli studi clinici che porta a risultati incompleti, limitando così il mercato globale dei software per il matching degli studi clinici.
Dimensioni e previsioni del mercato del software di abbinamento delle sperimentazioni cliniche:
| Attribut du rapport | Détails |
|---|---|
|
Anno base |
2025 |
|
Periodo di previsione |
2026-2035 |
|
CAGR |
12,5% |
|
Dimensione del mercato dell'anno base (2025) |
209,55 milioni di dollari |
|
Dimensione del mercato prevista per l'anno (2035) |
680,48 milioni di dollari |
|
Ambito regionale |
|
Segmentazione del mercato del software di abbinamento delle sperimentazioni cliniche:
Utente finale (aziende farmaceutiche e biotecnologiche, organizzazioni di ricerca clinica (CRO), aziende di dispositivi medici)
Si prevede che il segmento delle aziende farmaceutiche e biotecnologiche raggiungerà una quota di mercato del software pari a oltre il 46,5% entro il 2035. L'evoluzione di questo segmento è attribuibile all'elevato numero di sperimentazioni farmacologiche necessarie per il lancio del prodotto. Ad esempio, secondo il rapporto della FDA statunitense dell'aprile 2024, il CDER ha lanciato con successo un centro per l'innovazione nella sperimentazione clinica (C3T1) per promuovere iniziative rivoluzionarie e fungere da punto centrale per il coordinamento, la condivisione delle conoscenze e la comunicazione con soggetti interni ed esterni. Pertanto, questo sviluppo in collaborazione con la FDA rappresenta un enorme contributo alla crescita del mercato a livello globale.
Componenti ( Software, Servizi )
Si prevede che il segmento software influenzerà il mercato del software per la corrispondenza delle sperimentazioni cliniche a un ritmo considerevole durante il periodo di previsione. Questa crescita è attribuibile all'aumento dell'utilizzo e dell'adozione di sperimentazioni farmacologiche, all'implementazione di attività di ricerca e sviluppo e ai generosi contributi delle organizzazioni mediche per promuovere e condurre sperimentazioni farmacologiche complesse. Ad esempio, come affermato nell'articolo di febbraio 2025 pubblicato da Drug Discovery Today, la probabilità media di un primo tasso di approvazione è del 14,3% per le principali aziende farmaceutiche basate sulla ricerca, con un intervallo compreso tra l'8% e il 23%. Ciò garantisce quindi un tasso di successo complessivo dello sviluppo clinico compreso tra il 7% e il 25%.
La nostra analisi approfondita del mercato globale dei software di abbinamento per le sperimentazioni cliniche include i seguenti segmenti:
Utente finale |
|
Componenti |
|
Modalità di distribuzione |
|

Vishnu Nair
Responsabile dello sviluppo commerciale globalePersonalizza questo rapporto in base alle tue esigenze — contatta il nostro consulente per approfondimenti e opzioni personalizzate.
Analisi regionale del mercato del software di abbinamento delle sperimentazioni cliniche:
Analisi del mercato del Nord America
Entro la fine del 2035, il mercato nordamericano dei software per l'abbinamento degli studi clinici dovrebbe dominare circa il 56,2% del fatturato. Fattori quali l'accettazione dei sistemi di abbinamento degli studi farmacologici da parte di organizzazioni biotecnologiche e farmaceutiche, strategie governative e l'adozione di software per l'abbinamento dei pazienti e degli studi clinici stanno fortemente rafforzando l'espansione del mercato nella regione. Ad esempio, nel settembre 2024 il National Institute of Health (NIH) ha lanciato una serie di iniziative, tra cui il programma Basic Experimental Studies Involving Humans (BESH), la revisione basata sugli studi clinici, i finanziamenti e le pratiche, i moduli informativi sugli esseri umani, i modelli di protocollo, nonché la formazione e le risorse adatte allo sviluppo del mercato.
Il mercato statunitense dei software per la corrispondenza degli studi clinici sta guadagnando terreno grazie all'adozione di linee guida adeguate da parte degli enti amministrativi. Ad esempio, la FDA statunitense, nel suo rapporto del settembre 2022, ha proposto la sezione 201(h) del Federal Food, Drug, and Cosmetic Act (FD&C Act) per includere software progettati per fornire supporto decisionale per la diagnosi, il trattamento, la prevenzione, la cura o l'attenuazione di malattie o altre condizioni di salute. Inoltre, ai sensi della sezione 520(o)(1)(E), i sistemi di imaging medico come raggi X, tomografia computerizzata (TC), risonanza magnetica (RM) ed ecografia sono idonei per scopi medici. Pertanto, l'implementazione di linee guida garantisce un impatto positivo sulla crescita del mercato.
Il mercato dei software per l'abbinamento delle sperimentazioni cliniche in Canada sta registrando una crescita significativa grazie agli investimenti governativi e ai contributi dei ricercatori. Secondo il rapporto del Canada Institutes of Health Research di luglio 2023, il governo canadese ha investito 250 milioni di dollari per sostenere i fondi per le sperimentazioni cliniche, un'iniziativa volta a rafforzare la strategia canadese per la biofabbricazione e le scienze della vita. Inoltre, nel febbraio 2024, i ricercatori dell'Ontario Institute of Cancer Research hanno sviluppato PMATCH, un sistema automatizzato per abbinare le sperimentazioni cliniche di medicina di precisione ai pazienti oncologici idonei. Pertanto, grazie a tutti questi sviluppi e finanziamenti, il mercato ha maggiori possibilità di crescere ed espandersi.
Statistiche di mercato APAC
Il mercato del software per la gestione degli studi clinici nell'area Asia-Pacifico (APAC) è la regione in più rapida crescita e si prevede che registrerà una crescita redditizia durante il periodo di previsione, grazie alla disponibilità di un elevato numero di pazienti. Inoltre, diverse organizzazioni stanno puntando a collocare le proprie attività di ricerca e sviluppo nella regione per supportare l'espansione del mercato. Ciò è dovuto all'aumento del numero di progetti IT in ambito sanitario, allo sviluppo dell'economia e al completo ammodernamento delle infrastrutture sanitarie, soprattutto nei paesi in via di sviluppo come India e Cina, che denotano la crescita del mercato.
Il mercato dei software per la gestione degli studi clinici in India prevede una crescita sostanziale, poiché questi studi sono facilmente implementabili per la valutazione di terapie a supporto dei pazienti oncologici. Ad esempio, secondo un articolo pubblicato da NLM nel febbraio 2024, NexCAR19 è la prima terapia cellulare CAR-T del Paese ad essere approvata dalla FDA statunitense, sulla base di due studi clinici su 64 pazienti con leucemia avanzata. Secondo gli studi, il 67% dei pazienti ha registrato una significativa riduzione del livello di cancro (risposta oggettiva), con la scomparsa completa del tumore in circa la metà dei casi (risposta completa). Pertanto, con tale sviluppo di terapie innovative, si prevede che il mercato prospererà con successo nel Paese.
Il mercato cinese dei software per l'abbinamento di studi clinici sta guadagnando visibilità grazie all'innovazione e ai progressi nella valutazione dell'aspetto clinico dei pazienti affetti da malattie rare. Secondo l'articolo del NLM del febbraio 2024, è stato condotto uno studio retrospettivo su 1.053 pazienti ricoverati con diagnosi di carcinoma epatocellulare, riguardante la valutazione dell'intelligenza artificiale nel sistema di abbinamento di studi clinici (CTMS). Lo studio ha rivelato un'affidabilità inter-interrogatori accettabile, compresa tra 0,65 e 0,88, con un tasso di accuratezza compreso tra il 92,9% e il 98,0%. Inoltre, la sensibilità è risultata compresa tra il 51,9% e l'83,5%, la specificità tra il 99,0% e il 99,1%, il valore predittivo positivo tra il 75,7% e l'85,1% e il valore predittivo negativo tra il 97,4% e il 98,9%.
Principali attori del mercato del software di abbinamento delle sperimentazioni cliniche:
- Advarra
- Panoramica aziendale
- Strategia aziendale
- Offerte di prodotti chiave
- Performance finanziaria
- Indicatori chiave di prestazione
- Analisi del rischio
- Sviluppo recente
- Presenza regionale
- Analisi SWOT
- Antidote Technologies, Inc.
- Accenture
- Sviluppo clinico IBM
- Applicazione mobile per sperimentazioni cliniche
- SSS Ricerca Clinica Internazionale
- Aris Global
- Clario
- Bsi Business Systems Integration AG
- Microsoft Corporation
- Sistemi Ofni
- Oracolo
- IQVIA
- Syneos Health
Le aziende che dominano il mercato del software per la gestione degli studi clinici stanno ottenendo una rapida visibilità grazie alla crescente domanda di analisi dei dati in tempo reale da parte dei ricercatori. Inoltre, i progressi nell'intelligenza artificiale (IA) stanno riformando le fasi chiave della progettazione degli studi clinici, puntando a tassi di successo cumulativi. Sulla base di ciò, nel gennaio 2024, Accenture ha annunciato un investimento strategico, tramite Accenture Ventures, in QuantHealth per consentire alle aziende farmaceutiche e biotecnologiche di sviluppare trattamenti per i pazienti in modo rapido ed economico. Ciò denota un approccio ottimistico verso un'espansione del mercato efficace ed efficiente.
Inoltre, grazie all'esclusiva tecnologia di intelligenza artificiale basata su un enorme set di dati di 350 milioni di pazienti, enormi grafici basati sulla conoscenza biomedica e dati di studi clinici, la piattaforma di simulazione di QuantHealth è in grado di prevedere i risultati degli studi con notevole accuratezza. Ciò consente inoltre di valutare le variazioni del protocollo e determinare il design di studio ideale per il successo, aiutando i team di ricerca e sviluppo (R&S) a prevedere i risultati degli studi clinici in modo più preciso e rapido, e a decidere se uno studio debba proseguire, ottimizzare le coorti, se i farmaci possano essere riadattati e altri fattori cruciali. Tutti questi fattori contribuiscono alla crescita del mercato a livello globale.
Ecco l'elenco di alcuni giocatori chiave:
Sviluppi recenti
- Nel gennaio 2025, Syneos Health ha firmato un accordo con ACTIVATO per espandere le competenze in materia di sperimentazione clinica in un'ampia gamma di aree terapeutiche in Giappone. L'obiettivo è accelerare l'impatto dello sviluppo clinico in questo mercato in rapida crescita e in continua evoluzione.
- Nel giugno 2024, IQVIA ha annunciato il lancio di One Home for Sites, l'ultima piattaforma tecnologica che funziona come un unico accesso e un'unica dashboard per i sistemi e le attività chiave che un sito di ricerca clinica deve eseguire in tutti gli studi clinici che sta conducendo.
- Nel maggio 2024, Oracle ha apportato miglioramenti alla sua soluzione globale Clinical One Randomization and Trial Supply Management (RTSM), migliorando la regionalizzazione, l'accesso e fornendo assistenza agli utenti con le normative specifiche per paese, oltre all'affidabilità e alla trasparenza delle sperimentazioni dall'inizio alla conclusione.
- Report ID: 7333
- Published Date: Aug 27, 2025
- Report Format: PDF, PPT
- Esplora un’anteprima delle principali tendenze di mercato e degli approfondimenti
- Rivedi tabelle di dati campione e suddivisioni per segmento
- Vivi la qualità delle nostre rappresentazioni visive dei dati
- Valuta la struttura del nostro rapporto e la metodologia di ricerca
- Dai uno sguardo all’analisi del panorama competitivo
- Comprendi come vengono presentate le previsioni regionali
- Valuta la profondità del profilo aziendale e del benchmarking
- Anteprima di come gli insight attuabili possano supportare la vostra strategia
Esplora dati e analisi reali
Domande frequenti (FAQ)
Software di abbinamento per studi clinici Ambito del rapporto di mercato
Il campione gratuito include le dimensioni attuali e storiche del mercato, le tendenze di crescita, grafici e tabelle regionali, profili aziendali, previsioni per segmento e altro ancora.
Contatta il nostro esperto
Copyright © 2026 Research Nester. Tutti i diritti riservati.




