Perspectivas del mercado para el tratamiento de la hemoglobinuria paroxística nocturna:
El mercado del tratamiento de la hemoglobinuria paroxística nocturna se valoró en 5 mil millones de dólares estadounidenses en 2025 y se espera que alcance los 13,94 mil millones de dólares estadounidenses para 2035, registrando una tasa de crecimiento anual compuesta (TCAC) de alrededor del 10.8% durante el período de pronóstico, es decir, entre 2026 y 2035. En 2026, el tamaño de la industria del tratamiento de la hemoglobinuria paroxística nocturna se estima en 5,49 mil millones de dólares estadounidenses.

El sólido crecimiento del mercado se atribuye a la creciente prevalencia de trastornos sanguíneos raros y a los avances en intervenciones terapéuticas, lo que favorece la inversión de las empresas del sector sanitario en el desarrollo, la distribución y la venta de terapias avanzadas para su tratamiento. Un artículo publicado en la Biblioteca Nacional de Medicina sobre las enfermedades hereditarias de la hemoglobina como una carga emergente para la salud mundial predijo que enfermedades como la hemoglobinuria paroxística nocturna causarían una grave carga para la salud mundial, especialmente en las economías emergentes.
La HPN es una enfermedad mediada por el complemento y requiere un tratamiento específico. El mercado mundial del tratamiento de la hemoglobinuria paroxística nocturna (HPN) se beneficia de las innovaciones en los inhibidores de C5. Por ejemplo, en marzo de 2020, un artículo publicado en la Biblioteca Nacional de Medicina indicó que Crovalimab, un anticuerpo con tecnología de reciclaje secuencial de anticuerpos monoclonales, se administró en pequeños volúmenes una vez cada 4 semanas y detectó inhibiciones completas de la vía terminal del complemento en pacientes con HPN, lo que justifica la siguiente fase de desarrollo clínico. El aumento de la aprobación clínica de fármacos para el tratamiento de la HPN, como Solaris (eculizumab), Ultomiris (ravulizumab) y Empaveli (pegcetacoplan), impulsa el crecimiento del mercado. Los actores del mercado se beneficiarán de la creciente adopción de técnicas de diagnóstico avanzadas que facilitan la detección temprana de la HPN.
Los rápidos avances en la secuenciación de ADN facilitan la identificación temprana de la HPN, lo que impulsa el crecimiento del mercado mundial del tratamiento de la hemoglobinuria paroxística nocturna (HPN) a medida que aumenta la demanda de nuevas terapias. Además, los actores del sector se centran en alianzas estratégicas para mejorar los canales de distribución en los mercados emergentes. La creciente demanda de tratamientos para la HPN ha llevado a las compañías farmacéuticas a impulsar la aprobación regulatoria de nuevas terapias. Los nuevos tratamientos que reciben aprobaciones regulatorias impulsan el crecimiento del mercado, ya que fabricantes, distribuidores y usuarios finales se benefician de una tendencia positiva en la aprobación de tratamientos. Por ejemplo, en septiembre de 2024, PIASKY de Roche recibió la aprobación de la Administración de Alimentos y Medicamentos (FDA) de EE. UU. A medida que el sector sanitario mundial aumenta la inversión en terapia génica y medicina de precisión, se prevén nuevas oportunidades en el mercado del tratamiento de la hemoglobinuria paroxística nocturna (HPN), lo que impulsará la sólida curva de crecimiento hacia el final del período de pronóstico.
Clave Tratamiento de la hemoglobinuria paroxística nocturna (HPN) Resumen de Perspectivas del Mercado:
Aspectos destacados regionales:
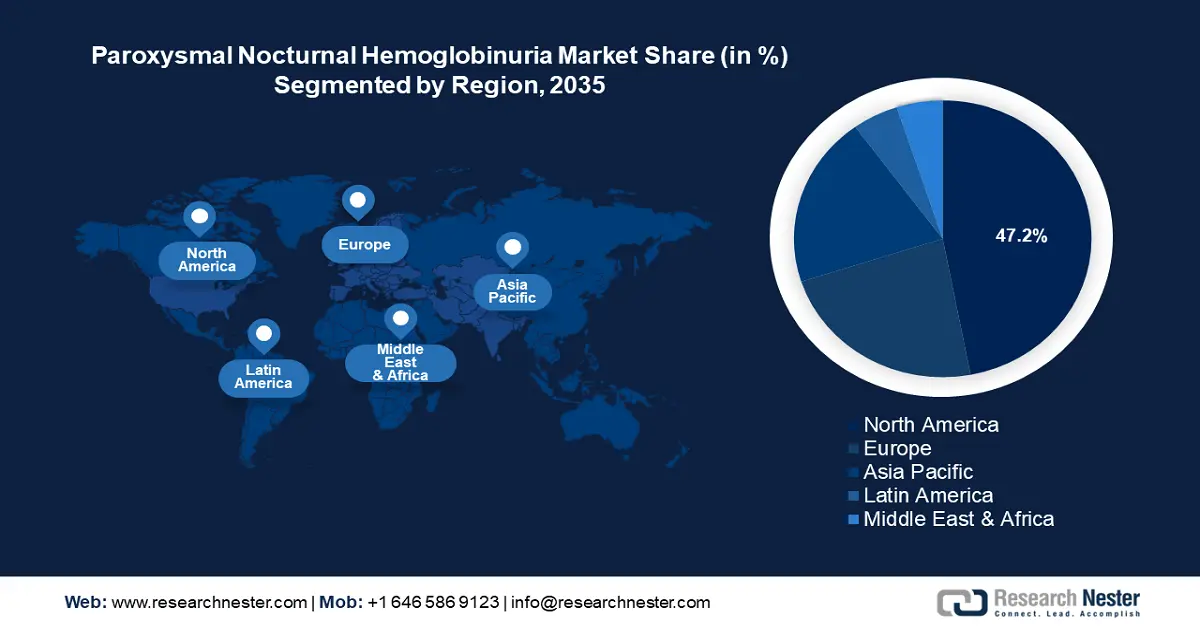
- América del Norte posee una participación del 47,2 % en el mercado de tratamiento de la hemoglobinuria paroxística nocturna, impulsada por una alta tasa de adopción de terapias avanzadas y un sólido marco regulatorio, lo que garantiza un crecimiento hasta 2035.
- Se prevé que el mercado europeo de tratamiento de la hemoglobinuria paroxística nocturna crezca rápidamente para 2035, impulsado por un sólido marco regulatorio y el impulso a la investigación de enfermedades raras.
Perspectivas del segmento:
- Se espera que el segmento de inhibidores del complemento alcance alrededor del 36,1 % de la cuota de mercado para 2035, gracias a su eficacia para reducir las necesidades de transfusión y mejorar la calidad de vida de los pacientes con HPN.
- Se prevé que el segmento de terapia con hierro experimente un sólido crecimiento entre 2026 y 2035, impulsado por su aplicación en el tratamiento de la hemólisis crónica y la anemia en pacientes con HPN.
Tendencias Clave de Crecimiento:
- Aumento de las aprobaciones regulatorias para nuevas terapias
- Avances en inhibidores del complemento
Principales desafíos:
- Conocimiento y diagnóstico limitados
- Alto costo del tratamiento
- Actores clave: AstraZeneca, Apellis Pharmaceuticals Inc., Novartis, Chugai Pharmaceuticals, Roche, UCB, Regeneron Pharmaceuticals.
Global Tratamiento de la hemoglobinuria paroxística nocturna (HPN) Mercado Pronóstico y perspectiva regional:
Tamaño del mercado y proyecciones de crecimiento:
- Tamaño del mercado para 2025: 5 mil millones de dólares
- Tamaño del mercado para 2026: 5490 millones de dólares
- Tamaño proyectado del mercado: 13940 millones de dólares para 2035
- Pronósticos de crecimiento: 10,8 % CAGR (2026-2035)
Dinámicas Regionales Clave:
- Región más grande: América del Norte (47,2 % de participación para 2035)
- Región de mayor crecimiento: Asia Pacífico
- Países dominantes: Estados Unidos, Alemania, Japón, Francia, Reino Unido
- Países emergentes: China, India, Brasil, México, Turquía
Last updated on : 25 August, 2025
Impulsores y desafíos del crecimiento del mercado de tratamiento de la hemoglobinuria paroxística nocturna:
Impulsores del Crecimiento
- Aumento de las aprobaciones regulatorias para nuevas terapias: El sector del tratamiento de la hemoglobinuria paroxística nocturna (HPN) está experimentando un aumento repentino en las aprobaciones de terapias, impulsado por la creciente demanda de tratamientos. La HPN se clasifica como una enfermedad rara y Rare Disease Advisor estima que los casos de HPN en EE. UU. rondan los 0,6 a 6,1 casos por millón de personas. La creciente investigación y el conocimiento de este trastorno sanguíneo raro han acelerado los ensayos clínicos y las tasas de aprobación por parte de los organismos reguladores, lo que permite a las compañías farmacéuticas distribuir opciones de tratamiento en los mercados. La aprobación acelerada de nuevos productos biológicos y terapias génicas impulsa la rápida introducción de tratamientos avanzados, como los inhibidores del complemento, en el mercado del tratamiento de la hemoglobinuria paroxística nocturna (HPN). Por ejemplo, en febrero de 2024, Chugai Pharmaceuticals informó que China fue el primer país en aprobar Crovalimab para el tratamiento de la HPN. El fármaco está destinado a mejorar la comodidad del paciente al permitir la autoinyección cada cuatro semanas.
- Avances en inhibidores del complemento: La creciente investigación y desarrollo de inhibidores del complemento, como los inhibidores de C5 ravulizumab y eculizumab, beneficia al sector global del tratamiento de la hemoglobinuria paroxística nocturna (HPN). Estos productos biológicos atacan la causa raíz de los pacientes con HPN. Además, los avances terapéuticos que mejoran los resultados del paciente y la comodidad impulsan el crecimiento del mercado del tratamiento de la hemoglobinuria paroxística nocturna (HPN). Por ejemplo, en octubre de 2023, la FDA aprobó el inhibidor de C5 del complemento Zilucoplan, bajo el nombre comercial Zilbrysq. A medida que aumentan las inversiones en investigación, se está posicionando para impulsar los estudios sobre inhibidores del complemento de nueva generación que pueden mejorar la eficacia de los tratamientos.
- Expansión de la medicina de precisión y la terapia génica: Las tendencias globales en atención médica están experimentando un impulso favorable a la medicina de precisión, lo que beneficia al mercado de tratamiento de la hemoglobinuria paroxística nocturna (HPN). Los avances en la edición genética CRISPR pueden abordar las mutaciones genéticas responsables de la HPN. Por ejemplo, en enero de 2021, la creación de modelos animales para la HPN mediante la edición genética CRISPR avanzó en la comprensión del mecanismo de patogénesis de la HPN. Además, las terapias emergentes tienen el potencial de proporcionar soluciones curativas que pueden reducir la dependencia a largo plazo de los medicamentos. Por ejemplo, en diciembre de 2023, Novartis presentó los resultados de una investigación de 48 semanas del ensayo de fase 3 APPLY-PNH, que demostró la eficacia a largo plazo de Fabhalta (Iptacopan) en adultos con HPN.
Desafíos
- Conocimiento y diagnóstico limitados: El conocimiento sobre la HPN sigue siendo limitado debido a la rareza del trastorno. Los mercados emergentes de tratamiento de la hemoglobinuria paroxística nocturna (HPN) se enfrentan a obstáculos para su crecimiento debido a la falta de conocimiento, un diagnóstico menos preciso y una infraestructura sanitaria inestable. Un diagnóstico tardío puede impedir que los pacientes reciban un tratamiento oportuno y también reducir la aplicación de nuevas terapias. Además, las complicaciones de la HPN se superponen con otras afecciones, como la anemia, lo que puede dificultar el diagnóstico.
- Alto costo del tratamiento: El alto costo del tratamiento asociado con la HPN puede obstaculizar el crecimiento del mercado de tratamiento de la hemoglobinuria paroxística nocturna (HPN). Los pacientes diagnosticados con HPN a menudo desarrollan anemia, lo que incrementa los costos del tratamiento. Además, los procedimientos de tratamiento complejos requieren especialistas y un equipo médico que puede incrementar los costos. Las dificultades del trasplante de médula ósea se suman a los desafíos del tratamiento. El alto precio puede disuadir a los pacientes de buscar tratamiento y sobrecargar los sistemas de salud. A medida que aumentan las presiones para contener los costos a nivel mundial, las compañías farmacéuticas se enfrentan al problema de equilibrar la asequibilidad con las ganancias.
Tamaño y pronóstico del mercado de tratamiento de la hemoglobinuria paroxística nocturna:
| Atributo del informe | Detalles |
|---|---|
|
Año base |
2025 |
|
Período de pronóstico |
2026-2035 |
|
Tasa de crecimiento anual compuesta (TCAC) |
10,8% |
|
Tamaño del mercado del año base (2025) |
5 mil millones de dólares |
|
Tamaño del mercado según el pronóstico anual (2035) |
13.940 millones de dólares |
|
Alcance regional |
|
Segmentación del mercado de tratamiento de la hemoglobinuria paroxística nocturna:
Tipo de tratamiento (inhibidores del complemento, terapia con hierro, fármacos inmunosupresores, trasplante de médula ósea, otros tipos de tratamiento)
Por tipo de tratamiento, se estima que el segmento de inhibidores del complemento representará alrededor del 36,1 % de la cuota de mercado del tratamiento de la hemoglobinuria paroxística nocturna (HPN) para 2035. El crecimiento del segmento se atribuye al tipo de tratamiento principal para la HPN. Las terapias con inhibidores del complemento permiten a los pacientes mejorar su calidad de vida y reducir la necesidad de transfusiones sanguíneas, lo que contribuye al rápido crecimiento del segmento. La aprobación continua de terapias complementarias junto con inhibidores del complemento, como ravulizumab, permitirá mantener la curva de crecimiento del segmento. Por ejemplo, en abril de 2024, Voydeya (Danicopan) fue aprobado en EE. UU. como terapia complementaria a ravulizumab o eculizumab para el tratamiento de adultos con HPN.
Se prevé que el segmento de tratamiento con hierro en el sector global de tratamiento de la hemoglobinuria paroxística nocturna registre un sólido crecimiento durante el período de pronóstico debido al aumento de su aplicación para el tratamiento de pacientes con hemólisis crónica que provoca deficiencia de hierro. La suplementación con hierro puede ser esencial para abordar la anemia causada por la degradación de glóbulos rojos en pacientes con HPN. Por ejemplo, según la Sociedad Americana de Hematología, las mujeres embarazadas con HPN tienen una mayor necesidad de suplementación con hierro debido a la hemólisis intravascular y, en ciertos casos, las pacientes con HPN pueden requerir hierro intravenoso durante el embarazo. La creciente concienciación sobre los tratamientos para la HPN y el diagnóstico precoz impulsarán la aplicación de la terapia con hierro para abordar complicaciones adicionales en pacientes con HPN.
Vía de administración (parenteral, oral)
Según la vía de administración, se proyecta que el segmento parenteral del mercado global de tratamiento de la hemoglobinuria paroxística nocturna (HPN) aumente su participación en los ingresos al final del período de pronóstico. Este crecimiento se debe a las aplicaciones en inhibidores del complemento como ravulizumab y eculizumab. La vía de administración parenteral garantiza una absorción eficaz, lo que proporciona beneficios inmediatos en el manejo de complicaciones potencialmente mortales. Además, las compañías farmacéuticas buscan mejorar la comodidad del paciente mediante el lanzamiento de nuevas terapias, como crovalimab, que los pacientes pueden autoadministrarse. Por ejemplo, en octubre de 2023, la FDA aprobó el inyector corporal de pegcetacoplan (Empaveli) para la autoadministración en el tratamiento de la HPN. Las tendencias indican avances en formulaciones subcutáneas que están posicionadas para continuar el sólido crecimiento de este segmento.
Nuestro análisis exhaustivo del mercado global de tratamiento de la hemoglobinuria paroxística nocturna (HPN) incluye los siguientes segmentos:
|
Tipo de tratamiento |
|
|
Uso final |
|

Vishnu Nair
Jefe de Desarrollo Comercial GlobalPersonalice este informe según sus necesidades: conéctese con nuestro consultor para obtener información y opciones personalizadas.
Análisis regional del mercado de tratamiento de la hemoglobinuria paroxística nocturna:
Pronóstico del Mercado de Norteamérica
Se prevé que la industria de Norteamérica alcance la mayor participación en los ingresos, con un 47,2%, para 2035, gracias a la alta tasa de adopción de terapias avanzadas y a un sólido marco regulatorio que favorece los ensayos clínicos y la aprobación de nuevos tratamientos. Norteamérica alberga importantes compañías farmacéuticas como Alexion Pharmaceuticals, desarrolladora de Soliris, y Ultomiris favorece su adopción en Norteamérica. Además, programas regulatorios de apoyo, como el Programa de Asistencia al Paciente RareCare de la Organización Nacional de Enfermedades Raras, reembolsan los costos de inscripción a talleres, conferencias y programas educativos relacionados con enfermedades raras, lo que fomenta el conocimiento de los tratamientos para la HPN. Las tendencias favorables en Norteamérica apuntan a que continuará el sólido crecimiento del mercado de tratamiento de la hemoglobinuria paroxística nocturna (HPN).
Estados Unidos posee la mayor participación en el sector de tratamiento de la HPN. El crecimiento del mercado en el país se debe a un sólido ecosistema regulatorio que garantiza la aprobación oportuna de nuevas terapias. Por ejemplo, en diciembre de 2023, McKesson Corporation anunció la disponibilidad de Fabhalta (Iptacopan) de Novartis, tras la aprobación de Fabhalta por parte de la FDA ese mismo mes. Además, el apoyo gubernamental a la investigación en medicina de precisión, con programas como la Iniciativa de Medicina de Precisión, crea un ecosistema propicio para la investigación avanzada sobre la HPN. A medida que instituciones académicas y compañías farmacéuticas colaboran para desarrollar terapias génicas, el mercado se perfila para mantener un crecimiento rentable.
Canadá exhibe un rápido crecimiento en el mercado norteamericano del tratamiento de la hemoglobinuria paroxística nocturna (HPN). Este crecimiento se atribuye a una mayor concienciación sobre el tratamiento de la HPN y a un mejor acceso a terapias avanzadas. Canadá cuenta con un sistema de salud público llamado Medicare que facilita el acceso de los pacientes a los altos costos del tratamiento de la HPN, mejorando así el acceso a una amplia gama demográfica. Además, el sistema regulatorio del país ha sido proactivo en la aprobación de nuevas terapias para el tratamiento de la HPN, lo que impulsa el sector en Canadá. Por ejemplo, en agosto de 2024, Voydeya fue aprobado por Health Canada como complemento de Ultomiris y Soliris en adultos diagnosticados con HPN.
Análisis del Mercado Europeo
Europa está preparada para registrar el crecimiento más rápido en el mercado del tratamiento de la hemoglobinuria paroxística nocturna (HPN) al final del período de pronóstico. Este crecimiento del mercado se debe a un sólido marco regulatorio y al impulso a la investigación de enfermedades raras, lo que beneficia al mercado. La Agencia Europea de Medicamentos (EMA) ha estado a la vanguardia al aprobar terapias líderes para el tratamiento de la HPN, garantizando su disponibilidad en toda la región e impulsando el acceso de los pacientes a terapias nuevas y avanzadas. Por ejemplo, en noviembre de 2020, la Comisión Europea autorizó la comercialización de Alexion para una nueva formulación de Ultomiris con un tiempo de infusión reducido para el tratamiento de la hemoglobinuria paroxística nocturna (HPN) y el síndrome hemolítico urémico atípico (SHUa). Francia y Alemania lideran el mercado europeo del tratamiento de la hemoglobinuria paroxística nocturna (HPN).
Alemania tiene una gran cuota de mercado en el sector de la hemoglobinuria paroxística nocturna en Europa. El mercado alemán se beneficia de su avanzada infraestructura sanitaria y de la presencia de instituciones de investigación y empresas biotecnológicas que impulsan la investigación sobre enfermedades raras. Este marco favorable para la investigación beneficia al mercado nacional del tratamiento de la hemoglobinuria paroxística nocturna (HPN), como lo demuestra el creciente número de ensayos clínicos. Por ejemplo, en abril de 2023, se presentaron datos del ensayo de fase 3 APPOINT-PNH en la reunión anual de 2023 de la Sociedad Europea de Trasplante de Sangre y Médula Ósea (EBMT), destacando que el iptacopan oral permite una reducción estimada del 92,2 % del inhibidor del complemento en pacientes con HPN y un aumento de hemoglobina de 2 g/dl o más sin necesidad de transfusiones sanguíneas.
Francia está en condiciones de registrar un rápido crecimiento en el sector de la hemoglobinuria paroxística nocturna (HPN) en Europa. El crecimiento del mercado del tratamiento de la hemoglobinuria paroxística nocturna (HPN) se debe a marcos sanitarios favorables, como el Plan Nacional Francés para las Enfermedades Raras. El próximo Plan Nacional Francés para las Enfermedades Raras se centrará en la investigación y el desarrollo, según el gobierno, lo que impulsará el crecimiento del sector del tratamiento de la HPN. Además, el Registro Francés del Síndrome de Insuficiencia Ósea ayuda a instituciones de investigación como la Sociedad Americana de Hematología a investigar el perfil molecular para la secuenciación de nueva generación, lo que puede impulsar el crecimiento del mercado. En mayo de 2024, Aspaveli (Pegcetacoplan) fue aprobado en Europa para el tratamiento de pacientes adultos con diagnóstico de HPN y anemia hemolítica. A medida que la investigación sobre HPN se intensifica y un sólido marco regulatorio en Europa beneficia al mercado nacional de tratamiento de la hemoglobinuria paroxística nocturna (HPN) en Francia, se prevé que el sector del tratamiento de la HPN continúe su crecimiento.
Actores clave en el mercado del tratamiento de la hemoglobinuria paroxística nocturna:
-
Se proyecta un sólido crecimiento del mercado mundial de tratamiento de la hemoglobinuria paroxística nocturna durante el período de pronóstico. Los principales actores del mercado están colaborando con distribuidores locales para penetrar en nuevos mercados e invertir en investigación y desarrollo para aumentar la eficacia del tratamiento.
- AstraZeneca
- Descripción general de la empresa
- Estrategia empresarial
- Ofertas de productos clave
- Rendimiento financiero
- Indicadores clave de rendimiento
- Análisis de riesgos
- Desarrollo reciente
- Presencia regional
- Análisis FODA
- Apellis Pharmaceuticals Inc.
- Novartis
- Chugai Pharmaceuticals
- Roche
- UCB
- Regeneron Pharmaceuticals
A continuación, se presentan algunos actores clave del mercado:
Desarrollos Recientes
- En agosto de 2024, Novartis anunció la aprobación acelerada por parte de la FDA de Iptacopan (Fabhalta), el primer inhibidor del complemento para la reducción de la proteinuria en la nefropatía primaria por IgA (NIgA). Esta aprobación acelerada se otorgó con base en el análisis provisional preespecificado del estudio APPLAUSE-NIgA de fase III.
- En julio de 2024, la Administración de Alimentos y Medicamentos (FDA) de EE. UU. aprobó Epysqli para el tratamiento de la HPN. Epysqli es un biosimilar de Soliris y puede prevenir la destrucción de glóbulos rojos en pacientes con HPN.
- Report ID: 6655
- Published Date: Aug 25, 2025
- Report Format: PDF, PPT
- Explore una vista previa de las principales tendencias e ideas del mercado
- Revise tablas de datos de muestra y desgloses por segmento
- Experimente la calidad de nuestras representaciones visuales de datos
- Evalúe nuestra estructura de informe y metodología de investigación
- Obtenga una vista de la análisis del panorama competitivo
- Comprenda cómo se presentan las previsiones regionales
- Evalúe la profundidad del perfilado de empresas y análisis comparativo
- Vea cómo los insights accionables pueden respaldar su estrategia
Explore datos y análisis reales
Preguntas frecuentes (FAQ)
Tratamiento de la hemoglobinuria paroxística nocturna (HPN) Alcance del informe de mercado
La muestra gratuita incluye el tamaño del mercado actual e histórico, tendencias de crecimiento, gráficos y tablas regionales, perfiles de empresas, previsiones por segmento y más.
Conéctate con nuestro experto
Derechos de autor © 2026 Research Nester. Todos los derechos reservados.




