Marktausblick für die Prüfung medizinischer Geräte:
Der Markt für die Prüfung von Medizinprodukten hatte 2025 ein Volumen von über 11,1 Milliarden US-Dollar und wird bis Ende 2035 voraussichtlich auf 25,3 Milliarden US-Dollar anwachsen, was einem durchschnittlichen jährlichen Wachstum von 9,6 % im Prognosezeitraum 2026–2035 entspricht. Im Jahr 2026 wird das Marktvolumen für die Prüfung von Medizinprodukten auf 12,7 Milliarden US-Dollar geschätzt.

Die steigenden regulatorischen Anforderungen in den Ländern treiben das Wachstum des Marktes für die Prüfung von Medizinprodukten voran. FDA, EMA und MHRA fordern Zertifizierungen und Testergebnisse von Herstellern, was zu einer verstärkten Nutzung von Medizinprodukteprüfungen führt. Laut Daten der Weltgesundheitsorganisation geben Länder jährlich mehr als 30,5 Milliarden US-Dollar für minderwertige Medizinprodukte, darunter auch Medizinprodukte, aus, die auf unzureichende Prüfverfahren zurückzuführen sind.
Gesundheitseinrichtungen und Diagnosezentren sind weitgehend auf Medizingeräte wie MRT- und Ultraschallgeräte angewiesen, um verschiedene Organe des menschlichen Körpers zu untersuchen. Defekte Medizingeräte können zu Fehldiagnosen und damit zu negativen Patientenergebnissen führen. Weltweit nehmen Herz-Kreislauf-Erkrankungen zu, wodurch präzise radiologische Bilder zur Bestimmung des Gefährdungsgrades unerlässlich werden. Das Marktwachstum geht mit der Verbesserung der Gerätegenauigkeit einher und ermöglicht so eine effektivere Prävention. Regionen wie der asiatisch-pazifische Raum fördern die Marktexpansion aufgrund kostengünstiger Wartung und qualifizierter Techniker.
Schlüssel Prüfung von Medizinprodukten Markteinblicke Zusammenfassung:
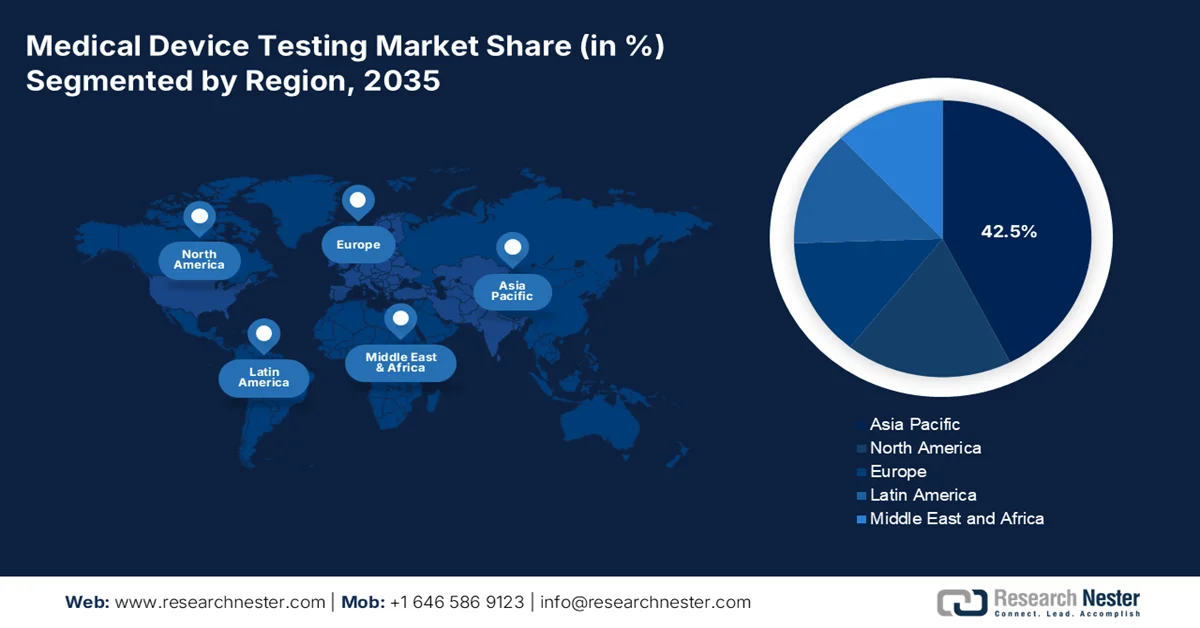
Regionale Highlights:
- Prognosen zufolge wird der Markt für die Prüfung von Medizinprodukten im asiatisch-pazifischen Raum bis 2035 einen beherrschenden Anteil von 42,5 % erreichen, was auf kosteneffiziente Produktionsökosysteme und eine steigende Nachfrage im Gesundheitswesen bei einer großen Patientenpopulation zurückzuführen ist.
- Nordamerika wird voraussichtlich auch 2035 einen substanziellen Marktanteil behalten, was durch starke Forschungskapazitäten und regulatorisch bedingte Testanforderungen für fortschrittliche Bildgebungs- und Diagnosegeräte untermauert wird.
Segmenteinblicke:
- Klinisches Segment: Im Markt für die Prüfung von Medizinprodukten wird dem klinischen Segment bis 2035 voraussichtlich ein dominanter Anteil von 60,5 % zugeschrieben, da es die letzte und wichtigste Zulassungsphase darstellt, die umfangreiche Studien am Menschen gemäß den strengen regulatorischen Vorgaben der FDA und der EMA erfordert.
- Segment Biokompatibilitätsprüfung: Es wird erwartet, dass das Segment der Biokompatibilitätsprüfung bis 2035 den größten Marktanteil einnehmen wird. Dies wird durch seine wichtige Rolle bei der Überprüfung der Gerätesicherheit, der toxizitätsfreien Zusammensetzung und der Einhaltung gesetzlicher Vorschriften zur Minimierung des Patientenrisikos gestützt.
Wichtigste Wachstumstrends:
- Zunahme digitaler Gesundheitsgeräte
- Investitionen im Gesundheitssektor
Größte Herausforderungen:
- Hohe Testkosten
- Lieferkettenengpässe
Wichtige Akteure: TÜV SÜD (Deutschland), DEKRA (Deutschland), BSI Group (Vereinigtes Königreich), Intertek (Vereinigtes Königreich), UL (Underwriters Laboratories) (USA), Eurofins Scientific (Luxemburg), Medistri (Schweiz), NAMSA (USA), Eurofins BioPharma Services (USA), Covance (USA)
Global Prüfung von Medizinprodukten Markt Prognose und regionaler Ausblick:
Marktgröße und Wachstumsprognosen:
- Marktgröße 2025: 11,1 Milliarden US-Dollar
- Marktgröße 2026: 12,7 Milliarden US-Dollar
- Prognostizierte Marktgröße: 25,3 Milliarden US-Dollar bis 2035
- Wachstumsprognose: 9,6 % jährliches Wachstum (2026–2035)
Wichtigste regionale Dynamiken:
- Größte Region: Asien-Pazifik (42,5 % Anteil bis 2035)
- Region mit dem schnellsten Wachstum: Asien-Pazifik
- Dominierende Länder: Vereinigte Staaten, China, Deutschland, Japan, Vereinigtes Königreich
- Schwellenländer: Indien, Brasilien, Südkorea, Mexiko, Singapur
Last updated on : 10 February, 2026
Markt für die Prüfung medizinischer Geräte – Wachstumstreiber und Herausforderungen
Wachstumstreiber
- Zunahme digitaler Gesundheitsgeräte: Das weltweite Bevölkerungswachstum führt zu einer höheren Prävalenz chronischer Erkrankungen und damit zu einer verstärkten Nutzung digitaler Gesundheitsgeräte wie Smartbands, die es Ärzten ermöglichen, Patienten aus der Ferne zu überwachen. Wearables und andere digitale Gesundheitsgeräte werden kontinuierlich weiterentwickelt und modifiziert, um Fehler zu minimieren. Hersteller testen ihre Produkte oft intern, um Kosten zu senken. Dabei werden Hardware und Software umfassend geprüft, um eine kontinuierliche Leistungsfähigkeit zu gewährleisten. Schwellenländer wie China und Indien produzieren in großem Umfang Medizinprodukte, die ebenfalls ständige Weiterentwicklungen und Tests erfordern und so zu einer höheren Marktakzeptanz beitragen. Laut der National Library of Medicine tragen 21 % der US-Bevölkerung Fitness-Tracker, die präzise Messungen und damit strenge Tests erfordern und so das Marktwachstum fördern.
- Investitionen im Gesundheitssektor: Die Marktnachfrage wird durch umfangreiche Investitionen der Regierung und anderer Institutionen zur Verbesserung der diagnostischen Effektivität und zur Erzielung positiver Patientenergebnisse angetrieben. Laut OECD-Daten von 2023 werden über 11,5 % des BIP für die Verbesserung der Gesundheitsinfrastruktur aufgewendet, was die Nachfrage nach Medizingeräten und damit einhergehend vermehrte Tests und Weiterentwicklungen verdeutlicht. Japans medizinische Infrastruktur ist technologieabhängig und nutzt komplexe, hochmoderne Medizingeräte. Diese Systeme kommen häufig in kritischen Bereichen wie der Reanimation und der Notaufnahme zum Einsatz und tragen zur Lebenserhaltung bei. Daher ist die Genauigkeit und Präzision dieser Systeme unerlässlich, was das Marktwachstum zusätzlich ankurbelt.
- Technologische Weiterentwicklungen: Weltweit werden Medizingeräte innovativ weiterentwickelt, was zu effektiveren Behandlungen und Diagnosen chronischer Erkrankungen führt. Hersteller integrieren KI und Cloud-Computing in Medizingeräte und treiben so das Marktwachstum voran. Die hochmodernen Medizingeräte müssen umfangreichen Tests unterzogen werden, um die korrekte Integration von Software und Hardware zu gewährleisten. Roboterassistierte Operationsgeräte werden in Gesundheitseinrichtungen zunehmend eingesetzt, um Schmerzen während Operationen zu minimieren und eine höhere diagnostische Genauigkeit zu erzielen. Dies erfordert umfangreiche Tests und Anpassungen, um Fehler zu reduzieren und einheitliche Operationsergebnisse zu gewährleisten, was wiederum die Marktexpansion fördert.
Herausforderungen
- Hohe Prüfkosten: Die Prüfung von Medizinprodukten kann sehr teuer sein, was das Marktwachstum bremst. Hersteller bevorzugen zudem interne Produktprüfungen, um Kosten zu senken. Dies schränkt die Möglichkeiten für Outsourcing ein und bremst somit das Marktwachstum. Die zunehmenden behördlichen Auflagen führen zu längeren Wartezeiten und damit zu höheren Prüfkosten.
- Lieferkettenengpässe: Die Prüfung von Medizinprodukten erfordert spezielle Ausrüstung, deren Beschaffung aufgrund geopolitischer Probleme oft schwierig ist. Die eingeschränkte Verfügbarkeit der Materialien hat das Marktwachstum stark beeinträchtigt und zu einem Rückgang der Medizinprodukteprüfung geführt. Hersteller lagern die Prüfungen häufig an renommierte Labore aus, die mit der stark gestiegenen Nachfrage überlastet sind. Dies kann zu Verzögerungen bei den Prüfungen führen und das Marktwachstum weiter bremsen.
Marktgröße und Prognose für die Prüfung medizinischer Geräte:
| Berichtsattribut | Einzelheiten |
|---|---|
|
Basisjahr |
2025 |
|
Prognosejahr |
2026–2035 |
|
CAGR |
9,6 % |
|
Marktgröße im Basisjahr (2025) |
11,1 Milliarden US-Dollar |
|
Prognostizierte Marktgröße (2035) |
25,3 Milliarden US-Dollar |
|
Regionaler Geltungsbereich |
|
Marktsegmentierung für die Prüfung medizinischer Geräte:
Phasensegmentanalyse
Es wird erwartet, dass das klinische Segment bis Ende 2035 mit 60,5 % den größten Anteil am Markt für Medizinprodukte halten wird. Dies ist auf die rasante Entwicklung von Medizinprodukten zurückzuführen, bei denen klinische Studien als letzte Phase des Zulassungsverfahrens gelten. Medizinprodukte werden an Menschen getestet, um ihre Wirksamkeit und Anwendbarkeit zu verbessern. Die verschärften globalen Vorschriften von Behörden wie der FDA und der EMA erfordern umfassende Bewertungen und klinische Zulassungen, um die Belastung für die Patienten so gering wie möglich zu halten und die Patientenversorgung zu optimieren. Klinische Studien gelten allgemein als sicher, woraufhin die Produkte auf den Markt gebracht werden, was das Wachstum des Marktes für die Prüfung von Medizinprodukten weiter ankurbelt. Wearables werden häufig direkt auf der Haut getragen, was aufgrund loser Anschlüsse zu Stromschlägen führen kann. Daher sind Tests erforderlich, um die Sicherheit und Wirksamkeit der Geräte zu gewährleisten.
Segmentanalyse der Dienstleistungsarten
Der Biokompatibilitätstest nimmt aufgrund seiner Bedeutung für die Prüfung der Sicherheit und Genauigkeit von Medizinprodukten den größten Anteil ein. Biokompatibilitätstests bewerten Produkte umfassend und minimieren so potenzielle Risiken. Sie gewährleisten, dass Medizinprodukte frei von toxischen, mutagenen und immunogenen Komponenten sind, die dem Patienten schaden könnten. Die Zulassungsbehörden fordern strenge Produktprüfungen, einschließlich Biokompatibilitätstests, um Infektionen und Hautreizungen während der Anwendung weiter auszuschließen. Die von den Herstellern durchgeführten Biokompatibilitätstests erweitern den Markt erheblich.
Unsere detaillierte Analyse des globalen Marktes umfasst die folgenden Segmente:
Segment | Teilsegmente |
Serviceart |
|
Phasentyp |
|

Vishnu Nair
Leiter - Globale GeschäftsentwicklungPassen Sie diesen Bericht an Ihre Anforderungen an – sprechen Sie mit unserem Berater für individuelle Einblicke und Optionen.
Markt für die Prüfung medizinischer Geräte – Regionale Analyse
Einblicke in den asiatisch-pazifischen Markt
Der asiatisch-pazifische Markt (APAC) wird voraussichtlich einen Anteil von 42,5 % halten. Grund dafür sind die niedrigen Herstellungskosten für Testkomponenten, die es den Anbietern ermöglichen, die weltweite Nachfrage nach Tests für Medizinprodukte zu steigern. Stryker eröffnete 2024 eine Einrichtung für Lebenszyklustests von Medizinprodukten, um potenzielle Risiken zu minimieren und die Wirksamkeit zu ermitteln. Das neue Labor verfügt über qualifizierte Mikrobiologen, die umfassende mikrobiologische Tests der Produkte durchführen und so deren Sicherheit erhöhen. Die große Bevölkerung in der Region hat die Verbreitung von Krankheiten begünstigt, wodurch der Bedarf an präzisen Systemen unerlässlich wird und das Wachstum des asiatisch-pazifischen Marktes weiter ankurbelt.
China verfügt aufgrund der niedrigen Komponenten- und Arbeitskosten über ein starkes Produktionsökosystem, das den Markt für Elektrotechnik und Elektronik antreibt. Das stetige Wachstum dieses Marktes verstärkt wiederum das Wachstum des Marktes für Medizinprodukte, der strenge Prüfungen und Zertifizierungen erfordert. Die kostengünstige Fertigung und das kontinuierliche Wachstum der Medizinprodukteproduktion erweitern den Markt. China ist bevölkerungsreich und die Prävalenz chronischer Krankheiten nimmt zu, was präzise Testergebnisse erfordert und den Markt für Medizinprodukteprüfungen weiter beflügelt.
Indien baut seine Gesundheitsinfrastruktur, insbesondere nach der Pandemie, stetig aus. Um der steigenden Nachfrage gerecht zu werden, werden derzeit Krankenhäuser und Diagnosezentren errichtet. Kliniken und Krankenhäuser setzen zahlreiche medizinische Geräte ein, darunter MRT- und CT-Systeme, die Bilder der menschlichen Körperstrukturen erzeugen. Diese Systeme müssen hinsichtlich ihrer Funktionen und ihrer Leistungsfähigkeit in Notfällen umfassend getestet werden. Die Präsenz mehrerer wichtiger Akteure im Land motiviert die Hersteller, sich Prüfungen zu unterziehen und Qualitätszertifizierungen zu erlangen.
Einblicke in den nordamerikanischen Markt
Nordamerika verfügt über ausgeprägte Forschungs- und Innovationskompetenzen, die das Wachstum fortschrittlicher Medizinprodukte vorantreiben, deren Wirksamkeit durch Tests nachgewiesen werden muss. Die Region beherbergt zudem eine große Anzahl von Menschen mit vielfältigen medizinischen Bedürfnissen, die bildgebende Verfahren wie MRT und CT benötigen, um Krankheiten effektiv erkennen zu können. Solche Geräte müssen getestet werden, um eine patientenorientierte Versorgung und positive Behandlungsergebnisse zu gewährleisten. Behörden und Aufsichtsorgane drängen Hersteller zur Vorlage von Testzertifikaten, die durch die Minimierung potenzieller Risiken die Genauigkeit und Biokompatibilität der Produkte sicherstellen. Die Innovationskraft und die große Bevölkerungszahl sind maßgebliche Treiber des nordamerikanischen Marktes für die Prüfung von Medizinprodukten.
Die US-amerikanische Arzneimittelbehörde FDA hat strenge Richtlinien und Vorschriften erlassen, die die Geräteprüfung und die Erlangung von Zulassungszertifikaten standardisieren und so zur Sicherstellung von Qualität und Leistung beitragen. In den USA steigt das verfügbare Einkommen, was Patienten dazu veranlasst, eine hochwertige Gesundheitsversorgung in Anspruch zu nehmen und dadurch die Nutzung von Medizinprodukten beschleunigt. Zahlreiche Krankenhäuser und Kliniken haben ebenfalls Medizinprodukte eingeführt, um die steigende Nachfrage der Bevölkerung zu decken. Die Leistungsprüfung dieser Geräte unterstützt die Entscheidungsfindung und trägt zu einer besseren Gesundheitsversorgung der Patienten bei. Die Bemühungen der FDA und das steigende verfügbare Einkommen der Bevölkerung fördern das Wachstum des Marktes für medizinische Testgeräte in den USA.
Der kanadische Markt für die Prüfung von Medizinprodukten wird von regulatorischen Vorgaben, Innovation und Patientensicherheit bestimmt, was eine patientenorientierte Versorgung fördert. Das Land konzentriert sich auf die Durchführung klinischer Studien für Medizinprodukte, um deren Eignung und Verträglichkeit am Menschen zu beurteilen. Die Langzeitstudien verbessern die Leistungsfähigkeit der Produkte und minimieren das Anwendungsrisiko. Auch die Marktbeobachtung ist wichtig: Patientenfeedback und -reaktionen werden erfasst, um die Wirksamkeit der Produkte zu verstehen und diese weiter zu verbessern, damit Patienten eine einheitliche Versorgung erhalten.
Einblicke in den europäischen Markt
Der europäische Markt für die Prüfung von Medizinprodukten wird aufgrund von Innovationen und verschärften Regulierungen voraussichtlich bis Ende 2035 einen bedeutenden Anteil einnehmen. In Europa gelten strenge Vorschriften für Medizinprodukte, die Hersteller verpflichten, Wirksamkeitsnachweise zu erbringen, um die patientenorientierte Versorgung zu verbessern. Die Innovationskraft der Region beschleunigt das Marktwachstum zusätzlich. Künstliche Intelligenz und Cloud-Computing in Medizinprodukten erfordern umfangreiche Prüfungen und iterative Verbesserungen, um Anwendungsfehler zu vermeiden. Der britische Gesundheitsdienst NHS und andere Institutionen fördern die Fernüberwachung von Patienten und benötigen daher präzise Gesundheitstracker, auf deren Grundlage eine effektive Diagnose gestellt werden kann.
Das Vereinigte Königreich verfügt über eine große Anzahl von Krankenhäusern und Kliniken, die die Zugänglichkeit verbessern und dadurch den Bedarf an Medizinprodukten steigern. Diese Geräte werden von externen Unternehmen auf ihre Eigenschaften und ihre Wirksamkeit in der patientenorientierten Versorgung geprüft. Auch die steigende Produktion trägt maßgeblich zur Nachfrage nach Medizinprodukteprüfungen im Land bei. Mit der zunehmenden Innovation der Hersteller in ihren Produktportfolios wird auch die Nachfrage nach Medizinprodukteprüfungen steigen. Gemäß den britischen Vorschriften ist die Norm ISO 10993 für Produkte unerlässlich, da sie umfangreiche Produktprüfungen und die Bewertung der Biokompatibilität erfordert. Der Ausbau der Gesundheitsinfrastruktur und die staatlichen Regulierungen verstärken das Wachstum des britischen Marktes.
Der deutsche Markt für die Prüfung von Medizinprodukten unterliegt bestimmten Richtlinien und Protokollen für digitale Gesundheitsüberwachungsgeräte. Diese Produkte müssen von staatlichen Stellen auf Leistungsfähigkeit und Biokompatibilität geprüft werden. Deutschland bevorzugt klinische Studien für alle Medizinprodukte, die bei kritischen und komplexen Eingriffen wie kardiologischen und onkologischen Operationen eingesetzt werden. Roboterassistierte Operationen nehmen in Deutschland zu und beflügeln das Marktwachstum. Die Tests umfassen auch die Entnahme von Proben bei den Patienten, um die Genauigkeit und Wirksamkeit der Medizinprodukte zu überprüfen.
Wichtigste Akteure auf dem Markt für Medizinprodukteprüfung:
- TÜV SÜD (Deutschland)
- DEKRA (Deutschland)
- BSI-Gruppe (Vereinigtes Königreich)
- Intertek (Vereinigtes Königreich)
- UL (Underwriters Laboratories) (USA)
- Eurofins Scientific (Luxemburg)
- Medistri (Schweiz)
- NAMSA (USA)
- Eurofins BioPharma Services (USA)
- Covance (USA)
- Unternehmensübersicht
- Geschäftsstrategie
- Wichtigste Produktangebote
- Finanzielle Leistung
- Wichtigste Leistungsindikatoren
- Risikoanalyse
- Aktuelle Entwicklung
- Regionale Präsenz
- SWOT-Analyse
Die Akteure im Markt für die Prüfung medizinischer Geräte werden im Prognosezeitraum voraussichtlich einem intensiven Wettbewerb ausgesetzt sein. Der Markt ist sowohl von etablierten Marktführern als auch von neuen Marktteilnehmern geprägt. Dennoch ist das Marktwachstum moderat. Neue Marktteilnehmer setzen die etablierten Unternehmen stark unter Druck und verhindern, dass diese einen Großteil des Umsatzanteils erzielen. Spezialisierte Hersteller sorgen für ein wettbewerbsintensives Marktumfeld. Die wichtigsten Marktteilnehmer erhalten erhebliche staatliche Unterstützung für Forschung und Innovation.
Unternehmenslandschaft des Marktes für die Prüfung medizinischer Geräte:
- TÜV SÜD : Ein Unternehmen, das sich auf Prüf- und Qualitätsmanagementdienstleistungen für Medizinprodukte spezialisiert hat. Es führt klinische Studien und Biokompatibilitätsstudien durch, um die Produktqualität und -wirksamkeit zu bewerten. TÜV SÜD erfüllt die Anforderungen verschiedener Aufsichtsbehörden wie der FDA und der EMA, was die Durchführung effektiver Studien mit Medizinprodukten ermöglicht.
- DEKRA: Ein führender Anbieter von Prüfdienstleistungen für Medizinprodukte mit einem breiten Portfolio, darunter Prüfungen zur Einhaltung regulatorischer Vorgaben, Biokompatibilität und klinische Studien. Das Unternehmen bedient verschiedene Branchen, darunter die Automobil-, Gesundheits- und Elektronikindustrie, die strenge Produktprüfungen fordern. Die Risikobewertung und Qualitätssicherung werden von Herstellern häufig genutzt, um potenzielle Produktrisiken zu minimieren.
- BSI Group: Das Unternehmen zählt zu den ältesten und renommiertesten Dienstleistern mit langjähriger Erfahrung in standardisierten Prüfverfahren. Es bietet Prüfungen für Medizinprodukte mit Schwerpunkt auf behördlichen Zulassungen, Biokompatibilitätstests und ISO-Zertifizierungen an, die von Europa und der FDA akkreditiert sind. Dank seiner umfassenden Expertise im Zulassungsprozess von Medizinprodukten ist die BSI Group in zahlreichen Ländern vertreten.
- Intertek ist ein in Großbritannien ansässiges Unternehmen für Qualitätssicherung und Zertifizierung, das verschiedene Branchen, darunter das Gesundheitswesen und die Automobilindustrie, bedient. Der Fokus liegt auf Produktqualitätsprüfungen, Konformitätsprüfungen und Biokompatibilitätstests, die Produktzertifizierungen und deren Markteinführung ermöglichen. Intertek ermutigt Hersteller weltweit, ihre Produkte prüfen und zertifizieren zu lassen.
- Underwriters Laboratories (UL): Ein weltweit tätiges Unternehmen für Sicherheitswissenschaften, das sich auf die Prüfung, Zertifizierung und Inspektion von Medizinprodukten und einer Reihe weiterer Produkte spezialisiert hat. UL bietet zudem elektrische und Materialprüfungen für Medizinprodukte an und trägt so zur Erhöhung der Produktsicherheit bei. UL ist von der FDA und der EMA, den wichtigsten Zulassungsbehörden für Medizinprodukte, anerkannt.
Hier ist eine Liste der wichtigsten Akteure auf dem globalen Markt:
Neueste Entwicklungen
- Im Januar 2025 eröffnete Eurofins sein neues Verpackungsprüflabor, um den Markt für die Prüfung von Medizinprodukten zu erweitern. Die neue Einrichtung wird die Biokompatibilität und Sterilität der Produkte messen. Sie wird die regulatorischen Prüfungen in den USA, Europa und im asiatisch-pazifischen Raum verbessern.
- Im Januar 2025 kündigte Medistri die Expansion in Ungarn an, um den Zugang zu Gesundheitslösungen zu verbessern. Die neue Anlage bietet eine Sterilisationskapazität von über 15.000 Paletten pro Jahr und deckt damit den Bedarf optimal. Die hauseigenen Labordienstleistungen gewährleisten eine lückenlose Qualitätskontrolle und hohe betriebliche Effizienz.
- Report ID: 3866
- Published Date: Feb 10, 2026
- Report Format: PDF, PPT
- Entdecken Sie eine Vorschau auf die wichtigsten Markttrends und Erkenntnisse
- Prüfen Sie Beispiel-Datentabellen und Segmentaufgliederungen
- Erleben Sie die Qualität unserer visuellen Datendarstellungen
- Bewerten Sie unsere Berichtsstruktur und Forschungsmethodik
- Werfen Sie einen Blick auf die Analyse der Wettbewerbslandschaft
- Verstehen Sie, wie regionale Prognosen dargestellt werden
- Beurteilen Sie die Tiefe der Unternehmensprofile und Benchmarking
- Sehen Sie voraus, wie umsetzbare Erkenntnisse Ihre Strategie unterstützen können
Entdecken Sie reale Daten und Analysen
Häufig gestellte Fragen (FAQ)
Prüfung von Medizinprodukten Umfang des Marktberichts
Die kostenlose Stichprobe umfasst aktuelle und historische Marktgrößen, Wachstumstrends, regionale Diagramme und Tabellen, Unternehmensprofile, segmentweise Prognosen und mehr.
Kontaktieren Sie unseren Experten
Urheberrecht © 2026 Research Nester. Alle Rechte vorbehalten.




