体外诊断市场展望:
2025年体外诊断市场规模为781亿美元,预计到2035年底将达到1522亿美元,在预测期(即2026-2035年)内,复合年增长率为6.9%。2026年,体外诊断行业规模估计为834亿美元。

市场增长轨迹主要受慢性病和传染病预防筛查项目检测量不断增长的影响,而这主要是由人口结构和公共卫生压力驱动,而非个人需求。根据美国国立卫生研究院 (NIH) 2023 年 11 月发布的研究,美国十分之六的人至少患有一种慢性病,十分之四的人患有多种慢性病,这导致各医疗机构对常规和长期诊断检测的需求增加。美国糖尿病协会 2023 年 11 月的报告显示,仅糖尿病一项就影响了美国超过 3800 万人,这进一步凸显了实验室检测在监测和风险分层方面的高利用率。传染病监测仍然是另一个结构性需求驱动因素。世界卫生组织 2025 年 11 月的报告记录了全球超过 1070 万例结核病病例,并指出需要持续监测艾滋病毒、乙型肝炎、丙型肝炎和新出现的病原体。
美国慢性病患病率及影响
统计学 | 价值 | 详情/来源参考 |
患有至少一种主要慢性疾病的人 | 1.29亿 | 包括心脏病、癌症、糖尿病、肥胖症、高血压;由美国卫生与公众服务部定义。 |
与慢性疾病相关的主要死亡原因 | 前十名中的前五名 | 可预防和可治疗的慢性疾病。 |
患病率趋势 | 稳步增长 | 过去二十年来,这种情况一直持续下去;预计未来还将继续。 |
多种慢性疾病 | 42%的人拥有2个或以上;12%的人拥有5个或以上。 | 受影响比例不断增加。 |
医疗保健支出归因 | 每年 4.1 万亿美元的 90% | 慢性疾病和精神健康状况的管理/治疗 |
资料来源:美国疾病控制与预防中心,2024年2月
政府支持的筛查计划,例如欧美地区的人群癌症筛查项目,进一步提升了基线检测量,而人口老龄化则增加了医院和参考实验室网络的检测利用率。这些因素共同支撑着一个稳定、高通量的诊断检测环境,并确保了试剂、仪器和耗材采购周期的可预测性。从政策和资金角度来看,公共医疗支出和监管在塑造市场格局方面发挥着决定性作用。美国医院协会2024年12月发布的报告指出,2023年美国国家医疗支出达到4.9万亿美元,其中实验室服务是诊断诊疗路径中不可或缺的重要组成部分。诸如临床实验室收费标准等报销机制直接影响着检测项目的组合和普及率,尤其对高通量检测项目影响显著。
关键 体外诊断 市场洞察摘要:
区域亮点:
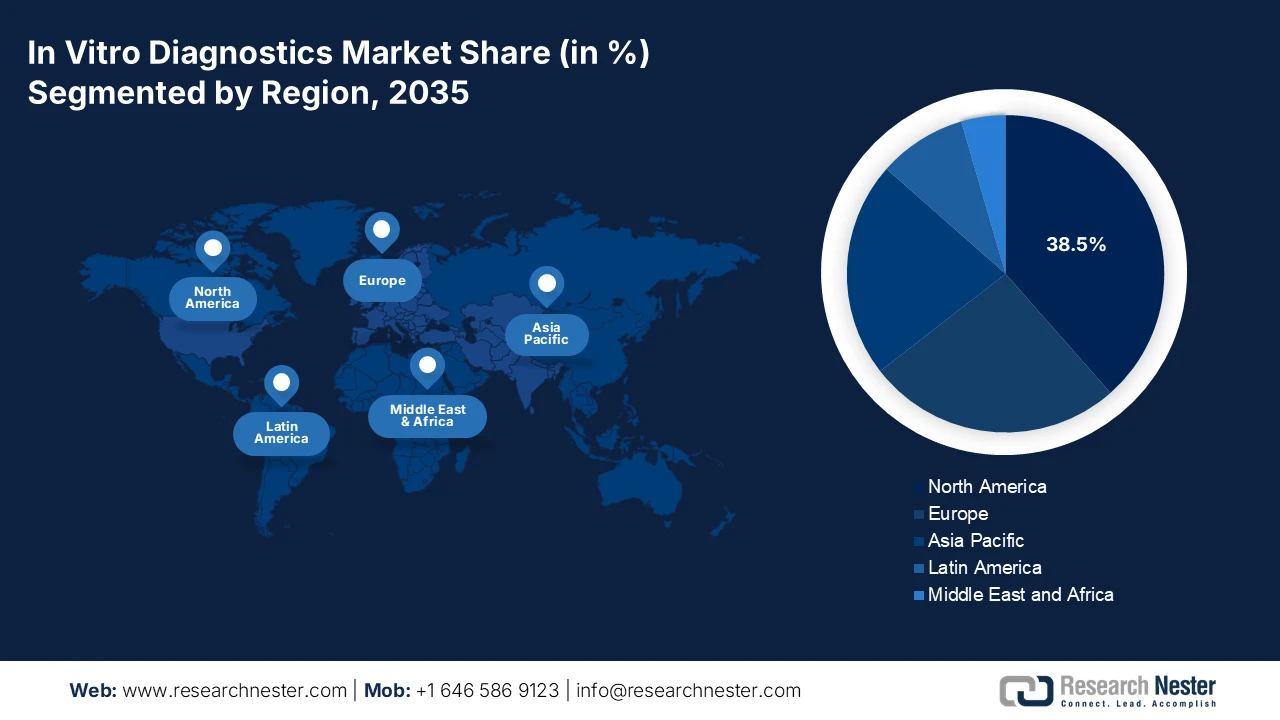
- 预计到 2035 年,北美体外诊断市场将占据 38.5% 的收入份额,这得益于先进的医疗保健基础设施、精准医疗的强劲普及以及在 FDA 和 CMS 的有利框架下支持的人工智能诊断平台。
- 亚太地区预计将成为增长最快的地区,在 2026 年至 2035 年期间的复合年增长率将达到 6.8%,这得益于大规模的公共医疗保健投资、慢性病患病率的上升以及即时诊断和分子诊断的快速普及。
细分市场洞察:
- 体外诊断市场中的试剂和试剂盒细分市场预计将在 2035 年占据 75.4% 的市场份额,这得益于其循环消费模式、不断扩大的基于生物标志物的测试菜单以及大规模的公共卫生监测采购。
- 预计到 2035 年,医院和诊所将占据最大的终端用户份额,这得益于它们集中了复杂的诊断工作量,以及自动化、高通量实验室系统的加速部署。
主要增长趋势:
- 慢性疾病负担加重推动纵向检测
- 诊断是全民健康覆盖的重要支柱。
主要挑战:
- 报销流程复杂且价格压力大。
- 技术快速过时
主要参与者:罗氏诊断、雅培实验室、丹纳赫公司、西门子医疗、赛默飞世尔科技、强生公司、希森美康公司、贝克顿·迪金森公司、生物梅里埃、奎斯特诊断、基立福、博雅生物、凯杰、迈瑞、豪洛捷、迪亚索林、深圳迈瑞生物医疗电子、积水医疗、Ortho Clinical Diagnostics、Werfen。
全球 体外诊断 市场 预测与区域展望:
市场规模及增长预测:
- 2025年市场规模: 781亿美元
- 2026年市场规模: 834亿美元
- 预计市场规模:到2035年将达到1522亿美元
- 增长预测:年复合增长率 6.9%(2026-2035 年)
关键区域动态:
- 最大区域:北美(到2035年占38.5%的份额)
- 增长最快的地区:亚太地区
- 主要国家:美国、德国、日本、中国、英国
- 新兴国家:印度、韩国、新加坡、巴西、澳大利亚
Last updated on : 30 January, 2026
体外诊断市场——增长驱动因素和挑战
增长驱动因素
- 慢性病负担加重推动纵向检测:慢性病患病率持续上升,扩大了对常规和重复诊断检测的基本需求,从而推动了体外诊断市场的发展。美国疾病控制与预防中心(CDC)的报告指出,美国许多人患有慢性病,需要持续的实验室监测。此外,糖尿病也是对生化和免疫分析检测产生持续需求的疾病之一。全球范围内也出现了类似的趋势,世界卫生组织(WHO)2025年9月的报告指出,非传染性疾病占全球死亡人数的74%。大量的疾病病例推动了检测需求的增长,并促使企业采用可扩展的试剂供应模式以及与中心实验室签订长期服务协议。
- 诊断是全民健康覆盖的支柱:诊断是直接影响市场准入质量和医疗服务效果的关键驱动因素。世界卫生组织2025年3月发布的报告估计,近70%的临床决策取决于诊断测试结果,这凸显了实验室服务在有效治疗路径中的核心作用。然而,各国政府和多边机构正在扩大国家基本诊断清单,并将公共资金用于实验室能力建设、人员培训和供应链强化。这些政策驱动的投资正在将诊断纳入公共资助的初级和二级医疗保健体系。从市场角度来看,这种转变支持新兴经济体持续的、以数量为导向的需求增长,主要体现在政府采购和捐助方支持的卫生项目中,而非可自由支配的私人支出中。
- 政府对精准医疗计划的资助:国家对精准医疗或个性化医疗的投资正在推动伴随诊断和先进基因组检测的需求。这些计划资助用于指导靶向治疗的检测方法的研究、开发和整合。美国国立卫生研究院 (NIH) 资助的“我们所有人”研究计划旨在收集一百万人的基因和健康数据,这本身就促进了基因组测序及相关诊断方法的应用。同样,英国基因组学计划 (Genomics England) 和澳大利亚等国的国家基因组医学计划也强制要求使用特定的基于二代测序 (NGS) 的诊断方法,从而为与资助治疗方案相关的已获批准的检测方法创造了有保障的市场。
挑战
- 报销流程复杂且价格压力巨大:在市场上,从保险公司获得有利的报销代码和支付费率至关重要。各国政府积极限制药品价格以控制医疗预算。尽管检测试剂盒具有突破性意义,但由于联邦医疗保险(Medicare)的影响,领先厂商推出的此类产品仍面临多年的报销挑战,难以获得商业认可。虽然市场有所增长,但日本和欧盟等主要市场的政府价格限制压缩了制造商的利润空间。
- 技术快速过时:快速的创新步伐可能导致新产品迅速过时。企业必须持续投资于下一代平台。例如,专注于传统PCR系统的公司将面临被拥有液滴数字PCR技术的公司的取代,后者在液体活检等特定应用领域具有更高的精度,相关内容已在年度研发投资报告中详细阐述。
体外诊断市场规模及预测:
| 报告属性 | 详细信息 |
|---|---|
|
基准年 |
2025 |
|
预测年份 |
2026-2035 |
|
复合年增长率 |
6.9% |
|
基准年市场规模(2025 年) |
781亿美元 |
|
预测年份市场规模(2035 年) |
1522亿美元 |
|
区域范围 |
|
体外诊断市场细分:
产品与服务细分市场分析
试剂盒及试剂子细分市场占据主导地位,预计到2035年底将占据75.4%的市场份额。这一主导地位源于诊断检测固有的高用量重复消费模式,其中仪器通常与长期服务合同捆绑销售,以确保试剂的持续采购。肿瘤学、神经病学和传染病领域的新生物标志物的不断涌现推动了检测项目的持续扩展,直接促进了试剂的销售。公共卫生部门对传染病监测的投入是推动这一增长的关键因素。根据美国国家过敏症和传染病研究所2025年的数据,到2025年,过敏和传染病研究的经费将达到65.81亿美元,主要用于购买检测试剂盒和试剂,以维持国家监测和应对能力。这种批量采购试剂的模式旨在维持国家监测和应对能力。这种公共卫生领域的批量采购模式凸显了该细分市场的稳定性和增长潜力,而高通量实验室平台的自动化进一步促进了这一增长。
美国国家过敏症和传染病研究所(NIAID)研究经费历史(截至2025年)
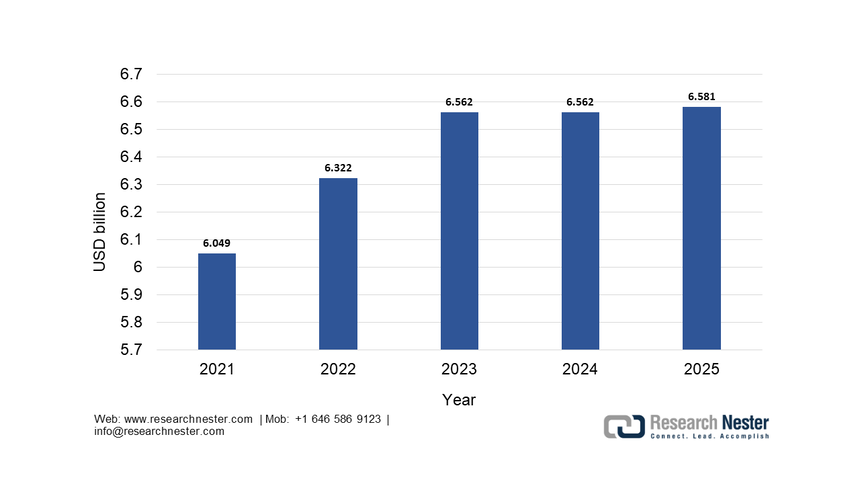
资料来源:NIAID 2025
最终用户细分分析
医院和诊所仍然是体外诊断市场的主要终端用户,预计将占据最大的市场份额。其核心地位源于它们作为急症急救和高复杂度检测的主要枢纽,这些检测无法分散进行。该领域的增长得益于集成式自动化实验室系统的普及,这些系统旨在高效处理海量检测,同时医院肿瘤科和心脏科中心也扩展了专业检测。美国政府的医疗保健支出数据提供了重要的统计佐证。根据美国医疗保险和医疗补助服务中心的数据,2022年美国医院护理服务的医疗保健支出增长至4.5万亿美元,预计还将继续增长。这笔巨额资金直接用于医院的基础设施投资,包括先进诊断设备和患者护理所需的耗材,从而巩固了该领域的市场领导地位。
测试地点段分析
在体外诊断市场中,即时检测(PoC)细分市场占据主导地位。其扩张主要得益于医疗保健分散化、患者自我管理以及对即时临床决策需求的强劲趋势。主要驱动因素包括将持续血糖监测纳入糖尿病管理标准诊疗流程,以及先进的CLIA豁免分子检测设备在临床上用于快速传染病诊断。美国公共卫生报告已明确记录了这一增长的统计数据。这一发展趋势正在从根本上重塑诊断格局,将关键检测从中心实验室直接转移到患者身边。随着技术的进步,PoC检测变得更加精准、经济和便捷,确保其作为现代响应式医疗保健服务基石的地位。
我们对市场的深入分析涵盖以下几个方面:
部分 | 子段 |
产品与服务 |
|
技术 |
|
应用 |
|
测试地点 |
|
最终用户 |
|
标本 |
|
可用性 |
|

Vishnu Nair
全球业务发展主管根据您的需求定制此报告 — 联系我们的顾问,获取个性化见解和选项。
体外诊断市场——区域分析
北美市场洞察
北美体外诊断市场占据主导地位,预计在评估期内将保持38.5%的市场份额。该市场的发展主要得益于先进的医疗基础设施和高昂的医疗支出。关键驱动因素包括精准医疗的广泛应用、对即时检测和居家检测需求的不断增长,以及肿瘤学和基因组学检测的强大研发管线。美国食品药品监督管理局 (FDA) 和医疗保险和医疗补助服务中心 (CMS) 的报销政策等监管框架塑造了市场格局,在促进创新的同时控制了成本。一个主要趋势是将人工智能和大数据分析集成到诊断平台中,以提高准确性和工作流程效率。此外,市场也面临整合,主要参与者正在收购创新型标准化医疗服务并扩大诊断能力,这主要是为了应对疫情凸显的手术积压问题,从而推动对高效实验室自动化的需求。
美国体外诊断市场以高创新性和严格的价值论证为特征,这主要得益于全球最大的医疗保健预算。一个主要趋势是向分散式检测的转变,这得益于美国医疗保险和医疗补助服务中心(CMS)对家用设备(例如连续血糖监测仪)的报销,旨在减少慢性病管理中的住院治疗。美国疾病控制与预防中心(CDC)强调快速分子诊断和基因组测序在抗菌素耐药性监测和疫情应对方面的公共卫生作用,并指导联邦采购。美国食品药品监督管理局(FDA)已批准多种体外诊断设备,例如ARUP Laboratories公司的AAV5 DetectCDx,这凸显了优先考虑用于靶向治疗的新型生物标志物的监管路径。
FDA批准的伴随诊断设备(体外和成像工具)
诊断名称 | 指示 - 样品类型 | 药品商品名 | 生物标志物 | 生物标志物(详情) | 批准日期 |
AAV5 DetectCDx(ARUP 实验室) | 甲型血友病患者 - 血浆 | 罗克塔维安 | 抗AAV5抗体 | 针对腺相关病毒5型(AAV5)病毒载体的抗体 | 2023年6月29日 |
Abbott RealTime IDH1(雅培分子诊断公司) | 骨髓增生异常综合征(MDS)——外周血或骨髓 | 蒂布索沃 | IDH1 | R132 突变(R132C、R132H、R132G、R132S 和 R132L) | 2023年10月24日 |
Abbott RealTime IDH1(雅培分子诊断公司) | 急性髓系白血病——外周血或骨髓 | 雷兹利迪亚 | IDH1 | R132 突变(R132C、R132H、R132G、R132S 和 R132L) | 2022年12月1日 |
安捷伦 Resolution ctDx FIRST 检测(Resolution Bioscience 公司) | 非小细胞肺癌(NSCLC)- 血浆 | 克拉扎蒂 | 克拉斯 | KRAS G12C | 2022年12月12日 |
来源:FDA 2025年12月
加拿大的体外诊断市场受其单一支付方、省级管理的医疗保健体系的影响,该体系优先考虑成本控制和公平获取医疗服务。一个主要趋势是联邦和省级政府加大投资,以解决疫情加剧的诊断积压问题。例如,安大略省政府在2022年3月的报告中指出,安大略省投资3.24亿美元用于扩建MRI和CT扫描能力,包括配套的实验室基础设施。采购很大程度上受到加拿大卫生技术评估机构(CADTH)开展的卫生技术评估的影响,该机构在各省采用相关技术前会评估其临床和成本效益。加拿大公共卫生机构致力于加强对传染病和抗菌素耐药性的国家监测,这催生了对标准化高通量实验室平台的需求。
亚太市场洞察
亚太地区体外诊断市场增长最快,预计在2026年至2035年预测期内将以6.8%的复合年增长率增长。推动市场增长的因素包括医疗保健投资的大幅增长、疾病负担的加重以及技术的普及应用。主要催化剂包括政府主导的大规模医疗基础设施建设,例如中国的“健康中国2030”计划以及印度和泰国推行的全民健康覆盖,这些举措显著提高了诊断的可及性。不断壮大的中产阶级、人口老龄化导致糖尿病和癌症高发以及日益增强的健康意识,都在推动私营部门的需求。市场趋势正朝着本地化生产方向发展,以降低对进口的依赖;同时,即时诊断和分子诊断在传染病管理中的快速普及以及数字化医疗的整合也在加速推进。
中国市场扩张由政府集中规划和执行,并通过“健康中国2023”战略推进,该战略优先发展早期筛查和预防保健,推动公共卫生项目的大规模采购。政府鼓励本土创新和“中国制造”自主研发,显著提升了迈瑞等本土企业在核心实验室领域的领先地位。国家药品监督管理局简化了关键检测产品的审批流程,包括肿瘤和传染病高通量检测平台。公共投资规模是推动市场扩张的关键因素。根据美国国家医学图书馆(NLM)2024年9月发布的研究报告,全国卫生总支出达到85327.49亿元人民币,并保持了较高的基线水平,直接用于在各县和社区卫生服务中心部署诊断设备。
受人口、经济和政策因素的推动,印度体外诊断市场有望实现持续的长期增长。人口老龄化、可支配收入增加以及生活方式相关疾病的日益普遍,都推动了对常规和预防性诊断检测的需求增长。患者对早期检测态度的转变、更广泛的保险覆盖以及即时诊断技术的日益普及,进一步提升了城市和半城市地区的检测量。在供应方面,印度投资局2021年6月发布的报告指出,印度政府推出的生产关联激励计划2.0是一项旨在加强国内体外诊断制造能力并降低进口依赖的结构性催化剂。该计划的目标企业是本地制造收入达到或超过500亿卢比的公司,旨在打造具有全球竞争力的印度制造商,使其能够融入国际价值链并扩大先进诊断技术的应用规模。
欧洲市场洞察
欧洲市场已趋于成熟,不断发展,其特点是监管力度强劲、成本控制压力大,以及大力推进一体化医疗保健。体外诊断监管的实施是主导因素,提高了合规门槛,有利于拥有完善质量体系的大型成熟企业,但也可能阻碍小型新进入者的创新。关键驱动因素包括该地区人口老龄化、需要监测的慢性病患病率不断上升,以及为改善治疗效果和降低长期成本而对个性化医疗和早期诊断的战略性关注。欧盟委员会的“欧盟健康计划”(EU4Health)是一项重要的需求催化剂,旨在通过资金支持加强包括跨境健康威胁在内的医疗卫生体系。
德国体外诊断市场由其庞大的法定医疗保险体系和密集的医院及独立实验室网络所主导。人口老龄化以及对早期诊断和门诊治疗的高度重视是推动市场增长的结构性因素,也带动了检测量的增加。《数字医疗法》和《医院未来法》的实施是关键的催化剂,为数字基础设施建设提供了数十亿欧元的资金,强制要求将诊断数据整合到电子病历中,从而刺激了对联网设备的需求。德国联邦统计局2023年4月发布的报告显示,2021年德国医疗保健支出达到4741亿欧元,持续增长,为诊断服务和采购提供了充足且不断扩大的资金基础。
英国体外诊断市场在脱欧后由英国药品和保健产品监管局 (MHRA) 监管,并采用一套独特的监管框架。推动市场增长的主要动力是英国国家医疗服务体系 (NHS) 的长期计划,该计划优先考虑癌症早期诊断和社区护理,从而引导市场需求转向快速诊断中心和即时检测。英国世界领先的基因组医学服务为先进的分子诊断和伴随诊断创造了高价值的市场空间。NHS 诊断活动的关键统计指标是择期手术的积压情况。NHS 英格兰分部 2024 年 2 月的报告显示,等待关键诊断检测超过 6 周的患者人数高达 334,900 人,凸显了持续的高需求和系统压力,这也促使 NHS 不断投资和采购诊断能力,以缩短患者的等待时间。
体外诊断市场主要参与者:
- 罗氏诊断(瑞士)
- 雅培实验室(美国)
- 丹纳赫公司(贝克曼库尔特等)(美国)
- 西门子医疗(德国)
- 赛默飞世尔科技(美国)
- 强生公司(Ortho Clinical Diagnostics)(美国)
- Sysmex公司(日本)
- 贝克顿·迪金森公司(BD)(美国)
- 生物梅里埃(法国)
- Quest Diagnostics(美国)
- 格里福尔斯(西班牙)
- Bio-Rad Laboratories(美国)
- 凯杰(德国)
- 迈瑞(中国)
- Hologic(美国)
- Diasorin(意大利)
- 深圳迈瑞生物医疗电子(中国)
- 积水医疗(日本)
- Ortho Clinical Diagnostics(美国)
- 韦尔芬(西班牙)
- 公司概况
- 商业战略
- 主要产品
- 财务业绩
- 关键绩效指标
- 风险分析
- 最新进展
- 区域影响力
- SWOT分析
- 罗氏诊断凭借其从诊断到治疗的一体化战略,在全球体外诊断市场占据主导地位。该公司大力投资于高通量实验室自动化和数据管理软件,以简化临床工作流程。一项关键举措是将体外诊断与数字健康平台融合,利用人工智能解读其肿瘤、心脏病和传染病产品组合中的复杂数据,从而支持个性化医疗决策。该公司预计,2024年诊断产品总销售额将增长4%。
- 雅培公司是分散式体外诊断市场的领军企业,尤其擅长快速即时检测和便携式检测。其战略重点是通过手持式 i-STAT 和可扩展的 Alinity 系列等平台,实现诊断的普及化。雅培积极拓展市场,提供高通量检测产品,确保在传统实验室之外,从诊所到社区等场所,都能在数分钟内获得临床级别的检测结果。2024 年,公司总销售额达 420 亿美元。
- 丹纳赫公司凭借其在体外诊断市场的垂直整合优势,旗下拥有贝克曼库尔特、徕卡生物系统和赛菲德等运营公司。丹纳赫业务系统致力于推动持续创新和卓越运营。在战略层面,该公司专注于打造从样本制备、组织病理学到分子诊断的端到端解决方案,尤其通过其赛菲德GeneXpert系统,拓展了医院获得性传染病和呼吸道疾病的快速分子检测。
- 西门子医疗在体外诊断市场中扮演着举足轻重的角色,尤其注重实验室效率、互联互通和可持续发展。其Atellica解决方案可实现高通量免疫分析和临床化学检测的自动化和整合。一项核心战略举措是构建一个数字化互联的诊断生态系统,将体外诊断数据与影像和治疗信息整合到其syngo虚拟驾驶舱平台中,从而支持医疗系统实现全面的患者管理和运营智能。
- 赛默飞世尔科技通过提供支撑全球检测的关键仪器、试剂和耗材,巩固了其在体外诊断市场的基石地位。其战略的核心在于凭借其丰富的产品组合,成为临床实验室和体外诊断试剂生产商不可或缺的合作伙伴。公司专注于支持从研究和临床试验检测到大规模商业化检测的整个开发周期,尤其是在免疫诊断和分子诊断领域。
以下是全球市场主要参与者的名单:
全球体外诊断市场高度集中,由来自美国、欧洲和日本的跨国公司主导。这些行业领导者通过大量的研发投入和战略收购来拓展检测产品组合,并进军高增长的新兴市场,尤其是在亚洲。一个关键趋势是将人工智能和数据分析技术整合到诊断平台中,以实现精准医疗。与此同时,受疫情影响,各公司正着力开发即时检测和快速诊断技术。为了保持市场主导地位,企业正与科技公司和医疗服务提供商建立合作关系,打造一体化的诊断解决方案,同时还要应对各地日益严格的监管审查。例如,希森美康集团位于印度的新生产基地将于2025年4月全面投产,并推出“印度制造”系列产品。
体外诊断市场企业格局:
最新发展
- 2025 年 6 月, Fujirebio宣布收购 Plasma Services Group,巩固了其作为 IVD 和生命科学行业关键和高质量生物原材料供应商的地位。
- 2025年2月, Aiforia Technologies Plc宣布已成功获得体外诊断医疗器械法规(IVDR)认证。与此同时,该公司推出了三款获得CE-IVD认证的全新人工智能模型,用于乳腺癌和前列腺癌的诊断。
- 2024年1月, ELITechGroup宣布推出获得CE-IVDR认证的GI Bacterial PLUS ELITe MGB试剂盒,进一步拓展其体外诊断产品组合。该公司计划在下一季度推出三款涵盖所有胃肠道感染的试剂盒。
- Report ID: 1354
- Published Date: Jan 30, 2026
- Report Format: PDF, PPT
- 探索关键市场趋势和洞察的预览
- 查看样本数据表和细分分析
- 体验我们可视化数据呈现的质量
- 评估我们的报告结构和研究方法
- 一窥竞争格局分析
- 了解区域预测的呈现方式
- 评估公司概况与基准分析的深度
- 预览可执行洞察如何支持您的战略
探索真实数据和分析
常见问题 (FAQ)
免费样本包括当前和历史市场规模、增长趋势、区域图表和表格、公司概况、按细分市场的预测等内容。
联系我们的专家
版权所有 © 2026 Research Nester。保留所有权利。




