黏多醣貯積症(MPS)治療市場展望:
2025年,黏多醣貯積症(MPS)治療市場規模為44億美元,預計到2035年底將達到110億美元,在預測期(即2026-2035年)內,複合年增長率為10.8%。 2026年,黏多醣貯積症(MPS)治療產業的規模估計為48億美元。
黏多醣貯積症治療市場的成長因素可歸納為一個核心策略架構。這些因素包括治療方法的進步、在研療法的創新、合適的孤兒藥立法、經濟模式以及診斷流程的最佳化。根據MDPI於2025年3月發表的一篇文章,全球約27.4萬項臨床試驗中,約有2%在非洲進行;2022年,超過2000種基因療法成功應用於心血管疾病、血液疾病、神經系統疾病和腫瘤等疾病的治療。這有力地表明,治療領域的研究投入正在增加,這也使得該市場在國際上獲得了更高的關注。
此外,新興市場的擴張、產業整合的策略性措施、國家衛生研究院的設立、行政審批以及國家罕見疾病組織的建立,也推動了全球黏多醣貯積症治療市場的發展。根據美國國家醫學圖書館(NLM)2022年10月的文章,目前已發現約6000至8000種罕見疾病,其中約80%為遺傳性疾病,50%至75%為兒童期發病。此外,歐盟法規將此類疾病定義為在歐洲每10萬名患者中影響超過50人的嚴重疾病,而美國的《孤兒藥法案》則將其定義為在美國影響超過20萬人的疾病,這些因素都進一步刺激了市場需求。
黏多醣貯積症(MPS)治療市場-成長驅動因素與挑戰
成長驅動因素
- 創新藥物遞送技術:這些技術旨在有效地將結合或包裹的治療藥物作為載體,使其高效且精準地到達作用部位,從而推動全球黏多醣貯積症治療市場的發展。根據美國國家醫學圖書館 (NLM) 2023 年 6 月發表的一篇文章,約 30% 的綜合醫療實體和近 50% 的先進藥物化合物可用於產品生產,而這些藥物本身俱有疏水性。在這種情況下,建議採用液態載體系統來提高近年來迅速增長的低水溶性藥物的生物利用度。
- 適用生物標記的增加:這些生物標記能夠有效測量體內存在的指標,這些指標對於個人化治療、風險評估、預後判斷和疾病診斷至關重要,從而推動了黏多醣貯積症治療市場的發展。根據2022年6月發布的JTO報告,一項針對17,513名患者的臨床研究記錄了83,064次基因組生物標記檢測。在所有參與者中,28.3%至68.1%接受了生物標記檢測,這為不同國家患者的整體市場前景帶來了正面影響。
- 新生兒篩檢計畫的擴展:這些計畫至關重要,因為它們能夠在症狀出現之前識別出患有危急且可治療疾病的新生兒,從而促進黏多醣貯積症治療市場的發展。此外,這也有助於及時幹預,克服或減輕長期健康問題和發育風險,從而保障兒童的健康成長。根據美國國家醫學圖書館 (NLM) 2023 年 5 月的文章,美國的新生兒篩檢計畫已由推薦統一篩檢組 (RUSP) 制定了州級指導方針,該篩檢組包含 26 種次要疾病和 35 種核心疾病,適用於多種疾病的診斷,從而提升了整體市場。
2024年細胞和基因療法的定量結果將推動黏多醣貯積症治療市場的發展
輸出 | 數位 |
科學家支持 | 228 |
支持的項目 | 144 |
人力(初級研究員/高級研究員/研究助理等)支持 | 307 |
專利申請/已授權專利 | 7 |
技術/產品開發 | 6 |
組織的研討會/培訓項目 | 5 |
資料來源:生物技術部
針對罕見疾病和未確診疾病的大規模基因組計畫正在推動MPS治療市場的發展。
國家 | 項目名稱 | 樣本量 | 專案年份 | NGS技術 |
澳洲 | 基因組學健康未來使命 | 20萬 | 2018年至今(預計2028年完工) | 根據項目情況而定 |
加拿大 | 罕見疾病基因體學合作 | 全國 | 2019年至今 | 根據項目情況而定 |
中國 | 精準醫療計劃 | 10萬至1億 | 2015年至今(預計2030年完工) | 全基因組定序 |
法國 | 法國基因組醫學2025 | 每年234,000 | 2015年至今(預計2025年完工) | 全基因組定序/全外顯子定序/RNA |
日本 | 基因組醫學聯盟 | 全國 | 2018年至今 | 全基因組定序 |
英國 | 我們未來的健康 | 5,000,000 | 2020年至今 | 根據項目情況而定 |
我們 | 美國國立衛生研究院未確診疾病項目 | 全國 | 2008年至今 | WES/微陣列 |
資料來源:美國國家醫學圖書館,2022年10月
挑戰
- 生物製劑供應鏈的複雜性:基因療法和酵素替代療法 (ERT) 的生產環節極其複雜,依賴於客製化的生產設施和對關鍵原材料的精細化國際供應鏈,這對黏多醣貯積症 (MPS) 的治療市場造成了負面影響。此外,從工廠到患者,有效維持對溫度要求較高的生物製劑的冷鏈運輸,在物流方面成本高且極具挑戰性。而且,任何類型的干擾,從地緣政治問題到單一工廠的品質控制風險,都可能導致國際生產停滯。
- 在極小樣本人群中展現價值:在小樣本人群中開展有針對性的、穩健的臨床試驗,在倫理和科學上都極具挑戰性,這阻礙了全球粘多醣貯積症治療市場的發展。另一方面,健康技術評估機構(HTA)常常認為單臂對照試驗和基於自然數據的試驗不足以提供充分的證據,而生產商也難以提供高品質的統計證據,這迫使他們依賴終點指標和基於患者的結局,從而在全球市場發展中造成了缺口。
黏多醣貯積症(MPS)治療市場規模及預測:
| 報告屬性 | 詳細資訊 |
|---|---|
|
基準年 |
2025 |
|
預測年份 |
2026-2035 |
|
複合年增長率 |
10.8% |
|
基準年市場規模(2025 年) |
44億美元 |
|
預測年份市場規模(2035 年) |
110億美元 |
|
區域範圍 |
|
黏多醣貯積症(MPS)治療市場區隔:
給藥途徑分段分析
預計到2035年底,靜脈注射(IV)療法在黏多醣貯積症治療市場中將佔據77.3%的最大份額。該領域的成長主要歸功於其能夠補充電解質和體液、恢復血液容量,並確保藥物的有效輸送。根據美國國家癌症研究所2025年5月發表的一篇文章,靜脈注射維生素C的劑量可超過500毫克,與口服相比,這會導致血液中抗壞血酸的濃度更高。此外,2022年6月《臨床微生物學與感染》雜誌的報告指出,目前有多種靜脈注射抗菌藥物可供選擇,其劑量方案各不相同,其中氟氯西林佔23%,哌拉西林佔17.2%,萬古黴素佔11.6%,芐青黴素佔11%,這些都有利於該領域的增長。
最終用戶細分分析
在黏多醣貯積症(MPS)治療市場中,專科診所預計將在預測期結束時佔據第三大市場。 MPS治療的特殊性極大地推動了該細分市場的發展,MPS治療需要包括代謝疾病專家、神經科醫生和遺傳學家在內的多學科團隊合作。此外,專科診所還承擔著複雜的靜脈生物製劑輸注、診斷以及確保患者協調持續管理的中心職能。同時,專科診所在不良事件處理和方案製定方面也至關重要,因此成為醫保支付方和製藥公司最青睞的合作夥伴。
治療段分析
在預測期內,酵素替代療法(ERT)預計將在黏多醣貯積症治療市場中佔據第二大份額。此細分市場的成長主要得益於其對有效治療遺傳性酵素缺乏症和溶小體貯積症的重要性,其作用機制是透過補充缺失或不足的酶,減少毒性底物的累積。為此,一項針對221名受試者的臨床研究於2025年7月發表在《分子遺傳學與代謝》期刊。在研究中,被誤診的受試者接受了ERT治療,治療持續時間為8.7年,而平均治療暴露時間為11.7年,相當於2197患者年。
我們對市場的深入分析涵蓋以下幾個面向:
部分 | 子段 |
給藥途徑 |
|
最終用戶 |
|
治療 |
|
類型 |
|
分銷管道 |
|
治療類型 |
|

Vishnu Nair
全球業務發展主管根據您的需求自訂本報告 — 與我們的顧問聯繫,獲得個人化的洞察與選項。
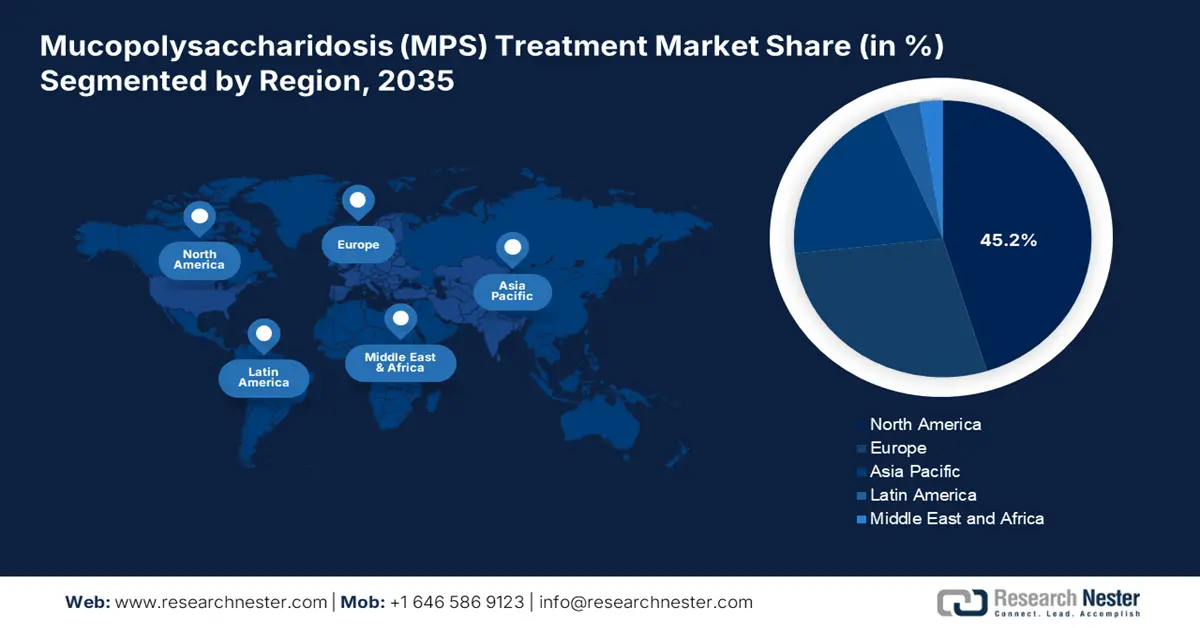
黏多醣貯積症 (MPS) 治療市場—區域分析
北美市場洞察
預計到2035年底,北美黏多醣貯積症治療市場將佔據45.2%的最高市場。該地區市場的成長主要歸功於一個協同生態系統的存在,該系統能夠有效地將高成本的藥物研發成果商業化、批准並為其提供資金。這包括不斷上漲的藥品價格、強勁的風險投資以及完善的保險體系。正如美國國家醫學圖書館(NLM)2023年2月的文章所述,美國食品藥物管理局(FDA)已批准了最新的孤兒藥和非孤兒藥,分別耗資218,872美元和12,798美元,從而推動了該地區市場的發展。
由於聯邦法規、多方付費保險體系、醫療補助和醫療保險的報銷機制以及激烈的市場競爭等因素的複雜相互作用,美國黏多醣貯積症治療市場正顯著成長。此外,美國國家醫學圖書館 (NLM) 2023 年 11 月發表的文章指出,截至 2023 年,聖菲利波症候群的經濟負擔估計已達 20 億美元,這極大地推動了美國市場的發展。此外,自患童出生起,每個家庭的負擔增加了 800 萬美元。
由於加拿大藥品與衛生技術機構 (CADTH) 進行的可負擔性評估、加拿大衛生部批准審查和上市,以及隨後由泛加拿大製藥聯盟 (pCPA) 管理的談判,加拿大黏多醣貯積症治療市場也呈現上升趨勢。此外,2025 年 4 月美國國家醫學圖書館 (NLM) 的文章指出,加拿大衛生部長宣布了最新的國家罕見疾病藥物策略,並撥款 15 億美元,為期三年多。該策略旨在進一步優化罕見疾病治療的可近性,其中包括向各地區和省份提供近 14 億美元的資金,以增加藥物供應。
北美仿製藥審批帶來的歷史性節省
年 | 總節省金額(十億美元) | 首款仿製藥節省金額(十億美元) |
2018 | 17.8 | 4.0 |
2019 | 24.8 | 9.4 |
2020 | 10.7 | 1.8 |
2021 | 16.6 | 1.7 |
2022 | 18.9 | 5.2 |
資料來源: FDA,2024年10月
亞太市場洞察
預計亞太市場將在預測期內成為成長最快的地區。該地區市場的發展主要受人口基數、確診和接受治療的患者數量、診斷能力的提升以及將價格昂貴的孤兒藥納入國家醫保體系的有效談判等因素的推動。此外,2022年4月發布的亞太醫療報告顯示,該地區在全民健康覆蓋(UHC)方面的投資高達2.5兆美元,而這筆資金以往不足以涵蓋高品質技術的普及應用。同時,檢測的普及和分散化正在推動個人化醫療模式的出現,這些都對市場成長產生了積極影響。
由於國家醫保藥品目錄(NRDL)的實施、標準化折扣機制、按量計價模式以及透過合作實施的策略,中國市場正日益受到關注。根據2024年9月發表在《罕見疾病孤兒網雜誌》(Orphanet Journal of Rare Diseases)上的一篇文章,一項針對180名黏多醣貯積症(MPS)患者的臨床研究評估了該疾病的負擔。研究顯示,住院治療的直接醫療費用為81,086.7元人民幣,佔總費用的63.7%,從而有效促進了中國市場的整體成長。
由於韓國擁有完善的衛生技術評估體系、成本效益分析、政府更多地採用風險分擔協議(RSA)以及製造商能夠提供真實世界證據,韓國的黏多醣貯積症治療市場也在蓬勃發展。在這方面,美國國家生物技術資訊中心(NCBI)2024年5月發表的文章指出,自韓國啟動衛生技術重新評估以來,已有262例病例成功完成重新評估,其中126例(佔48.1%)涉及最初不在國民健康保險(NHI)覆蓋範圍內的醫療服務。
歐洲市場洞察
在預測期內,歐洲在黏多醣貯積症治療市場上預計將佔據相當大的市場。該地區市場的成長主要得益於歐洲藥品管理局 (EMA) 的集中式行政審批、定價和報銷政策以及合適的醫療和科研儀器的採購。根據美國國家醫學圖書館 (NLM) 2024 年 9 月發表的一篇文章,該地區的藥品審批系統已批准 14 種藥物,英國則批准了 12 種。此外,就研發狀態而言,該地區有 3 種藥物正在研發中,而英國則有 5 種,因此具備提升市場規模的潛力。
由於《藥品市場改革法案》(AMNOG)的實施、合適的對照療法、國家法定醫療保險基金協會以及可靠的健康和臨床經濟數據,德國的黏多醣貯積症治療市場也不斷成長。根據《多發性硬化症及相關疾病》雜誌2024年8月發表的一篇文章,德國估計有29,604名多發性硬化症(MS)患者開始接受治療,其中29.6%的患者積極遵循了HHAE策略。此外,2022年德國採用此策略的患者人數增加了14%,顯示治療師對市場成長的重要性。
由於法國國家衛生署(HAS)下屬的透明度委員會提供的評級和評估、較高的保費以及廣泛的報銷政策,法國的黏多醣貯積症(MPS)治療市場正在蓬勃發展。根據世界衛生組織2024年4月的報告,法國的補充醫療保險(CHI)已為近95%的人口優化了財務狀況。這是因為低收入家庭可以免費使用補充醫療保險,或獲得補貼,為市場繁榮創造了巨大的機會。
2023年歐洲醫療科學儀器進出口
國家 | 出口(美元) | 進口(美元) |
比利時 | 2000萬 | 430萬 |
西班牙 | 1560萬 | - |
英國 | 1510萬 | 1320萬 |
德國 | 1380萬 | 1.53億 |
愛爾蘭 | 1070萬 | 2930萬 |
義大利 | 950萬 | 2460萬 |
波蘭 | 900萬 | 450萬 |
俄羅斯 | 750萬 | 130萬 |
資料來源: OEC,2025年8月
黏多醣貯積症(MPS)治療市場主要參與者:
- BioMarin製藥公司(美國)
- 公司概況
- 商業策略
- 主要產品
- 財務業績
- 關鍵績效指標
- 風險分析
- 最新進展
- 區域影響力
- SWOT分析
- 賽諾菲(法國)
- Regenxbio公司(美國)
- UCB SA(比利時)
- Inventiva Pharma(法國)
- ArmaGen公司(美國)
- Denali Therapeutics Inc.(美國)
- Sangamo Therapeutics, Inc.(美國)
- Abeona Therapeutics Inc.(美國)
- 韓國綠十字公司
- GC製藥(韓國)
- Amicus Therapeutics, Inc.(美國)
- M6P Therapeutics(美國)
- Passage Bio, Inc.(美國)
- Sarepta Therapeutics, Inc.(美國)
國際黏多醣貯積症 (MPS) 治療市場呈現寡占格局,主要由創新生物技術公司和專業製藥巨頭主導。此外,值得關注的策略性舉措包括持續投入研發資金,開發尖端療法,例如可穿透中樞神經系統的酵素替代療法 (ERT) 和基因療法,旨在滿足日益增長的神經系統症狀治療需求。同時,各公司積極爭取孤兒藥資格認定,以獲得更高的定價和市場獨佔權;例如,武田製藥和 BioMarin 已利用各自成熟的商業設施在全球範圍內推出產品,從而推動了全球粘多醣貯積症 (MPS) 治療市場的擴張。
以下是全球市場主要參與者的名單:
最新動態
- 2025 年 2 月, Ultragenyx Pharmaceutical Inc.宣布,美國 FDA 已批准其生物製品許可申請 (BLA),以有效尋求提高 UX111 AAV 基因療法作為 A 型 Sanfilippo 綜合徵患者可能治療方法的認可度。
- 2024 年 11 月, PTC Therapeutics, Inc.宣布其基因療法已獲得美國 FDA 批准,該療法非常適合用於治療 AADC 缺乏症,是美國首個獲準直接向大腦給藥的基因療法。
- Report ID: 5215
- Published Date: Sep 26, 2025
- Report Format: PDF, PPT
- 探索关键市场趋势和洞察的预览
- 查看样本数据表和细分分析
- 体验我们可视化数据呈现的质量
- 评估我们的报告结构和研究方法
- 一窥竞争格局分析
- 了解区域预测的呈现方式
- 评估公司概况与基准分析的深度
- 预览可执行洞察如何支持您的战略
探索真实数据和分析
常见问题 (FAQ)
黏多醣貯積症治療 市场报告范围
免費樣本包含目前與歷史市場規模、成長趨勢、區域圖表與表格、公司概況、依細分市場的預測等內容。
聯絡我們的專家




