膠質瘤診斷與治療市場展望:
2025年,膠質瘤診斷和治療市場規模為38.1億美元,預計到2035年將超過62.7億美元,在預測期(即2026年至2035年)內,複合年增長率將超過5.1%。 2026年,膠質瘤診斷和治療產業的規模預計為39.8億美元。

根據2023年《腦與脊椎期刊》的報告,膠質母細胞瘤是一種高度侵襲性的神經膠質瘤,也是最常見的惡性中樞神經系統(CNS)腫瘤之一。其全球發生率為每10萬人3.19例。美國國家醫學圖書館(NLM)2023年1月的研究顯示,全球膠質瘤的發生率高達42.8%。因此,醫療系統亟需配備完善的基礎設施並支援各種治療方法,這推動了該領域的顯著成長。這些致命腦部惡性腫瘤發生率的逐步上升引起了公共和私人醫療機構的關注,促使它們增加對膠質瘤診斷和治療市場的投資。
然而,近年來,膠質母細胞瘤(GBM)等晚期膠質瘤的初始治療費用顯著更高。根據2024年3月發表於《神經腫瘤學與神經外科腫瘤學》雜誌的一篇文章的估算,每位新確診的GBM患者初始治療費用為95,377美元。此後,患者平均每月需花費18,053美元,平均存活期為5.9個月,使其成為治療費用最高的疾病之一。因此,膠質瘤的診斷和治療市場正在不斷改進產品線,以提供更優惠的定價,縮小經濟差距,並提高治療普及率。
基於此,2021年發表於《JCO全球腫瘤學》期刊的文章介紹了一種對印度而言相對經濟實惠的治療方案——替莫唑胺聯合放療,該方案在降低成本和提高療效方面分別實現了90.0%和80.0%的提升。這促進了新型混合型和可近性治療方案的研發,使該領域更加多元化,並創造了更大的投資空間。此外,這也鼓勵全球先驅者投入大量研發,以尋找最合適的解決方案,從而提高膠質瘤診斷和治療市場的可用性。
歐洲、北美和中國(美國除外)膠質母細胞瘤治療費用(2024 年)
治療類型 | 每位患者的平均費用(美元) |
手術切除 | 10,042.0 |
放射治療 | 6,777.0 |
聯合治療(手術、放射治療和化學治療) | 62,602.0 |
資料來源:美國國家醫學圖書館研究
關鍵 膠質瘤的診斷和治療 市場洞察摘要:
區域亮點:
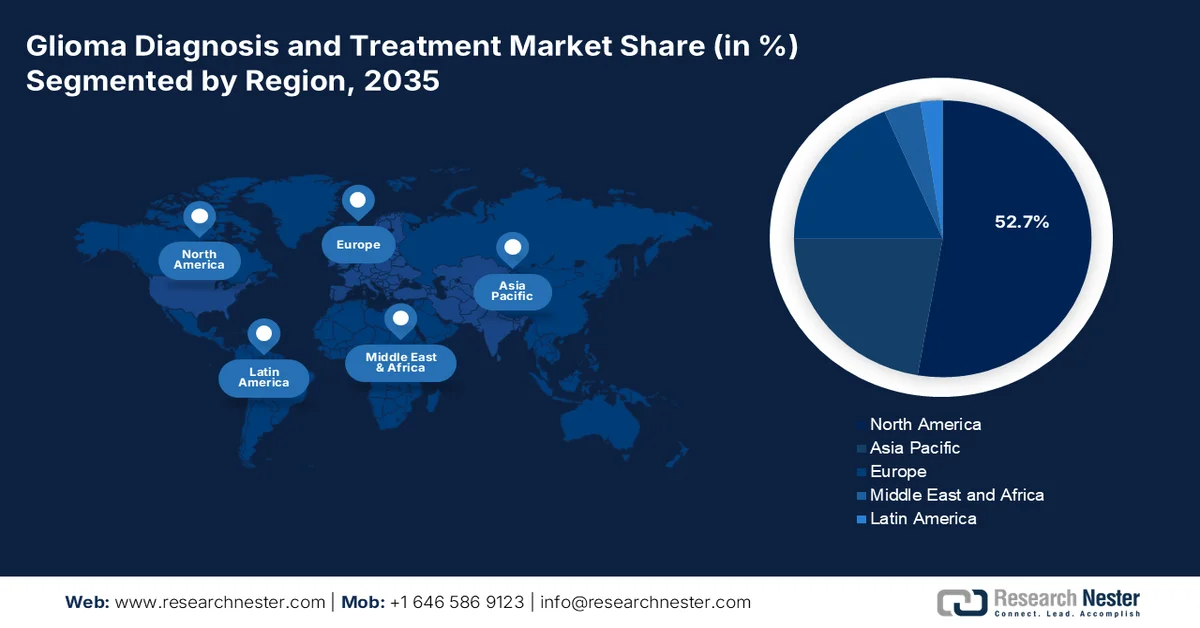
- 預計到 2035 年,北美將佔據膠質瘤診斷和治療市場的主導地位,收入份額超過 52.7%,這得益於完善的醫療保健基礎設施和強大的分銷網絡,以及監管方面的進步。
- 預計到 2035 年,亞太地區將迎來顯著成長,這得益於精準醫療的快速發展以及為應對膠質瘤死亡率上升而不斷增加的投資。
細分市場洞察:
- 由於醫療基礎設施的擴張、可及性的提高以及強有力的機構資金支持,到 2035 年,醫院和診所部門將佔膠質瘤診斷和治療市場 70.8% 以上的份額。
- 預計在預測期內,原發性腫瘤部分將佔最大份額,這主要歸因於星狀細胞瘤、室管膜瘤和少突膠質細胞瘤的高發生率和侵襲性進展。
主要成長趨勢:
- 對腦腫瘤的關注與投入日益增加
- 檢測和治療方法的創新
主要挑戰:
- 類型和市場需求的多樣性
- 猶豫不決與較高的復發率
主要參與者:安捷倫科技公司、沃特世公司、島津公司、珀金埃爾默公司、布魯克公司、ACD/Labs、SepSolve Analytical。
全球 膠質瘤的診斷和治療 市場 預測與區域展望:
市場規模及成長預測:
- 2025年市場規模: 38.1億美元
- 2026年市場規模: 39.8億美元
- 預計市場規模:到2035年將達到62.7億美元
- 成長預測:複合年增長率 5.1%(2026-2035 年)
關鍵區域動態:
- 最大區域:北美(到2035年佔52.7%的份額)
- 成長最快的地區:亞太地區
- 主要國家:美國、德國、日本、英國、法國
- 新興國家:中國、印度、日本、韓國、德國
Last updated on : 25 February, 2026
膠質瘤診斷和治療市場—成長驅動因素和挑戰
成長驅動因素
對腦腫瘤的關注和投資日益增長:腦腫瘤與腦癌的密切關聯促使全球各地的管理機構將廣泛存在的膠質瘤診斷和治療市場列為優先事項。多個公共機構的努力正在確保不斷增長的資金流入,從而推動該領域的發展。例如,2022年3月,《綜合支出法案》增加了對美國腦腫瘤專案機構的撥款。這使得美國衛生高級研究計畫署(ARPA-H)、美國國立衛生研究院(NIH)和美國國家癌症研究所(NCI)分別獲得了10億美元、450億美元和70億美元的撥款。這些措施也鼓勵私人企業投入資源。
- 檢測和治療方法的創新:人們對早期及先進檢測和介入益處的認識不斷提高,推動了膠質瘤診斷和治療市場的需求成長。持續的研發和發現正以改善患者預後和治療反應為動力,推動該領域呈指數級增長。根據世界衛生組織2023年10月發布的報告,在兒童腦腫瘤中,膠質瘤亞型藥物研發數量最多(156種),其中40.0%正在進行II期臨床試驗。在總共187種新療法中,膠質瘤佔35.0%,包括70種口服藥物和24種兒童適用藥物。
挑戰
類型和市場需求的多樣性:這種疾病包含多種複雜的突變類型和特徵,可能無法透過現有的膠質瘤診斷和治療方案進行有效治療。此外,許多膠質瘤患者無症狀且具有異質性,導致早期難以發現和乾預,進而影響現有療法的療效。為了緩解這些問題,需要進行更深入的研究,引入客製化和研發的療法和策略。
- 由於復發率較高,治療方案的選擇往往受到阻礙:血腦障壁常常阻礙口服給藥,迫使醫師採取其他更積極的治療手段。尤其對於兒童患者而言,這些方法會帶來嚴重的健康影響。此外,抗藥性腫瘤的出現也使得患者難以耐受和應對長期治療。這些因素共同導致家長或家庭不願接受這些療法,限制了膠質瘤診斷和治療市場的份額。
膠質瘤診斷及治療市場規模及預測:
| 報告屬性 | 詳細資訊 |
|---|---|
|
基準年 |
2025 |
|
預測年份 |
2026-2035 |
|
複合年增長率 |
5.1% |
|
基準年市場規模(2025 年) |
38.1億美元 |
|
預測年份市場規模(2035 年) |
62.7億美元 |
|
區域範圍 |
|
膠質瘤診斷和治療市場細分:
最終用戶細分分析
在膠質瘤診斷和治療市場,預計到2035年,醫院和診所將佔超過70.8%的收入份額。基礎設施投入的增加,以及醫療服務可近性的提高(尤其是在已開發國家),正在推動這一領域的發展。美國醫院協會在2022年8月發布的報告顯示,醫院每年為社區帶來的經濟效益高達1,100億美元。許多臨床研究表明,患者早期入院接受治療可獲得更好的治療效果,這使得醫院成為居民可靠的就醫選擇。此外,醫療必需品的便利供應和政府補貼也促使人們加大對醫療機構的投資,並激勵企業將醫療網絡納入其主要分銷管道。
類型細分分析
就類型而言,原發性腫瘤預計將在預測期內佔據膠質瘤診斷和治療市場的最大份額。此亞型的高發生率是該細分市場的主要成長因素。原發性膠質瘤主要包括星狀細胞瘤、室管膜瘤和少突膠質細胞瘤,根據美國國家醫學圖書館(NLM)的數據,到2023年,它們的全球發生率分別為20.3%、3.2%和3.9%。另一份來自同一來源的報告指出,膠質母細胞瘤(一種星狀細胞瘤)的平均存活期為9個月。這表明,由於該細分市場的高發病率和高死亡率,其成長勢頭強勁。此外,這些疾病的侵襲性和快速進展使其成為醫療系統的首要關注點。
我們對全球膠質瘤診斷和治療市場的深入分析涵蓋以下幾個方面:
最終用戶 |
|
類型 |
|
診斷 |
|
治療 |
|
年級 |
|
地點 |
|

Vishnu Nair
全球業務發展主管根據您的需求自訂本報告 — 與我們的顧問聯繫,獲得個人化的洞察與選項。
膠質瘤診斷與治療市場—區域分析
北美市場洞察
預計到2035年,北美在膠質瘤診斷和治療市場將佔超過52.7%的市場。該地區的醫療保健產業擁有完善的基礎設施和強大的供應鏈,這提高了該領域的可及性和可用性,確保了業務的穩定發展。這也吸引了眾多外國製藥巨頭參與其中。例如,2024年4月,Telix Pharmaceuticals公司獲得了美國FDA對其在研膠質瘤成像產品TLX101-CDx的快速通道資格認定。該公司選擇與北美領先的商業化和生產企業PharmaLogic Holdings Corp合作,負責該產品在北美地區的分銷。由此可見,本地支持也對該市場的發展起了推動作用。
除了完善的監管框架外,美國膠質瘤診斷和治療市場還受益於不斷增長的醫療保健支出和許多研究機構。過去十年,美國已建立起一套高效的工具庫和卓越的學術網絡,用於開展卓有成效的大規模臨床試驗,從而推動了許多發現。例如,2023年6月,加州大學洛杉磯分校(UCLA)參與了一項國際隊列研究,旨在評估vorasidenib的療效。該評估結果幫助這種標靶療法獲得了全球認可,因為它能夠減緩膠質瘤的進展,且副作用和神經功能缺損更少。這不僅有助於藥物的審批流程,也有助於製藥公司改善其產品線,使其更具市場競爭力。
加拿大兒童膠質瘤(GMB)發病率的突然上升,促使該國更加關注膠質瘤的診斷和治療市場。這種疾病對年輕一代的影響及其與腦癌的關聯引起了國家衛生部門的關注,並推動了該領域的穩定資金流入。例如,2023年5月,一個科學家團隊獲得了5萬美元的資助,為腦癌高風險的兒童膠質瘤患者開發量身定制且毒性更小的治療和識別方法。研究團隊認為,這項計畫有望建立一套新型的、按年齡分層的、經濟高效的分子檢測指南。這些資金將為該領域未來的研究提供資金支持。
亞太市場洞察
預計亞太地區在預測期內膠質瘤診斷和治療市場將呈現顯著成長。精準醫療的卓越發展和快速進步對該領域起到了積極的推動作用。根據 Research Nester 估計,到 2035 年底,亞太地區的精準腫瘤學產業預計將在全球收入中佔 43.0% 的最高份額。同時,該地區也預計在同一時期佔據精準醫療業務 30.5% 的顯著份額。此外,由於膠質母細胞瘤 (GBM) 導致的低收入和中等收入國家死亡率不斷上升,促使各國政府建設完善的基礎設施,推動了該領域的需求。
印度正致力於降低膠質瘤診斷和治療的可及性並提高其價格可負擔性。這個新興的醫藥領域正透過學術創新和政府合作,為該領域的臨床發現奠定堅實的基礎。例如,2024年12月,印度衛生與家庭福利部國務部長宣布啟動由生物技術產業研究協助委員會(BIRAC)監督的CAR-T細胞療法研究計畫。這些項目旨在開發價格合理的細胞療法產品,例如免疫療法,以對抗包括膠質母細胞瘤在內的多種癌症。
中國也面臨膠質母細胞瘤(GBM)發生率持續上升的困境,促使政府加強對膠質瘤診斷和治療市場的投資。根據美國國家醫學圖書館(NLM)2022年9月發表的一項研究,該疾病的總體存活期為10.6個月,平均發病年齡為57±14歲。儘管發病率較低,但中國仍計劃透過醫療體系充足的資源供應來提高生存率,從而保障老年族群的健康。例如,2020年5月,中國國家藥品監督管理局(NMPA)批准再鼎醫藥和諾華醫療的聯合方案Optune+替莫唑胺上市,用於治療復發性和新發GBM病例。
膠質瘤診斷與治療市場參與者:
- 賽默飛世爾科技公司
- 公司概況
- 商業策略
- 主要產品
- 財務業績
- 關鍵績效指標
- 風險分析
- 最新進展
- 區域影響力
- SWOT分析
- Emcure製藥股份有限公司
- 西格瑪奧德里奇公司
- 輝瑞公司
- 泰姬製藥有限公司
- 諾華國際股份公司
- 梯瓦製藥工業股份有限公司
- GE醫療
- 西門子醫療
- 飛利浦醫療保健
- 默克公司
- 霍夫曼-羅氏股份公司
- Arbor Pharmaceuticals, LLC
- 太陽製藥工業有限公司
- Amneal Pharmaceuticals. LLC
- 阿斯利康
- 凱瑞斯特里姆健康
- 基金會醫學公司
由於膠質瘤診斷和治療市場的產品範圍有限,主要企業正在積極探索新的方法,例如細胞療法,以擴展其產品組合。許多企業也致力於開發聯合療法,以提高現有藥物組合的療效和安全性。例如,2023年3月,諾華公司獲得FDA批准,將Tafinlar(達拉非尼)和Mekinist(曲美替尼)聯合用於治療1歲及以上攜帶BRAF V600E突變的低度膠質瘤患兒。這種聯合療法被認為是合適的選擇,可以滿足此類病例的全身性治療需求。這些藥理學先驅包括:
最新動態
- 2025年1月, Foundation Medicine的FoundationOneCDx獲得FDA批准,可作為OJEMDA(由Day One Biopharmaceuticals開發)的伴隨診斷解決方案。它可以提高使用II型RAF抑制劑治療兒童、復發性或難治性低度膠質瘤患者的療效。
- 2024年10月,賽默飛世爾科技公司獲得FDA批准,可在應用標靶治療前使用伴隨診斷試劑盒(CDx)Ion Torrent Oncomine Dx Target Test。此方法旨在識別或檢測12歲及以上患有2級IDH突變型膠質瘤的成人和兒童是否符合VORANIGO治療的條件。
- Report ID: 7379
- Published Date: Feb 25, 2026
- Report Format: PDF, PPT
- 探索关键市场趋势和洞察的预览
- 查看样本数据表和细分分析
- 体验我们可视化数据呈现的质量
- 评估我们的报告结构和研究方法
- 一窥竞争格局分析
- 了解区域预测的呈现方式
- 评估公司概况与基准分析的深度
- 预览可执行洞察如何支持您的战略
探索真实数据和分析
常见问题 (FAQ)
膠質瘤的診斷和治療 市场报告范围
免費樣本包含目前與歷史市場規模、成長趨勢、區域圖表與表格、公司概況、依細分市場的預測等內容。
聯絡我們的專家
版权所有 © 2026 Research Nester。保留所有权利。




